
题目列表(包括答案和解析)
8、室温下,某溶液中由水电离出的H+和OH-的物质的量浓度的乘积为1×10-28,满足此条件下的溶液中一定可以大量共存的离子组是( )
A.Fe2+、NO3-、Ba2+、Cl- B.Cl-、SO42-、K+、Na+
C.Fe3+、SO42-、MnO4-、Na+ D.Na+、K+、HCO3-、SO42-
7、根据热化学方程式:S(s) +O2(g)==SO2(g) △H=a kJ·mol-1(a=-297.2),下列说法中不正确的( )
A.S(s)在O2(g)中燃烧的反应是放热反应
B.S(g) +O2(g)==SO2(g) △H=b kJ·mol-1,则a<b
C.1 mol SO2(g)所具有的能量低于1 mol S(s)与1 mol O2(g)所具有的能量之和
D.16 g固体硫在氧气中充分燃烧,可放出148.6 kJ的热量
6、某氨水的pH=x,某盐酸的pH=y;已知x+y=14,且x<11;若将上述氨水与盐酸等体积混合后,所得溶液中各种离子浓度由大到小的排列顺序为( )
A.C(Cl-)>C(NH4+)>C(OH-)>C(H+) B.C(Cl-)>C(NH4+)>C(H+)>C(OH-)
C.C(NH4+)>C(Cl-)>C(H+)>C(OH-) D.C(NH4+)>C(Cl-)>C(OH-)>C(H+)
5、已知H2(g)、C2H4(g)和C2H5OH(l)的燃烧热分别为285.8kJ/mol;1411.0kJ/mol和1366.8kJ/mol,则由C2H4(g)和H2O (g)反应生成C2H5OH(l)的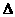 H为( )
H为( )
A.-44.2kJ/mol B.+44.2kJ/mol C.-330kJ/mol D.+330kJ/mol
4、下列说法正确的是( )
A.25℃时,pH为9的Na2CO3溶液和pH为5的FeCl3溶液中,水的电离程度不同
B.在含有Fe3+的KNO3溶液中,可通过加热的方法除去Fe3+,证明盐的水解是放热反应
C.25℃时,等体积等物质的量浓度的NaCl和NaClO溶液中所含离子总数相等
D.等物质的量浓度的①NH4Cl、②NH4HSO4、③Na2S、④NaNO3,其中pH由大到小的排列为:③>④>①>②
3、下列微粒对水的电离平衡无影响的是( )
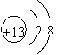
A.F- B. C.H2O D.HCl
2、已知室温时,0.1mol/L 某一元酸 HA在水中有0.1% 发生电离, 下列叙述错误的是( )
A.此酸的电离平衡常数为1×10-7 B.该溶液的pH=4
C.升高温度,溶液的pH增大
D.由HA电离出的C(H+)约为水电离出的C(H+)的106倍
1、下列离子方程式中,属于水解反应的是( )
A.HCOOH+H2O HCOO-+H3O+ B.CO2+H2O
HCOO-+H3O+ B.CO2+H2O HCO3-+H+
HCO3-+H+
C.CO32-+H2O HCO3-+OH- D.HS-+H2O
HCO3-+OH- D.HS-+H2O H3O++S2-
H3O++S2-
28.A是芳香烃的含氧衍生物。具有以下性质:(1)在一定温度和压强下将A气化,其气体的质量是同温同压下等体积氢气质量的76倍;(2)称取15.2gA,在0.85mol氧气中恰好完全燃烧,得到CO2和水蒸气的混合物,且两者的物质的量之比为2:1。请回答:
(1)试通过计算确定烃A的相对分子质量为 ,分子式是 。
(2)A遇三氯化铁溶液不变色,l mol A与足量金属钠作用能放出1 molH2,1 mol A最多只能与1 mol NaOH反应,若A苯环上的一元取代物共有三种, 则A的结构简式应为 。
昌化中学高二化学第二次月考
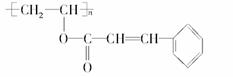
27.(10分)感光性高分子是一种在彩电荧光屏及大规律集成电路制造中应用较广的新型高分子材料。其结构简式为:
?
试回答下列问题:
(1)在一定条件下,该高聚物可发生的反应有(填写编号)________。
①加成反应 ②氧化反应 ③消去反应 ④酯化反应 ⑤取代反应
(2)该高聚物和NaOH溶液发生反应的化学方程式为
_____________________________________________________________________。
(3)该高聚物在催化剂和酸性环境下水解后得到相对分子质量较小的产物是A,则:
①A在一定条件下与甲醇发生反应的化学方程式为
_____________________________________________________________________。
②A的同分异构体有多种,其中与A不同类别且含有苯环、 ,苯环上有两个取代基的结构简式是(任写两种)
、
。
,苯环上有两个取代基的结构简式是(任写两种)
、
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com