
题目列表(包括答案和解析)
7.(12分)现有A、B、C三种烃,其球棍模型如下图: 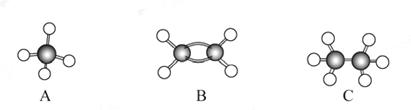
(1)等质量的以上物质完全燃烧时耗去O2的量最多的是_____ (填对应字母,下同);
(2)同状况、同体积的以上三种物质完全燃烧时耗去O2的量最多的是_____ ;
(3)等质量的以上三种物质燃烧时,生成二氧化碳最多的是_____ ,生成水最多的是_____ 。
(4)在120 ℃、1.01×105Pa下时,有两种气态烃和足量的氧气混合点燃,相同条件下测得反应前后气体体积没有发生变化,这两种气体是_____ 。


[实验·探究]
6.(6分)相对分子质量为72的烷烃,其分子式是____,
若此有机物的一氯代物分子中有两个-CH3,两个-CH2-, 一个 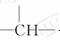 和一个-Cl,它的可能结构分别是____ 、 ____ 、 ____ 、 ____ 。
和一个-Cl,它的可能结构分别是____ 、 ____ 、 ____ 、 ____ 。
[解析]根据烷烃通式为CnH2n+2,相对分子质量
=14n+2=72,故n=5。由于含有一个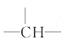 ,说明含有一个
,说明含有一个
支链,支链可以是甲基,也可以是Cl原子。
5.根据下表中烃的分子式排列规律,判断空格中烃的同分异构体数目是( )

A.3 B.4 C.5 D.6
[解析]选A。根据表中烃分子式排列规律,空格中烃分子式应为C5H12,其同分异构体有正戊烷、异戊烷和新戊烷。
4.下列各组物质不属于同系物的是( )
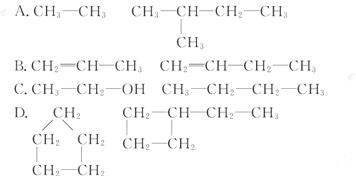
[解析]选C。结构相似,分子组成上相差一个或若干个CH2原子团的化合物互为同系物,故A、B、D均符合,而C项两者结构不相似,并且相差不是整数个CH2原子团,所以不属于同系物。
3.(2010·长春高一检测)已知丙烷的二氯代物有4种同分异构体,则其六氯代物的同分异构体的数目为( )
A.2种 B.3种 C.4种 D.5种 [[解析]选C。丙烷的分子式为C3H8,故C3H6Cl2与C3H2Cl6具有相同的同分异构体数,故选C。
2.有两种气态烷烃的混合物,在标准状况下其密度为 1.16 g·L-1 ,则关于该混合物组成的说法正确的是( )
A.一定有甲烷
B.一定有乙烷
C.不可能是甲烷和乙烷的混合物
D.可能是乙烷和丙烷的混合物
[解析]选A。两气态烷烃的平均相对分子质量为M=1.16×22.4=26>16,故混合气体中一定有甲烷,另一烷烃可能为乙烷、丙烷或丁烷,故A正确。
1.(2010·青岛高一检测)下列说法正确的是( )
A.碳碳间以单键结合,碳原子剩余价键全部与氢原子结合的烃一定是饱和链烃
B.分子组成符合CnH2n+2的烃一定是烷烃
C.正戊烷分子中所有碳原子均在一条直线上
D.新戊烷的一氯取代物有2种
[解析]选B。A项符合条件的烃为饱和烃,可为烷烃,也可为环烷烃,但分子组成符合CnH2n+2的烃一定为烷烃,故A错误,B正确;在烷烃分子中与碳原子紧邻的四个原子构成四面体形,所以正戊烷分子中所有碳原子呈锯齿形,而非直线形,C错误;新戊烷分子完全对称,分子中只有一种氢原子,故一氯取代物只有一种,D错误。
24.(12分)把煤作为燃料可通过下列两种途径:
途径I:C(s) +O2 (g) == CO2(g) △H1<0 ①
途径II:先制成水煤气:C(s) +H2O(g) == CO(g)+H2(g) △H2>0 ②
再燃烧水煤气:2CO(g)+O2 (g) == 2CO2(g) △H3<0 ③
2H2(g)+O2 (g) == 2H2O(g) △H4<0 ④
请回答下列问题:
(1)途径I放出的热量 ( 填“大于”“等于”或“小于”) 途径II放出的热量,原因是
。
(2)△H1、△H2、△H3、△H4的数学关系式是 。
(3)12g 炭粉在氧气中不完全燃烧生成一氧化碳,放出110.35kJ热量。其热化学方程式为 。
(4)煤炭作为燃料采用途径II的优点有
。
23. (8分)废旧印刷电路板的回收利用可实现资源再生,并减少污染。废旧印刷电路板经粉碎分离,能得到非金属粉末和金属粉末。
(8分)废旧印刷电路板的回收利用可实现资源再生,并减少污染。废旧印刷电路板经粉碎分离,能得到非金属粉末和金属粉末。
 (1)下列处理印刷电路板非金属粉末的方法中,不符合环境保护理念的是 (填字母)。
(1)下列处理印刷电路板非金属粉末的方法中,不符合环境保护理念的是 (填字母)。
 A.热裂解形成燃油 B.露天焚烧
A.热裂解形成燃油 B.露天焚烧
 C.作为有机复合建筑材料的原料 D.直接填埋
C.作为有机复合建筑材料的原料 D.直接填埋
 (2)用
(2)用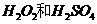 的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
的混合溶液可溶出印刷电路板金属粉末中的铜。已知:

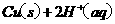 ====
====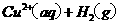
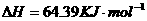

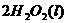 ====
====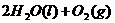
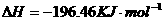

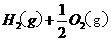 ====
==== 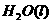
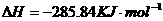
 在
在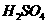 溶液中
溶液中 与
与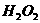 反应生成
反应生成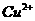 和
和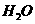 的热化学方程式为
的热化学方程式为
。
 (3)在298K下,C、Al的单质各1mol完全燃烧,分别放出热量aKJ和bKJ。又知一定条件下,Al能将C从CO2置换出来,写出此置换反应的热化学方程式
(3)在298K下,C、Al的单质各1mol完全燃烧,分别放出热量aKJ和bKJ。又知一定条件下,Al能将C从CO2置换出来,写出此置换反应的热化学方程式
22. (12分)2SO2(g)+O2(g)
=2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH=
-99kJ·mol-1。请回答下列问题:
(12分)2SO2(g)+O2(g)
=2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH=
-99kJ·mol-1。请回答下列问题:
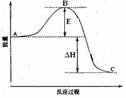
 (1)图中A、C分别表示
、
,E的大小对该反应的反应热 (填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点 ____________(填“升高”还是“降低”),△H
(填“变大”、“变小”或“不变”),理由是
(1)图中A、C分别表示
、
,E的大小对该反应的反应热 (填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点 ____________(填“升高”还是“降低”),△H
(填“变大”、“变小”或“不变”),理由是
 (2)图中△H=
KJ·mol-1;
(2)图中△H=
KJ·mol-1;
 (3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化为V2O5。写出该催化循环机理的化学方程式
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化为V2O5。写出该催化循环机理的化学方程式
、 。
 (4)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3
molSO3(g)的△H(要求计算过程)。
(4)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3
molSO3(g)的△H(要求计算过程)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com