
题目列表(包括答案和解析)
2.只用水就能鉴别的一组物质是
A.苯、乙酸、四氯化碳 B.乙醇、乙醛、乙酸
C.乙醛、乙二醇、硝基苯 D.苯酚、乙醇、甘油
1.下列关于烃的叙述中,正确的是
A.烃就是分子里含有碳原子的化合物
B.烃是指燃烧后生成二氧化碳和水的有机物
C.烃是指分子里含有碳、氢元素的化合物
D.烃是指仅由碳和氢两种元素组成的化合物
30、(10分)铁及铁的化合物在生产、生活中有着重要的用途。
(1)聚合硫酸铁(简称PFS)的化学式为 [ Fe (OH)n(S04) (3-n) / 2 ]m ,现代潜水处理工艺中常利用PFS在水体中形成絮状物,以吸附重金属离子。则PFS的中心原子未成对电子数为__ 个。
(2)六氰合亚铁酸钾K4[Fe(CN)6]可用做显影剂,该化合物中存在的化学键类型有_____ ____ 。
(3)CN一中碳原子的杂化轨道类型是 _______ :写出一种与CN一互为等电子体的分子的化学式_____ ___;
(4)三氯化铁常温下为固体,熔点304℃,沸点3160C 在3000C以上可升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁晶体为______ 晶体。
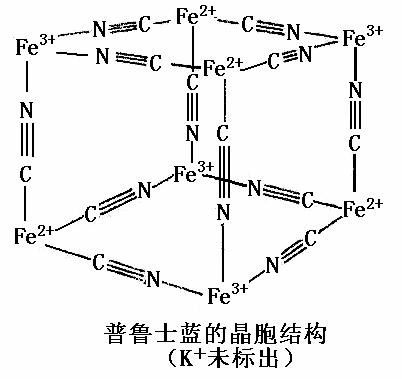
(5)普鲁士蓝是一种配合物,可用作染料,它的结构单元如下图所示,普鲁士蓝中 n(K+):n(Fe3+):n(Fe2+):n(CN一)= _____ ___。
29、(10分)下表是元素周期表的一部分。表中所列字母分别代表一种化学元素。
|
a |
|
|
|||||||||||||||
|
b |
|
|
|
c |
d |
e |
f |
|
|||||||||
|
g |
h |
i |
j |
|
k |
l |
m |
||||||||||
|
n |
|
|
|
|
|
|
o |
|
|
|
|
|
|
|
|
|
|
试回答下列问题:
 (1)请写出元素O的基态原子电子排布式
。
(1)请写出元素O的基态原子电子排布式
。
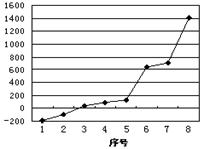
(2)第三周期8种元素按单质熔点高低的顺序如右图,其中序号“8”代表 (填元素符号);其中电负性最大的是 (填右图中的序号),
第一电离能最大的是 (填右图中的序号)。
(3)由j原子跟c原子以1 : 1相互交替结合而形成的晶体,晶体类型与晶体j相同。两者相比熔点更高的是 (填化学式),试从结构角度加以解释 。
(4)COCl2俗称光气,分子中C原子采取 杂化成键;分子中的共价键含有 (填标号)
a.2个σ键 b.2个π键 c.1个σ键、2个π键 d.3个σ键、1个π键
28、(16分) 已知 X、Y、Z、Q、R、E六种元素中,原子序数X<Y<Z<Q<R<E,其结构或性质信息如下表。
|
元素 |
结构或性质信息 |
|
X |
原子的L层上s电子数等于p电子数。 |
|
Y |
原子核外的L层有3个未成对电子。 |
|
Z |
在元素周期表的各元素中电负性仅小于氟。 |
|
Q |
单质常温、常压下是气体,原子的M层上有1个未成对的p电子。 |
|
R |
核电荷数是Y与Q的核电荷数之和 |
|
E |
原子序数比R大3 |
请根据信息回答有关问题:
(1)元素Y的原子核外共有 种不同运动状态的电子,有 种不同能级的电子。
(2) X、Y、Z三种元素的第一电离能由高到低的排列次序依次为(写元素符号) 。
(3)X、Z、Q元素均表现最低化合价时的三种氢化物中,沸点由高到低的排列次序依次为(写化学式) 。
(4)R的核外电子排布式为 。R的一种配合物的化学式为RCl3·6H2O。已知0.01 molRCl3·6H2O在水溶液中用过量硝酸银溶液处理,产生0.02 mol AgCl沉淀。此配合物最可能是 。
A.[R(H2O)6]Cl3 B.[R(H2O)5Cl]Cl2·H2O
C.[R(H2O)4Cl2]Cl·2H2O D.[R(H2O)3Cl3]·3H2O
(5)元素E能形成八面体构型的配合物离子[E (YH3) x Q 2]+,则中心原子为(写化学式) ,配位体为(写化学式) ,x 的值为 。
(6) Y的最低价氢化物与Z的一种氢化物反应,生成的两种产物均不污染环境,其反应的化学方程式为 。
27、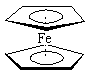 二茂铁[(C5H5)2Fe]
分子是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等。它的结构如右图所示,下列说法正确的是( )
二茂铁[(C5H5)2Fe]
分子是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等。它的结构如右图所示,下列说法正确的是( )
A.二茂铁中Fe2+与环戊二烯离子(C5H5-)之间为离子键
B.1mol环戊二烯(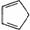 )中含有σ键的数目为5NA
)中含有σ键的数目为5NA
C.分子中存在π键
D.Fe2+的电子排布式为1s22s22p63s23p63d44s2
26、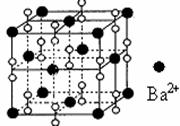 钡在氧气中燃烧时得到一种钡的氧化物晶体,结构如右图所示,有关说法不正确的是( )
钡在氧气中燃烧时得到一种钡的氧化物晶体,结构如右图所示,有关说法不正确的是( )
A.该晶体属于离子晶体
B.晶体的化学式为Ba2O2
C.该晶体晶胞结构与NaCl相似
D.与每个Ba2+距离相等且最近的Ba2+共有12个
25、X和Y是原子序数大于4的短周期元素,Xm+和Yn-两种离子的核外电子排布相同,下列说法中正确的是 ( )
A.第一电离能X<Y B.X的原子半径比Y小
C.电负性X>Y D.X和Y的核电荷数之差为m-n
24、 最近意大利罗马大学的科学家获得了极具理论研究意义的N4分子。N4分子结构如右图所示,已知断裂1 mol N-N吸收167
kJ热量,生成1 mol N
最近意大利罗马大学的科学家获得了极具理论研究意义的N4分子。N4分子结构如右图所示,已知断裂1 mol N-N吸收167
kJ热量,生成1 mol N N放出942 kJ热量,根据以上信息和数据,下列说法正确的是(
)
N放出942 kJ热量,根据以上信息和数据,下列说法正确的是(
)
A、N4属于一种新型的化合物
B、N4与N2互称为同位素
C、N4沸点比P4(白磷)高
D、1 mol N4气体转变为N2将放出882 kJ热量
23、用R代表短周期元素,R原子最外层的p能级上的未成对电子只有2个。下列关于R的描述中正确的是( )
A、R的氧化物都能溶于水
B、R的最高价氧化物对应的水化物都是H2RO3
C、R的氢化物中心原子的杂化方式都相同
D、R的氧化物都能与NaOH反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com