
题目列表(包括答案和解析)
19、在容积为2升的密闭容器中,有反应:
mA(g)+nB(g)  pC(g)+qD(g),经过5分钟达到平衡,此时,各物质的变化为:A减少了amol·L-1,B的平均反应速度VB=a/15mol·L-1·min-1,C增加了2a/3 mol·L-1,这时,若压缩容器的体积,发现A与C的百分含量不变,则m:n:p:q为( )
pC(g)+qD(g),经过5分钟达到平衡,此时,各物质的变化为:A减少了amol·L-1,B的平均反应速度VB=a/15mol·L-1·min-1,C增加了2a/3 mol·L-1,这时,若压缩容器的体积,发现A与C的百分含量不变,则m:n:p:q为( )
A.3:1:2:2 B.1:3:2:2 C.3:1:2:1 D.1:1:1:1
18、在Na2HPO4溶液中,存在着下列平衡:
HPO42- H++ PO43- HPO42-+H2O
H++ PO43- HPO42-+H2O H2PO4-+OH-
H2PO4-+OH-
已知该溶液呈碱性。欲使溶液中的HPO42-、H+ 、PO43-浓度都减小,可采取的方法是( )
A. 加石灰水 B. 加盐酸 C.加烧碱 D.用水稀释
17、室温下,给定的四组溶液,各组离子一定能够大量共存的是( )
A.使酚酞试液变红的溶液: Na+、Cl-、SO42-、Fe3+
B.水电离出来的c(H+)=10-13mol/L的溶液:K+、HCO3-、Br-、Ba2+
C.c(H+)=10-12 mol·L-1的溶液:K+、Ba2+、Cl-、Br-
D.所含溶质为Na2SO4的溶液:K+ 、HCO3-、NO3-、Al3+
16、将 a g 含NaOH样品溶解在 b mL 0.l mol·L-1 的硫酸中,再加入 c mL 0.1 mol·L-1 的氢氧化钡溶液,反应后所得溶液恰好呈中性,则样品中NaOH的纯度是( )
A.[(b-c)/125a]×100% B.[(b-2c)/125a]×100%
C.[(b-c)/250a]×100% D.[(8b-8c)/a]×100%
15、 下列事实不能用勒夏特列原理解释的是( )
A.打开碳酸饮料会有大量气泡冒出
B.用难溶FeS固体除去工业废水中的Pb2+
C.温度控制在500℃有利于合成氨反应
D.实验室用排饱和食盐水的方法收集氯气
14、用物质的量均是0.1 mol的CH3COOH和CH3COONa配成1L混合溶液,已知其中c(CH3COO-)大于c(Na+),对该混合溶液的下列判断正确的是( )
A.c(CH3COOH)>c(CH3COO-)
B.c(CH3COO-)+c(CH3COOH)=0.1 mol·L-1
C.c(H+)>c(OH-)
D.c(CH3COO-)+c(OH-)=0.1mol·L-1
13、向三份0.1 mol·L-1Na2CO3溶液中分别加入少量NH4NO3固体、NaHCO3固体、HCl气体(忽略溶液体积变化),则CO32-浓度的变化依次为( )
A.减小、增大、减小 B.增大、减小、减小
C.减小、增大、增大 D.增大、减小、增大
12、向某密闭容器中充入1 mol CO和2 mol H2O(g),发生反应:
CO+H2O(g) CO2+H2,当反应达到平衡时,CO的体积分数为x,若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于x的是( )
CO2+H2,当反应达到平衡时,CO的体积分数为x,若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于x的是( )
A.0.5 mol CO+2 mol H2O(g)+1 mol CO2+1 mol H2
B.1 mol CO+1 mol H2O(g)+1 mol CO2+1 mol H2
C.0.5 mol CO+1.5 mol H2O(g)+0.4 mol CO2+0.4 mol H2
D.0.5 mol CO+1.5 mol H2O(g)+0.5 mol CO2+0.5 mol H2
11、某学生用碱式滴定管量取0.1mol/L的NaOH溶液,开始时仰视液面,读数为11.00mL,取出部分溶液后,俯视液面,读数为19.00mL,实际取出液体的体积是 ( )
A.大于8.00mL B.小于8.00mL C.等于8.00mL D.无法确定
10、如图表示反应2 SO2(g)+ O2(g)  2 SO3(g) △H<0的正反应速率随时间的变化情况,试根据此曲线判断下列说法可能正确的是( )
2 SO3(g) △H<0的正反应速率随时间的变化情况,试根据此曲线判断下列说法可能正确的是( )
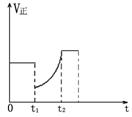 A.t1时减小了SO2 的浓度,增加了SO3的浓度,平衡向
A.t1时减小了SO2 的浓度,增加了SO3的浓度,平衡向
逆反应方向移动
B.t1时降低了温度,平衡向正反应方向移动
C.t1时减小了压强,平衡向逆反应方向移动
D.t1时增加了SO2 和O2的浓度,平衡向正反应方向移动
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com