
21.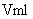 、
、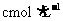 的
的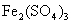 溶液恰好与25.00ml、0.1mol/L的盐酸羟胺[
溶液恰好与25.00ml、0.1mol/L的盐酸羟胺[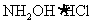 ]完全反应,
]完全反应,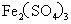 被还原成
被还原成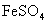 。用0.05
。用0.05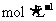 的酸性
的酸性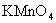 溶液滴定所得溶液,使
溶液滴定所得溶液,使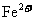 全部转化为
全部转化为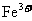 ,消耗了20ml,
,消耗了20ml,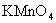 溶液。
溶液。
(1)写出酸性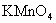 溶液与
溶液与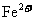 反应的离子方程式
反应的离子方程式
(2)盐酸羟胺被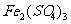 氧化后的氧化产物是 ,简单计算过程:
氧化后的氧化产物是 ,简单计算过程:
20.(20分)常见的粗盐主要含有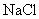 和少量的
和少量的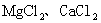 ,由于有
,由于有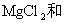
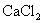 的存在,使得食盐容易板结,下面实验可以确定粗盐中
的存在,使得食盐容易板结,下面实验可以确定粗盐中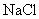 的质量分数,也可以制得纯净的
的质量分数,也可以制得纯净的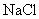 ,根据实验步骤填写下列空白:
,根据实验步骤填写下列空白:
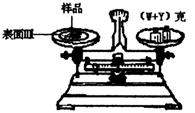
①调整托盘天平零点
②称取样品W克
③将样品溶解于适量的蒸馏水
④滴加稍过量的A溶液,有沉淀产生,沉淀完全后过滤
⑤将得到的滤渣用蒸馏水多次洗涤,烘干,得纯净固体W1克
⑥滤液中加入稍过量的B溶液,又待沉淀完全后过滤
⑦将⑥得到的滤渣用蒸馏水多次洗涤,烘干,得纯净固体W2克
⑧在再后得到的滤液中加入稍过量C溶液,加热蒸发溶剂得到纯净 固体W3克
固体W3克
问题:
(1)调整天平零点时,若指针偏向左边,应将左边的螺丝帽向(填左、右) 旋转。
(2)某学生用已知质量Y克的表面皿,准确称取W克样品,他在托盘天平的右盘上放入(W+Y)克砝码,在左盘的表面皿中加入样品,这时指针偏向右边(如图所示),这时样品的实际质量m (填>,<,=)W。
(3)加入的试剂A是 ,B是 ,C是 。
(4)检验步骤④中A是否过量的方法是 。
(5)过滤时,某学生的操作如图,明显的错误有 处。
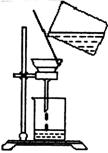
(6)两次洗涤沉淀,为了检验沉淀是否洗净,应在最后几滴洗出液中加入 ,
若 表示沉淀已洗净。
(7)该粗盐中 的质量分数的计算式是
。
的质量分数的计算式是
。
19.(8分)今有H2、O2、KOH溶液构成燃料电池,则正极通的气体应是 ,
负极电极反应式为 。
如把H2改为CH4,还是用KOH作导电解质,则电极反应式分别为
正极: 、负极 。
某一资料中记载着可以用电解KI水溶液的方法进行KIO3的工业化生产的信息,总的电解反应方程式为:KI+3H2O3=KIO3+3H2↑。
(1)椐此推测:
①阳极反应式是 ;
②阴极反应式是 。
(2)一位学生想用氢氧燃料电池来作电解KI水溶液进行KIO3的工业化生产的电源,工业生产1molKIO3,理论上需提供标准状况下的O2 L2、H2 L。
18.(16分)有机化合物A只含C、H两种元素,且其相对分子质量为56,与A相关的反应如下:
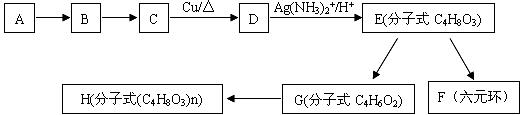
(1)指出反应类型:A→B E→F G→H
(2)写出E的含羟基和羟基所有同分异构体:
(3)写出反应方程式:(要求注明反应的条件)
①E→G
②E→F
③C与足量的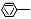 COOH
COOH
(4)H的一个链节中,最多 个原子处在同一个平面.
17.(10分)A、B、C、D、E、均为可溶于水的固体,所得的溶液只有E溶液有颜色。取一定量的固体C放在试管中用酒精灯加热,固体的质量会减少。组成这五种物质的离子有(各物质所含的离子均不相同)
|
阳离子 |
Na+ Mg2+ Al3+ Ba2+ Fe3+ |
|
阴离子 |
OH- Cl- 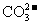 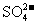 HCO3- HCO3- |
分别取它们的水溶液进行实验,结果如下:
①A溶液分别其他四种溶液反应,均有沉淀;
②B溶液分别与其四种溶液反应,也有沉淀;只是当B溶液加入到D溶液中时,先有沉淀继续加入B溶液时,沉淀会消失。
据此推断它们是A ;B ;C ;D ;E 。
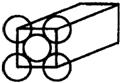
16、某金属晶体是面心立方体,立方体的每个面5个金属原子紧密堆砌(如图其余各面省略),金属原子半径为rcm,(设金属的相对原子质量为M),则该金属的密度为(设阿伏加德罗常数的符号为NA)( )
A、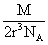
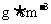 B、
B、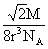
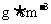
C、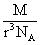
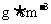 D、
D、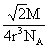
第Ⅱ卷(非选择题,共62分)
15、向NaBr、NaI、Na2SO3混合液中,通入一定量氯气后,将溶液蒸于并充分灼烧,得到固体剩余物质的组成可能是( )
A、NaCl B、NaCl 、Na2SO4
C、NaBr、Na2SO4 D、NaCl 、NaI、Na2SO4
14、工业上以硫铁矿为原料制硫酸所产生的尾气除了含有N2、O2外,还含有SO2。为了便于监控,实施环境保护,下列适合测定硫酸尾气SO2含量的是( )
A、品红溶液 B、氨水、酚酞试液
C、碘水、淀粉溶液 D、以上都能
13、下列物质性质的变化规律,与键的健能大小无关的是( )
A、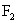 、
、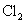 、
、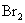 、
、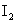 的熔点、沸点逐渐升高
的熔点、沸点逐渐升高
B、HF、HCl、HBr、HI的热稳定性依次减弱
C、金刚石的硬度、熔点、沸点都高于晶体硅
D、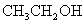 、
、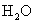 、
、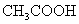 与Na反应由难到易
与Na反应由难到易
12、在常温常压下呈气态的化合物,降温使其固化得到的晶体属于( )
A、分子晶体 B、原子晶体
C、离子晶体 D、何种晶体无法判断
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com