
27.(15分)下图表示各物质之间的转化关系。已知:A、D、F、H均为单质,X常温下为无色液体,B为淡黄色固体,J溶于酸得到黄色溶液。
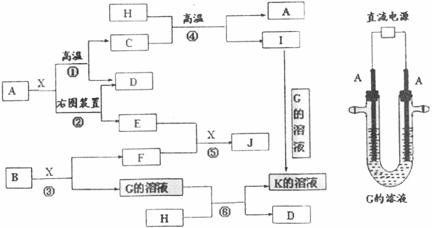
请按要求填空:
(1)写出B的电子式: 。
(2)写出生成E的电极反应式: ,反应⑤的现象是 。
(3)反应①的化学方程式是 ,在实验室中引发反应④的操作是 。
(4)反应⑥的离子方程式是 。
26.(15分)过氧乙酸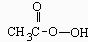 是广为使用的消毒剂。它可由
是广为使用的消毒剂。它可由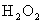 和冰醋酸反应制取,所以在过氧乙酸中常含有残留的
和冰醋酸反应制取,所以在过氧乙酸中常含有残留的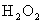 。测定产品中过氧乙酸浓度
。测定产品中过氧乙酸浓度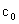 的方法和步骤如下:
的方法和步骤如下:
取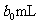 待测液,用硫酸使溶液酸化,再用浓度为
待测液,用硫酸使溶液酸化,再用浓度为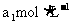 的
的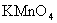 标准溶液滴定其中的
标准溶液滴定其中的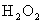 ,耗用
,耗用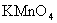 溶液的体积为
溶液的体积为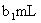 。(该反应记为①,滴定过程中
。(该反应记为①,滴定过程中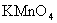 不与过氧乙酸反应,
不与过氧乙酸反应,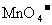 的还原产物是
的还原产物是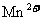 )。
)。
另取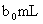 待测液。加入过量的
待测液。加入过量的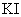 ,并用硫酸使溶液酸化,此时过氧乙酸和残留的
,并用硫酸使溶液酸化,此时过氧乙酸和残留的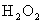 都能跟
都能跟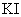 反应生成
反应生成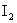 (前后两个反应分别记为②和③)。再用浓度为
(前后两个反应分别记为②和③)。再用浓度为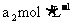 的
的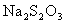 标准溶液滴定生成的
标准溶液滴定生成的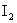 ,耗用
,耗用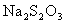 溶液体积为
溶液体积为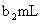 (反应④
(反应④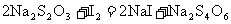 )。
)。
(1)写出上述反应①、②、③的离子反应方程式
① ② ③ 。
(2)用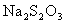 标准溶液滴定
标准溶液滴定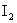 时,选用的指示剂是
。
时,选用的指示剂是
。
请根据上述实验数据计算过氧乙酸的浓度(用含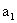 、
、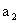 、
、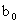 、
、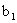 、
、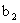 的代数式表示)
的代数式表示)
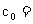 。
。
(3)为计算待测液中过氧乙酸的浓度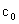 ,加入的
,加入的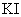 的质量已过量但没有准确称量,是否影响测定结果
(填“是”或“否”)。
的质量已过量但没有准确称量,是否影响测定结果
(填“是”或“否”)。
13.常温下,向一定体积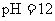 的
的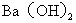 溶液中,逐滴加入一定物质的量浓度的
溶液中,逐滴加入一定物质的量浓度的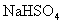 溶液,当溶液中的
溶液,当溶液中的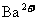 恰好完全沉淀时,溶液
恰好完全沉淀时,溶液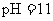 。若反应后溶液的体积等于
。若反应后溶液的体积等于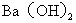 溶液与
溶液与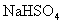 溶液体积之和,则
溶液体积之和,则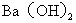 溶液和
溶液和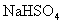 溶液的体积之比是:
溶液的体积之比是:
A.1:9 B.1:1 C.1:2 D.1:4
非选择题共10大题,共174分
12.由短周期元素构成的某离子化合物中,一个阳离子和一个阴离子核外电子数之和为20。下列说法中正确的是( )
A.晶体中阳离子和阴离子个数一定相等
B.晶体中一定含有离子键,可能含有共价键
C.所含元素一定不在同一周期,也不在第一周期
D.晶体中阳离子半径一定大于阴离子半径
11.I、在一定温度下,向一个容积不变的容器中,加入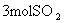 和
和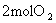 及固体催化剂,使之发生反应:
及固体催化剂,使之发生反应: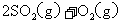

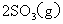 ;
;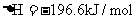 。平衡时容器内气体压强为起始时的90%。
。平衡时容器内气体压强为起始时的90%。
Ⅱ、保持同一反应温度,在相同容积的容器中,将起始物质的量改为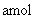
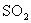 、
、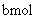
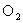 、
、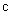
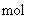
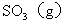
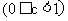 ,反应达到平衡时
,反应达到平衡时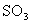 的体积分数为
的体积分数为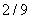 。I与Ⅱ放出的热量比较正确的是( )
。I与Ⅱ放出的热量比较正确的是( )
A.一定相等 B.前者一定小于后者
C.前者大于或等于后者 D.前者小于或等于后者
10.将一定体积的某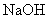 溶液分成两等份。一份用
溶液分成两等份。一份用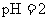 的一元酸
的一元酸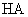 溶液中和,消耗酸溶液的体积为
溶液中和,消耗酸溶液的体积为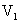 ;另一份用
;另一份用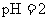 的一元酸
的一元酸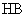 溶液中和,消耗酸溶液体积为
溶液中和,消耗酸溶液体积为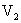 ,则下列叙述正确的是( )
,则下列叙述正确的是( )
A.若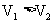 ,则说明
,则说明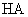 的酸性比
的酸性比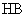 的酸性弱
的酸性弱
B.若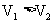 ,则说明
,则说明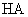 的酸性比
的酸性比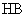 的酸性强
的酸性强
C.因为两种酸溶液的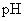 相等,故
相等,故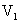 一定等于
一定等于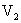
D.若将两种酸溶液等体积混合,混合溶液的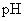 一定等于2
一定等于2
9.将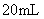
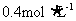 硝酸铵溶液与
硝酸铵溶液与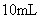
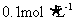 氢氧化钡溶液混合,则混合后溶液中各离子浓度的大小顺序是( )
氢氧化钡溶液混合,则混合后溶液中各离子浓度的大小顺序是( )
A.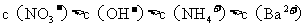
B.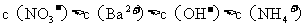
C.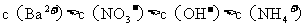
D.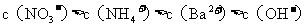
8.已知反应:①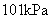 时,
时,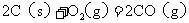 ;
;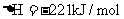 ②稀溶液中,
②稀溶液中,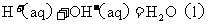 ;
;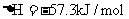 下列结论正确的是( )
下列结论正确的是( )
A.碳的燃烧热大于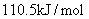
B.①的反应热为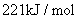
C.稀硫酸与稀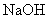 溶液反应的中和热为
溶液反应的中和热为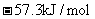
D.稀醋酸与稀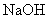 溶液反应生成
溶液反应生成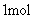 水,放出
水,放出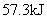 热量
热量
7.下列说法正确的是( )
A.I A族元素的金属性比ⅡA族元素的金属性强
B.ⅥA族元素的氢化物中,稳定性最好的其沸点也最高
C.同周期非金属氧化物对应的水化物的酸性从左到右依次增强
D.同周期元素的离子半径从左到右逐渐减小
6.甲、乙为短周期不同主族元素组成的单质,丙、丁为氧化物。它们存在如下转化关系: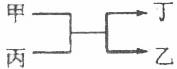 。组成单质甲、乙的元素分别为( )
。组成单质甲、乙的元素分别为( )
A.铝和铁 B.氟和氧 C.碳和氢 D.碳和硅
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com