
20£Æœ¬¡–Àµ∑®÷–’˝»∑µƒ «(°°°° )
A£Æ∏…±˘∆¯ªØ∫ÕI2…˝ª™øÀ∑˛µƒ◊˜”√¡¶œýÕ¨
B£ÆΩ ÙµºµÁµƒ µ÷ «Ω ٗٿÎ◊”‘⁄Õ‚µÁ≥°◊˜”√œ¬µƒ∂®œÚ“∆∂Ø
C£Æ¬»ªØƒ∆∫Õ¬»ªØ«‚»Ð”⁄ÀÆ ±£¨∆∆ªµµƒªØ—ߺ¸∂º «¿Î◊”º¸
D£Æ”√◊˜∏þŒ¬Ω·ππÃ’¥…≤ƒ¡œµƒSi3N4πÃà«∑÷◊”æßÃÂ
19£Æœ¬√ʵƒ≈≈–Ú≤ª’˝»∑µƒ «°°°°°°°°°° (°° °°)
A£Ææßû€µ„”…µÕµΩ∏þ£∫CF4<CCl4<CBr4<CI4°°
B£Æ»€µ„”…∏þµΩµÕ£∫Na>Mg>Al
C£Æ”≤∂»”…¥ÛµΩ–°:Ω∏’ Ø>úªØπË>æßÃÂπË°°
D£Ææß∏҃Д…¥ÛµΩ–°: NaF> NaCl> NaBr>NaI
18£Æœ¬¡–”–πÿ– ˆ’˝»∑µƒ «(°°°° )
A£Æ«‚º¸ «“ª÷÷Ãÿ ‚ªØ—ߺ¸£¨À¸π„∑∫µÿ¥Ê‘⁄”⁄◊‘»ªΩÁ÷–
B£Æ‘⁄--COOH∑÷◊”÷–∫¨”–1∏ˆ ÷–‘C‘≠◊”
C£Æµ‚µ•÷ ‘⁄ÀƻГ∫÷–»ÐΩ‚∂»∫Ж° «“ÚŒ™I2∫ÕH2O∂º «∑«º´–‘∑÷◊”°£
D£Æ∫¨—ıÀ·ø…”√Õ® ΩXOm(OH)n¿¥±Ì 棨»Ùn÷µ‘Ω¥Û£¨‘Ú∫¨—ıÀ·µƒÀ·–‘‘Ω¥Û
17£ÆœÚ ¢”–¡ÚÀ·Õ≠ÀƻГ∫µƒ ‘πпԺ”»Î∞±ÀÆ£¨ ◊œ»–Œ≥…ƒ—»ÐŒÔ£¨ºÃ–¯Ã̺”∞±ÀÆ£¨ƒ—»ÐŒÔ»ÐΩ‚µ√µΩ…Ó¿∂…´µƒÕ∏√˜»Ð“∫°£œ¬¡–∂‘¥Àœ÷œÛÀµ∑®’˝»∑µƒ «(°°°° )
A£Æ∑¥”¶∫ۻГ∫÷–≤ª¥Ê‘⁄»Œ∫Œ≥¡µÌ£¨À˘“‘∑¥”¶«∞∫Û≈‰¿Î◊”µƒ÷÷¿ý≤ª±‰
B£Æ≥¡µÌ»ÐΩ‚∫Û£¨Ω´…˙≥……Ó¿∂…´µƒ≈‰¿Î◊”[Cu(H2O)4] 2+
C£Æ‘⁄[Cu(NH3)4] 2+¿Î◊”÷–£¨Cu2+÷π©ø’πϵ¿£¨NH3∏¯≥ˆπ¬∂‘µÁ◊”
D£Æ≈‰ŒªÃ–Œ≥…≈‰Œªº¸µƒƒÐ¡¶£∫H2O> NH3
16£Æœ¬¡–Àµ∑®÷–’˝»∑µƒ «(°°°° )
A£Æ∑«Ω Ù‘™Àÿ≥ œ÷µƒ◊Ó∏þªØ∫œº€≤ª≥¨π˝∏√‘™Àÿ‘≠◊”µƒ◊ÓÕ‚≤„µÁ◊” ˝
B£ÆÕ¨÷Ð∆⁄‘™Àÿµƒ‘≠◊”∞Îæ∂¥”◊ÛµΩ”“÷Ω•‘ˆ¥Û£¨π µÁ∏∫–‘±ÿ“¿¥Œºı–°
C£Æ◊ÓÕ‚≤„”–2∏ˆµÁ◊”µƒ‘≠◊”∂º «Ω Ù‘≠◊”,◊ÓÕ‚≤„”–5∏ˆµÁ◊”µƒ‘≠◊”∂º «∑«Ω Ù‘≠◊”
D£ÆÕ¨÷Ð∆⁄‘™Àÿµƒ∑«Ω Ù–‘÷Ω•‘ˆ¥Û£¨π ú‘™Àÿµƒµ⁄“ªµÁ¿ÎƒÐ¥Û”⁄µ™‘™Àÿµƒµ⁄“ªµÁ¿ÎƒÐ
15£Æœ¬±ÌŒ™‘™Àÿ÷Ð∆⁄±Ì«∞Àƒ÷Ð∆⁄µƒ“ª≤ø∑÷£¨œ¬¡–”–πÿR°¢W°¢X°¢Y°¢ZŒÂ÷÷‘™Àÿµƒ– ˆ÷–£¨’˝»∑µƒ «(°°°° )
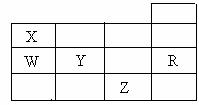
°° °°°°A£Æ≥£—πœ¬ŒÂ÷÷‘™Àÿµƒµ•÷ ÷–£¨Zµ•÷ µƒ∑–µ„◊Ó∏þ
B£ÆR◊ÓÕ‚≤„µÁ◊”≈≈≤ºŒ™2s22p6£¨µ⁄“ªµÁ¿ÎƒÐΩœ¥Û
C£Æ”…”⁄X∂‘”¶µƒ∆¯Ã¨«‚ªØŒÔ¥Ê‘⁄∑÷◊”º‰µƒ«‚º¸,π ∑–µ„∏þ”⁄W∂‘”¶µƒ∆¯Ã¨«‚ªØŒÔµƒ∑–µ„
D£Æ◊Ó∏þº€—ıªØŒÔ∂‘”¶µƒÀƪ،ԵƒÀ·–‘£∫Y<W
14£Æœ¬¡–ŒÔ÷ µƒ¡¢ÃÂΩ·ππ”ÎNH3œýÕ¨µƒ «(°° °°)
A£ÆH2O°°°°°° °°°°°° B£ÆH3O+°°°° °°°° C£ÆCH4°°°°°° D£ÆCO2
13£Æœ¬¡–ªØ—ß Ω÷–£¨ƒÐ’Ê µ±Ì æŒÔ÷ µƒ∑÷◊”◊È≥…µƒ «(°° °°)
A£ÆNaCl°°°° °°°°°° B£ÆCO2 °°°°°°°°°° C£ÆSiO2°°°° °°°°D£ÆCsCl°°
12£Æ‘⁄œ¬¡–ªØ—ß∑¥”¶÷–£¨º»”–¿Î◊”º¸°¢º´–‘º¸°¢∑«º´–‘º¸∂œ¡—£¨”÷”–¿Î◊”º¸°¢º´–‘º¸°¢∑«º´ –‘º¸–Œ≥…µƒ «(°° °°)
A£ÆCl2+H2O=HCl+HClO°°°°°° °°°°°°°°°°°°°° B£Æ2Na2O2+2CO2=2Na2CO3+O2
C£ÆMg3N2+6H2O=3Mg(OH)2°˝+2NH3°¸°° °° D£ÆNaOH+HNO3=NaNO3+H2O
11£Æœ¬¡–∑÷◊”÷–£¨À˘”–‘≠◊”∂º¬˙◊„◊ÓÕ‚≤„Œ™8µÁ◊”Ω·π𵃠«(°° °°)
A£ÆXeF2 °°°°°°°°°° B£ÆBCl3 °°°°°°°°°°°°°°°°°°°° C£ÆHClO°°°°°° °° D£ÆCF2Cl2
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com