
30.(11分)氧化还原反应中实际上包含有氧化和还原两个过程,下面是一个还原过程的反应式:
NO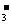 +H+→NO+H2O;现有KMnO4、Na2CO3、Cu2O、Fe2(SO4)3几种物质中的一种物质(A)能使上述还原过程发生。
+H+→NO+H2O;现有KMnO4、Na2CO3、Cu2O、Fe2(SO4)3几种物质中的一种物质(A)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的离子方程式,并标出电子转移的方向和数目
。
(2)上述反应中体现出了硝酸的 性质;
(3)反应中若产生0.1mol气体,则未被还原的硝酸的物质的量为 ;
(4)若1molA物质与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是
。
29.(15分)下图中所有物质均为中学化学常见物质,X含有四种元素,F、H是气体单质,Z是固体金属单质,Y中阳离子与阴离子个数比为2:1,化合物X、Y、A、D、E、G的焰色反应为黄色。I是白色沉淀,既能溶于盐酸,也可溶于强碱。
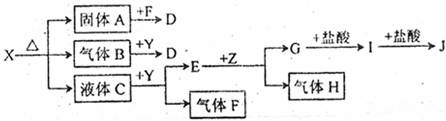
(1)写出X、E、I的化学式。X E I
(2)关于Y的说法正确的是
A.Y是氧化物 B.Y是过氧化物
C.Y是强电解质 D.Y是碱性氧化物
(3)写出B和Y反应的化学方程式:
(4)X和G的溶液能反应吗?如能反应,写出反应的离子方程式;如不能反应,请说明理由。
28.(15分)(I)A、B、C、D、E五种短周期主族元素的原子序数依次增大,且知:
①其原子半径大小关系是D>E>B>C>A;
②A、D同主族,B、C、E分处三个连续的主族,且最外层电子数依次增加;
③C是地壳中含量最多的元素。
请填写以下空白:
(1)用电子式表示C与D形成化合物的过程 。
(2)若适量气体A和1.4g气体B在一定条件下完全反应生成气态产物放出4.62kJ的热量,请写出该反应的热化学方程式: 。
(3)单质E与A、C、D三种元素形成的化合物反应的化学方程式为: 。
(II)不同元素的原子在分子内吸收电子的能力大小可用一定数值x来表示,若x越大,其原子吸引电子能力越强,在所形成的化合物中成为带负电荷的一方。
下面是某些短周期元素的x值:
|
元素符号 |
Li |
Be |
B |
C |
O |
F |
Na |
Al |
Si |
P |
S |
Cl |
|
x值 |
0.98 |
1.57 |
2.04 |
2.25 |
3.44 |
3.98 |
0.93 |
1.61 |
1.90 |
2.19 |
2.58 |
3.16 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(1)通过分析x值变化规律,确定Mg的x值范围: <x(Mg)< 。
(2)推测x值与原子半径的关系是:原子半径越大,x值 (“越大”或“越小”)
短周期元素的x值变化特点,体现了元素性质的 变化规律。
27.(19分)某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。
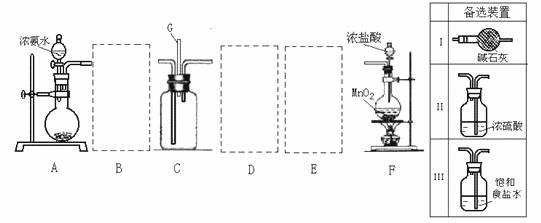
请回答下列问题:
(1)装置F中发生反应的离子方程式 。
(2)装置A中的烧瓶内固体宜选用 (选填以下选项的代号)
A.碱石灰 B.生石灰 C.二氧化硅 D.五氧化二磷 E.烧碱
(3)虚线框内应添加必要的除杂装置,请从上图的备选装置中选择。并将编号填入下列空格。
B__________、D__________、E__________(填编号)
(4)在常温下装置C内出现浓厚的白烟并在容器的内壁凝结,同时生成另一种无色无味的气体,该反应的化学方程式为: ;请设计一个实验方案鉴定该装置C内现出浓厚的白烟的成份: 。
13.将4.34gNa、Na2O、Na2O2的混合物与足量的水反应,在标准状况下得到672mL混合气体,将该混合气体通过放电,恰好完全反应,则它们的物质的量之比为 ( )
A.1:1:1 B.1:1:2 C.4:3:2 D.1:2:1
第Ⅱ卷
12.继科学家发现C3O2是金星大气成分之后,2004年,美国科学家通过“勇气”号太空车探测出水星大气中含有一种称为硫化羰(化学式为COS)的物质,已知硫化羰与二氧化碳的结构相似,但在氧气中会燃烧,下列有关C3O2与硫化羰的说法中不正确的是( )
A.C3O2与CO一样可以在氧气中燃烧生成CO2
B.C3O2、CO、CO2都有碳的氧化物,它们互为同素异形体
C.COS是由极性键构成的极性分子,分子中所有原子都满足8电子稳定结构
D.硫化羰在氧气中完全燃烧后的生成物是CO2和SO2
11.已知某溶液中存在较多的H+、SO2-4、NO-3,则溶液中还可能大量存在的离子组是( )
A.Na+、NH+4、Cl- B.Al3+、CH3COO-、Cl-
C.Mg2+、Cl-、Fe2+ D.Mg2+、Ba2+、Br-
10.下列有关元素周期表的说法正确的是 ( )
A.元素周期表包括7个周期,18个族
B.最活泼的非金属元素位于周期表的第15纵行
C.第五周期共包含18种元素
D.82号元素Pb位于周期表的第六周期第IV族
9.下列离子方程式中,正确的是 ( )
A.向饱和澄清石灰水中加入纯碱溶液:Ca(OH)2+CO2-3==CaCO3↓+2OH-
B.将铜片加入到稀硝酸中:Cu+8H++2NO-3==Cu2++2NO↑+4H2O
C.次氯酸钙溶液中通入少量二氧化硫:Ca2++2ClO-+H2O+SO2==CaSO3↓+2HClO
D.用NaOH溶液吸收过量的硫化氢气体:OH-+H2S==HS-+H2O
8.某密闭绝热容器中盛有饱和Ca(OH)2溶液,当加入少量CaO粉末时,下列说法正确的是
( )
①有固体析出 ②Ca(OH)2浓度增大 ③pH一定不变
④C(H+)·C(OH-)的积不变 ⑤C(H+)增大
A.① B.①③ C.②④ D.①⑤
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com