
(二)典型例题
例1:已知B、C是两个定点,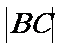 =8,且
=8,且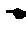 ABC的周长等于18,求这个三角形的顶点A的轨迹方程。
ABC的周长等于18,求这个三角形的顶点A的轨迹方程。
例2:已知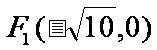
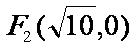 分别是椭圆的左右焦点,P是椭圆上的点,满足P
分别是椭圆的左右焦点,P是椭圆上的点,满足P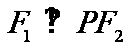 ,
,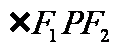 的平分线交
的平分线交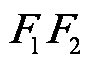 于M(
于M(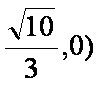 ,求椭圆方程。
,求椭圆方程。
例3:已知P点在以坐标轴为对称轴的椭圆上,点P到两个焦点的距离分别是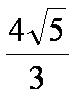 和
和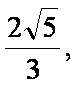 过P作焦点所在轴的垂线恰好过椭圆的一个焦点,求椭圆的方程。
过P作焦点所在轴的垂线恰好过椭圆的一个焦点,求椭圆的方程。
例4:设P(X、Y)是椭圆 的点,且P的纵坐标Y
的点,且P的纵坐标Y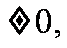 点A(-5、0)、
点A(-5、0)、
B(5、0),试判断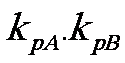 是否为定值?若是定值,求出该定值,若不是定值,说明理由。
是否为定值?若是定值,求出该定值,若不是定值,说明理由。
四:学生练习:
1、 椭圆5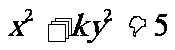 的一个焦点是(0,2),则K=
。
的一个焦点是(0,2),则K=
。
2、 设椭圆的两个焦点分别为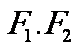 ,过
,过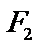 作椭圆长轴的垂线交椭圆于点P,若
作椭圆长轴的垂线交椭圆于点P,若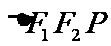 为等腰直角三角形,则椭圆的离心率为------------------。
为等腰直角三角形,则椭圆的离心率为------------------。
3、 若椭圆的长轴长与短轴长之比为2:1,它的一个焦点是(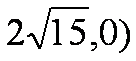 ,则椭圆的标准方程为------------------。
,则椭圆的标准方程为------------------。
4、 设椭圆的中心是坐标原点,长轴在X轴上,离心率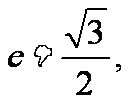 已知点P(0,
已知点P(0, 到这个椭圆上的点的最远距离是
到这个椭圆上的点的最远距离是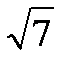 ,求这个椭圆方程。
,求这个椭圆方程。
五:小结后布置作业、P31 6、 8、 10
(一)、复习回顾:
(1) 椭圆的定义
(2) 椭圆的标准方程
(3) 椭圆的几何性质:
1.范围:
椭圆位于直线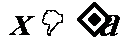 和
和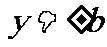 所围成的矩形里.
所围成的矩形里.
原因:由标准方程可知,椭圆上的点的坐标(x,y)都适合不等式
即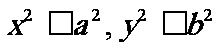 ,
,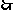
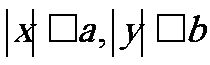
2.对称性:
从图形上看:椭圆关于x轴、y轴、原点对称。
从方程上看:
(1)把x换成-x方程不变,图象关于y轴对称;
(2)把y换成-y方程不变,图象关于x轴对称;
(3)把x换成-x,同时把y换成-y方程不变,图象关于原点成中心对称。
3.顶点:
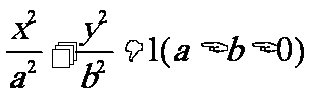
令 x=0,得 y=?,说明椭圆与 y轴的交点?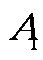 (-a,0),
(-a,0),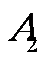 (a,0)
(a,0)
令 y=0,得 x=?说明椭圆与 x轴的交点?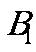 (0,-b),
(0,-b), 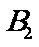 (0,b)
(0,b)
(1)顶点:椭圆与它的对称轴的四个交点,叫做椭圆的顶点。
(2)长轴、短轴:线段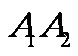 、线段
、线段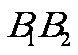 分别叫椭圆的长轴和短轴,它们的长分别等于2a和2b;
分别叫椭圆的长轴和短轴,它们的长分别等于2a和2b;
(3)a、b的几何意义:a是长半轴的长,b是短半轴的长;
4.离心率:
椭圆的焦距与长轴长的比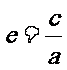 ,叫做椭圆的离心率.
,叫做椭圆的离心率.
说明①因为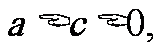 所以
所以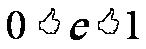 .
.
②e越接近1,则c越接近a,从而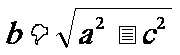 越小,因此椭圆越扁;反之,e越接近于0,c越接近于0,从而b越接近于a,这时椭圆就接近于圆;
越小,因此椭圆越扁;反之,e越接近于0,c越接近于0,从而b越接近于a,这时椭圆就接近于圆;
③当且仅当a=b时,c=0,这时两焦点重合,图形变为圆.
[对于上述性质要求学生熟练掌握,并能由此推出焦点在y轴的椭圆标准方程的几何性质(要求学生自己归纳),并能根据椭圆方程得到相应性质.
2.掌握椭圆标准方程中a、b、c关系;
1.掌握椭圆的几何性质:范围、对称性、顶点、长轴、短轴、离心率;
14. 已知某纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用右图中的装置进行实验。
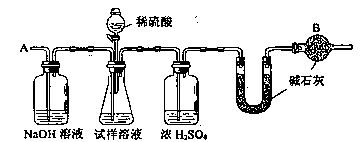
主要实验步骤如下:
① 按图组装仪器,并检验装置的气密性
② 将a g试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液
③ 称量盛有碱石灰的U型管的质量,得到b g
④ 从分液漏斗滴入6mol·L-1的硫酸,直到不再产生气体时为止
⑤ 从导管A处缓缓鼓入一定量的空气
⑥ 再次称量盛有碱石灰的U型管的质量,得到c g
⑦ 重复步骤⑤和⑥的操作,直到U型管的质量基本不变,为d g
请填空和回答问题:
⑴ 在用托盘天平称量关品时,如果天平的指针向左偏转,说明________________________。
⑵ 装置中干燥管B的作用是___________________________________________。
⑶ 如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果_________________(填偏高、偏低或不变)。
⑷ 步骤⑤的目的是__________________________________________。
⑸ 步骤⑦的目的是__________________________________________。
⑹ 试样中纯碱的质量分数的计算式为___________________。
⑺ 还可以用其它实验方法测定试样中纯碱的质量分数。请简述一种不同的实验方法。
13. 现有一定量含有Na2O杂质的Na2O2试样.请从图4-3中选用适当的实验装置,设计一个最简单的实验,则定Na2O2试样的纯度(可供选用的反应物只有CaCO3固体,6mol/L盐酸和蒸馏水).
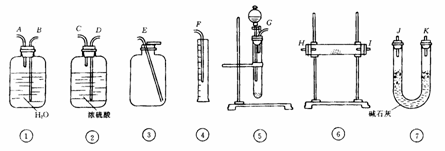
图4-3
请填写下列空白
(1)写出在实验中Na2O2和Na2O分别发生反应的化学方程式 , .
(2) 应选用的装置是(只要求写出图中装置的标号) .
(3)所选用装置的连接顺序应是(填各接口的字母,连接胶管省略)
12. 海水占地球总储水量的97.2%。若把海水淡化和化工生产结合起来
(1)海水中含有大量的氯化钠。氯化钠中的金属元素位于元素周期表第 族。
(2)目前国际上实用的“海水淡化”主要技术之一是蒸馏法。蒸馏法是将海水变成蒸汽,蒸汽经过冷却而得高纯度淡水,由此可判断蒸馏法是 (填物理变化、化学变化)
(3)工业上利用电解饱和食盐水可制得重要化工产品,反应式为:
 食盐+H2O NaOH+H2+Cl2(未配平)。该反应中食盐的化学式是_______________。利用电解所得气体制36.5%的浓盐酸1000t,最少需要消耗食盐
t。
食盐+H2O NaOH+H2+Cl2(未配平)。该反应中食盐的化学式是_______________。利用电解所得气体制36.5%的浓盐酸1000t,最少需要消耗食盐
t。
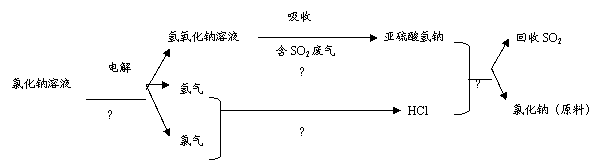 (4)近年来有人提出了一种利用氯碱工业产品及氯化钠循环治理含二氧化硫废气并回收二氧化硫的方法,该方法的流程如下:
(4)近年来有人提出了一种利用氯碱工业产品及氯化钠循环治理含二氧化硫废气并回收二氧化硫的方法,该方法的流程如下:
写出②④的化学反应方程式:
⑸ 上述亚硫酸氢钠与甲醛经过一定反应,可以合成俗称“吊白块”(雕白粉)的物质。因吊白块对人体有害,不能用于食品漂白。其结构简式为:HOCH2SO3Na,根据其结构特点,吊白块能发生的反应有:
A.皂化反应 B.聚合反应 C.与金属钠反应 D.氧化反应
11. 有M,R,Q,V,W,X,Y,Z八种物质,它们之间存在如下关系:
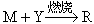 ‚
‚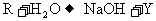 ƒ
ƒ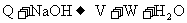
„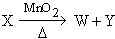
…
其M、Q、Y是单质,Q、Y在常温、常压下为气体,Z是硫酸盐,钠、钾化合物性质相似。
回答下列问题:
(1)写出各代号的化学式(或分子式)
M , R ,Q ,V ,W ,X ,
Y ,Z
(2)写出下列有关化学反应的方程式和离子方程式,并标出电子转移方向和总数
反应ƒ , 反应… ,
10、下列有碱金性铷(Rb)的叙述中,正确的是
A.灼烧氯化铷时,火焰有特殊颜色 B.硝酸铷是离子化合物,易溶于水
C.在钠、钾、铷三种单质中,铷的熔点最高 D.氢氧化铷是弱碱
9、将CO2分别通入下列各溶液中,不可能产生沉淀的是
A.CaCl2溶液 B.石灰水 C.饱和Na2CO3溶液 D.BaCl2溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com