
23ЁЂ(8Зж)гУ6 mol/L ЕФСђЫсХфжЦ100 mL 1.0 mol/L СђЫсЃЌШєЪЕбщвЧЦїгаЃК
AЃЎ100 mLСПЭВЁЁ BЃЎЭаХЬЬьЦНЁЁ CЃЎВЃСЇАєЁЁ DЃЎ50 mLШнСПЦПЁЁEЃЎ20 mL СПЭВ
FЃЎНКЭЗЕЮЙмЁЁ GЃЎ50 mLЩеБЁЁ HЃЎ100 mLШнСПЦП
(1)ЪЕбщЪБгІбЁгУвЧЦїЕФЪЧ(ЬюШыБрКХ)_________________________ЁЃ
(2)дкШнСПЦПЕФЪЙгУЗНЗЈжаЃЌЯТСаВйзїВЛе§ШЗЕФЪЧ(ЬюаДБрКХ)___________________ЁЃ
AЃЎЪЙгУШнСПЦПЧАМьВщЫќЪЧЗёТЉЫЎ
BЃЎШнСПЦПгУеєСѓЫЎЯДОЛКѓЃЌдйгУД§ХфШмвКШѓЯД
CЃЎХфжЦШмвКЪБЃЌШчЙћЪдбљЪЧЙЬЬхЃЌАбГЦКУЕФЪдбљгУжНЬѕаЁаФЕЙШыШнСПЦПжаЃЌЛКТ§МгШыеєСѓЫЎЕННгНќБъЯп1 -2cmДІЃЌгУЕЮЙмЕЮМгеєСѓЫЎЕНБъЯп
DЃЎХфжЦШмвКЪБЃЌШчЙћЪдбљЪЧвКЬхЃЌгУСПЭВСПШЁЪдбљКѓжБНгЕЙШыШнСПЦПжаЃЌЛКТ§МгШыеєСѓЫЎЕННгНќШнСПЦППЬЖШБъЯп1-2 cmДІЃЌгУЕЮЙмЕЮМгеєСѓЫЎЕНПЬЖШЯп
EЃЎИЧКУЦПШћЃЌгУЪГжИЖЅзЁЦПШћЃЌгУСэвЛжЛЪжЕФЪжжИЭазЁЦПЕзЃЌАбШнСПЦПЕЙзЊКЭвЁЖЏЖрДЮ
(3)дѕбљМьВщШнСПЦПЪЧЗёТЉЫЎЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
21ЁЂ
 (8Зж)ЧыНЋ5жжЮяжЪЃКN2OЁЂFeSO4ЁЂFe(NO3)3ЁЂHNO3КЭFe2(SO4)3ЗжБ№ЬюШыЯТУцЖдгІЕФКсЯпЩЯЃЌзщГЩвЛИіЮДХфЦНЕФЛЏбЇЗНГЬЪНЁЃ
(8Зж)ЧыНЋ5жжЮяжЪЃКN2OЁЂFeSO4ЁЂFe(NO3)3ЁЂHNO3КЭFe2(SO4)3ЗжБ№ЬюШыЯТУцЖдгІЕФКсЯпЩЯЃЌзщГЩвЛИіЮДХфЦНЕФЛЏбЇЗНГЬЪНЁЃ
_________+__________Ёњ__________+__________+__________+H2O
(2)ЗДгІЮяжаЗЂЩњбѕЛЏЗДгІЕФЮяжЪ__________ЃЌБЛЛЙдЕФдЊЫиЪЧ_________ЁЃ
(3)ЗДгІжа1 molбѕЛЏМС_______(ЬюЁАЕУЕНЁБЛђЁАЪЇШЅЁБ)___________ molЕчзгЁЃ
(4)ЧыНЋЗДгІЮяЕФЛЏбЇЪНМАХфЦНКѓЕФЯЕЪ§ЬюШыЯТСаЯргІЕФЮЛжУжаЃК
ЁЁ ЁЁ ЁЁЁЁЁЁЁЁ __________+ЁЁЁЁЁЁЁЁ __________ЁњЁЁЁЁЁЁЁЁЁЁ
22(6Зж)ЪЕбщЪвгаМзЁЂввСНЦПЮоЩЋШмвКЃЌЦфжавЛЦПЪЧЯЁбЮЫсЃЌСэвЛЦПЪЧЬМЫсФЦШмвКЁЃЮЊВтЖЈМзЁЂввСНЦПШмвКЕФГЩЗжМАЦфЮяжЪЕФСПХЈЖШЃЌНјаавдЯТЪЕбщЃК
ЂйСПШЁ25.00 mLМзШмвКЃЌЯђЦфжаЛКТ§ЕЮШыввШмвК15.00 mLЃЌЙВЪеМЏЕН224 mL(БъзМзДПі)ЦјЬхЁЃЂкСПШЁ15.00 mLввШмвКЃЌЯђЦфжаЛКТ§ЕЮШыМзШмвК25.00 mLЃЌЙВЪеМЏЕН112 mL(БъзМзДПі)ЦјЬхЁЃ
ЁЁ (1)ХаЖЯЃКМзЪЧ____ЁЁ ____ШмвКЃЌЦфЮяжЪЕФСПХЈЖШЮЊЁЁЁЁЁЁ molЁЄL-1ЁЃ
ЁЁ (2)ЪЕбщЂкжаЫљЗЂЩњЗДгІЕФРызгЗНГЬЪНЮЊ_______________________ЁЁ _____ ЁЃ
20ЁЂ0.4mol KMnO4дквЛЖЈЮТЖШЯТМгШШвЛЖЮЪБМфЩњГЩa mol O2 , НЋЪЃгрЕФЙЬЬхгыЙ§СПХЈбЮЫсЛьКЯМгШШгжЩњГЩb mol Cl2, ДЫЪБУЬдЊЫиОљвдMn2+ аЮЪНДцдкЁЃШєa+b=m,дђmЕФжЕПЩФмЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
AЃЎ1.20ЁЁЁЁЁЁ ЁЁЁЁ BЃЎ1.1ЁЁЁЁЁЁЁЁ ЁЁ CЁЂ0.9ЃЎЁЁ ЁЁЁЁ DЃЎ0.7
ЕкЂђОэ(ЗЧбЁдёЬт ЙВ45Зж)
19ЁЂНЋФЦЁЂУОЁЂТСИї0.3molЗжБ№ЗХШы100mlЁЁ 1molЁЄL-ЕФбЮЫсжаЃЌЭЌЮТЭЌбЙЯТВњЩњЕФЦјЬхЬхЛ§БШЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁ(ЁЁЁЁЁЁ )
AЁЂ3:2:1ЁЁЁЁЁЁЁЁ BЁЂ1:2:3ЁЁЁЁЁЁЁЁЁЁ CЁЂ1:3:2ЁЁЁЁЁЁЁЁЁЁ DЁЂ3:1:1
18ЁЂНЋ3.1gУОТСКЯН№ЭЖШыЕН500mlЁЁ 2molЁЄL-ЕФСђЫсШмвКжаЃЌН№ЪєЭъШЋШмНтЃЌдйМгШы4 molЁЄL-ЕФNaOHШмвКЃЌШєвЊЩњГЩГСЕэзюЖрЃЌдђгІМгШыетжжNaOHШмвКЕФЬхЛ§ЪЧЁЁЁЁ (ЁЁЁЁЁЁ )
AЁЂ200mlЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЁЂ250mlЁЁЁЁЁЁЁЁЁЁЁЁ CЁЂ500mlЁЁЁЁЁЁЁЁЁЁЁЁ DЁЂ560ml
17ЁЂШєІи1Іи2ЗжБ№БэЪОХЈЖШЮЊamolЁЄL-КЭbmolЁЄL-СђЫсЕФжЪСПЗжЪ§ЃЌЧвжЊ2aЃНbЃЌдђЯТСаЭЦЖЯе§ШЗЕФЪЧ(СђЫсЕФУмЖШБШДПЫЎДѓ)ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁЁЁ )
AЁЂ2Іи1ЃНІи2ЁЁЁЁЁЁ BЁЂІи1ЃН2Іи2ЁЁЁЁЁЁЁЁЁЁЁЁ CЁЂІи2>2Іи1ЁЁЁЁЁЁЁЁ DЁЂІи1<Іи2<2Іи1
16ЁЂвбжЊI-ЁЂFe2+ЁЂSO2ЁЂCl-КЭH2O2НдОпгаЛЙдадЃЌЫќУЧдкЫсадШмвКжаЛЙдадЕФЧПШѕЫГађЮЊЃКCl-ЃМ H2O2ЃМFe2+ЃМI-ЃМSO2ЃЌдђЯТСаЗДгІВЛПЩФмЗЂЩњЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁЁЁ )
AЁЂ2Fe3++SO2+2H2OЃН2Fe2++SO42-+4H+
BЁЂI2 +SO2+2H2OЃНH2SO4+2HI
CЁЂH2O2+ SO2ЃНH2SO4
DЁЂ2Fe3++I2ЃН2Fe2++2I-
15ЁЂЖдгкФГаЉРызгЕФМьбщМАНсТле§ШЗЕФЪЧ(ЁЁЁЁ )
AЁЂМгШыЯЁбЮЫсВњЩњЮоЩЋЦјЬхЃЌНЋЦјЬхЭЈШыГЮЧхЪЏЛвЫЎжаЃЌШмвКБфЛызЧЃЌвЛЖЈКЌгаCO32-
BЁЂМгШыТШЛЏБЕШмвКВњЩњАзЩЋГСЕэЃЌдйМгЯЁбЮЫсЃЌГСЕэВЛЯћЪЇЃЌвЛЖЈКЌгаSO42-
CЁЂМгШыЧтбѕЛЏФЦШмвКВЂМгШШЃЌВњЩњЕФЦјЬхФмЪЙЪЊШѓКьЩЋЪЏШяЪджНБфРЖЃЌвЛЖЈКЌгаNH4+
DЁЂМгШыЬМЫсФЦШмвКВњЩњАзЩЋГСЕэЃЌдйМгбЮЫсАзЩЋГСЕэЯћЪЇЃЌвЛЖЈКЌгаBa2+
14ЁЂдкЗДгІ5NH4NO3ЁЁ =ЁЁ 2HNO3 + 4N2Ёќ+ 9H2OЕФЗДгІжаЃЌЗЂЩњбѕЛЏЗДгІКЭЗЂЩњЛЙдЗДгІЕФЕЊдЊЫиЕФжЪСПБШЪЧЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ(ЁЁ ЁЁЁЁ)
AЃЎ5ЃК4ЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎ4ЃК5ЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎ5ЃК3ЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎ3ЃК5ЁЁ
13ЁЂЯТСабѕЛЏЛЙдЗДгІжаЃЌЫЎжЛзїЮЊЛЙдМСЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЁЁ ЁЁЁЁ)
A.ЁЁ CO+H2O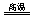 CO2+H2ЁЁЁЁЁЁЁЁ
ЁЁB.ЁЁ
3NO2+H2O = 2HNO3+NO
CO2+H2ЁЁЁЁЁЁЁЁ
ЁЁB.ЁЁ
3NO2+H2O = 2HNO3+NO
C.ЁЁ 2Na2O2+2H2O = 4NaOH+O2ЁќЁЁЁЁ D.ЁЁ 2F2+2H2O = 4HF+O2
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com