
²ÄĮĻ¶ž£ŗ2007Äź12ŌĀ£¬Ź®½ģČ«¹śČĖ“ó³£ĪÆ»įČżŹ®Ņ»“Ī»įŅéÉóŅ锶Ź³Ę·°²Č«·Ø(²Ż°ø)”·£¬ŹÜ¹śĪńŌŗĪÆĶŠ£¬ĪĄÉś²æŌŚ»įÉĻ¾ĶøĆ·Ø°øµÄŠŽ¶©²Ż°ø×÷ĮĖĖµĆ÷”£øł¾ŻĪÆŌ±³¤»įŅéµÄ¾ö¶Ø£¬ÉĻŹö·Ø°ø½«ĶعżĮ¢·ØĀŪÖ¤»įµČŠĪŹ½¹ć·ŗÕ÷ĒóŅā¼ū£¬ÉīČėŃŠ¾æĀŪÖ¤ŗó£¬ŌŁÓÉČĖ“ó³£ĪÆ»įÉóŅéĶعż”£
ĒėŌĖÓĆ”¶¹ś¼ŅŗĶ¹ś¼Ź×éÖƳ£Ź¶”·ÖŖŹ¶£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)”” øł¾Ż²ÄĮĻŅ»£¬¼ņŅŖ·ÖĪöĆĄ¹ś²śÉśÕāÖÖÕžÖĪĻÖĻóµÄŌŅņ”£(6·Ö)
(2)”” ¶Ō±ČĮ½Ōņ²ÄĮĻ£¬ĖµĆ÷ĪŅ¹ś¹ś¼ŅČØĮ¦ŌĖŠŠŌŌņ¼°ĘäÖŲŅŖŠŌ”£(7·Ö)
41”¢(37·Ö)
(1)ŌĖÓĆÕžÖĪÉś»īµÄÖŖŹ¶»Ų“š£ŗø÷¹śÓ¦ČēŗĪ¹²Ķ¬ĶĘ¶Æ½ØÉč³Ö¾ĆŗĶĘ½”¢¹²Ķ¬·±ČŁµÄŗĶŠ³ŹĄ½ē£æ(7·Ö)
²ÄĮĻ¶ž”” øÄøļæŖ·ÅŅŌĄ“£¬ČĖĆĒµÄĪļÖŹÉś»ī“ó“ó·įø»ĮĖ£¬µ«ČĖĆĒµÄŠŅø£øŠ²¢Ć»ÓŠĖęÖ®Ķ¬²½Ōö³¤”£½üÄźĄ“£¬”°ŠŅø£ÖøŹż”±³ÉĪŖČĖĆĒĢÖĀŪµÄŠĀĢā”£×ؼŅČĻĪŖ£¬”°ŠŅø£ÖøŹż”±µÄĢįÉż²»ÄÜȱɣ¾«ÉńµÄ×ĢŃųŗĶĪĻƵĽžČó£¬ŹęŠÄ”¢ŠŅø£µÄÉś»īĄė²»æŖ½”æµŗĶŠ³µÄ¾«Éń¼ŅŌ°”£
(2)½įŗĻ”¶ĪÄ»ÆÉś»ī”·ĖłŃ§ÖŖŹ¶£¬¾ĶČēŗĪ¹¹½Ø½”æµŗĶŠ³µÄ¾«Éń¼ŅŌ°ĢøĢøÄćµÄæ“·Ø”£(6·Ö)
20£®(6·Ö)Ļņ1LAlCl3 ŗĶFeCl3µÄ»ģŗĻČÜŅŗÖŠ¼ÓČėŗ¬a mol NaOHµÄČÜŅŗŹ±£¬²śÉśµÄ³ĮµķæÉ“ļµ½×ī“óÖµ£»¼ĢŠų¼ÓČėNaOHµÄČÜŅŗ£¬³ĮµķæŖŹ¼Čܽā£¬µ±Ē°ŗó¼ÓČėµÄNaOHµÄĪļÖŹµÄĮæ“ļµ½b molŹ±£¬³ĮµķĮæ²»ŌŁ±ä»Æ”£ĒóŌČÜŅŗÖŠFe3+µÄĪļÖŹµÄĮæÅØ¶Č”£
2009-2010ѧğ¶ČµŚŅ»Ń§ĘŚøßÖŠ½Ģѧ֏Įæ¼ą²ā(Ņ»)
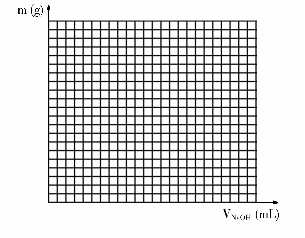
19£®(10·Ö)½«Ņ»¶ØĮæĆ¾ĀĮŗĻ½šĶźČ«ČÜÓŚ100mLijÅضČŃĪĖįÖŠ£¬²āµĆ»ģŗĻŅŗĄļc(Mg2+)= 2 mol”¤L-1”¢c(Al3+)=1mol”¤L-1”¢c(Cl-)= 8 mol”¤L-1£¬Ķł“Ė»ģŗĻŅŗ¼ÓČėÅضČĪŖ5 mol”¤L-1µÄNaOHČÜŅŗÖĮ¹żĮ棬¹ĄĖćŗóĒėŌŚÓŅĶ¼»³ö¼ÓČėNaOHČÜŅŗĢå»żÓė²śÉś³ĮµķÖŹĮæµÄ¹ŲĻµĶ¼Ź¾”£
18£®(16·Ö)Ņ½ÓĆĀČ»ÆøĘæÉÓĆÓŚÉś²ś²¹øĘ”¢æ¹¹żĆōŗĶĻūŃ×µČŅ©Īļ”£ŅŌ¹¤ŅµĢ¼ĖįøĘ(ŗ¬ÓŠÉŁĮæNa+”¢Al3+”¢Fe3+µČŌÓÖŹ)Éś²śŅ½Ņ©¼¶¶žĖ®ŗĻĀČ»ÆøĘ(CaCl2”¤2H2OµÄÖŹĮæ·ÖŹżĪŖ97.0%~99.9%)µÄÖ÷ŅŖĮ÷³ĢČēĻĀ£ŗ
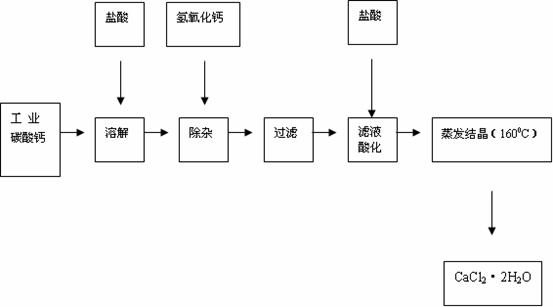
(1) ³żŌÓ²Ł×÷ŹĒ¼ÓČėĒāŃõ»ÆøĘ£¬µ÷½ŚČÜŅŗµÄpHĪŖ8.0 - ””8.5£¬ŅŌ³żČ„ČÜŅŗÖŠµÄÉŁĮæAl3+”¢
Fe3+”£¼ģŃéFe(OH)3ŹĒ·ń³ĮµķĶźČ«µÄŹµŃé²Ł×÷ŹĒ””””””””””””””””””””””””””””””””””
”””” ”””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””£
(2) Ėį»Æ²Ł×÷ŹĒ¼ÓČėŃĪĖį£¬µ÷½ŚČÜŅŗµÄpHŌ¼ĪŖ4.0£¬ĘäÄæµÄÓŠ£ŗ½«ČÜŅŗÖŠµÄÉŁĮæCa(OH)2×Ŗ»ÆĪŖCaCl2£»·ĄÖ¹ČÜŅŗĪüŹÕæÕĘųÖŠµÄCO2£»”””””””””””””””””””””””””””””” ”£
²ā¶Øѳʷ֊Cl-ŗ¬ĮæµÄ·½·ØŹĒ£ŗ
a”¢Č”0.75 gѳʷ£¬Čܽā£¬ŅĘŅŗ(ŗ¬Ļ“µÓŅŗ)£¬ŌŚ250 mLČŻĮæĘæÖŠ¶ØČŻ”¢Ņ”ŌČ£»
b”¢Č”25.00 mLÉĻŹö“ż²āČÜŅŗӌ׶ŠĪĘæÖŠ£»
c”¢ÓĆ0.05 mol”¤L-1 AgNO3ČÜŅŗµĪ¶ØÖĮÖÕµć£¬ĻūŗÄAgNO3ČÜŅŗĢå»żµÄĘ½¾łÖµĪŖ20.00 mL”£
¢Ł Čܽā£¬ŅĘŅŗ¶¼ÓƵ½µÄ²£Į§ŅĒĘ÷³żÉÕ±Ķā»¹ÓŠ”””””””””””””””””””””””””””””””””””” ”£
¢Ś ¶ØČŻµÄ²Ł×÷ŹĒ””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””
¢Ū ÉĻŹö²ā¶Ø¹ż³ĢÖŠŠčÓĆČÜŅŗČóĻ“µÄŅĒĘ÷ÓŠ”””””””””””””””””””””””””””””””””””””””” ”£
¢Ü ¼ĘĖćÉĻŹöѳʷ֊CaCl2”¤2H2OµÄÖŹĮæ·ÖŹżĪŖ”””””””””””””””””””””””””””””””””””” ”£
¢Ż ČōÓĆÉĻŹö·½·Ø²ā¶ØµÄѳʷ֊CaCl2”¤2H2OµÄÖŹĮæ·ÖŹżĘ«øß(²ā¶Ø¹ż³ĢÖŠ²śÉśµÄĪó²īæÉŗöĀŌ)£¬ĘäæÉÄÜŌŅņÓŠ”””””””””””””””””””””””” £»”””””””””””””””””””””””””””””””” ”£
17£®(14·Ö)ijŠ£»ÆѧŹµŃéŠĖȤŠ”×éĪŖĮĖĢ½¾æŌŚŹµŃéŹŅÖʱøCl2µÄ¹ż³ĢÖŠÓŠĖ®ÕōĘųŗĶHCl»Ó·¢³öĄ“£¬Ķ¬Ź±Ö¤Ć÷ĀČĘųµÄijŠ©ŠŌÖŹ£¬¼×Ķ¬Ń§Éč¼ĘĮĖČēĻĀĶ¼ĖłŹ¾µÄŹµŃé×°ÖĆ(Ö§³ÅÓƵÄĢś¼ÜĢØŹ”ĀŌ)£¬°“ŅŖĒó»Ų“šĪŹĢā”£
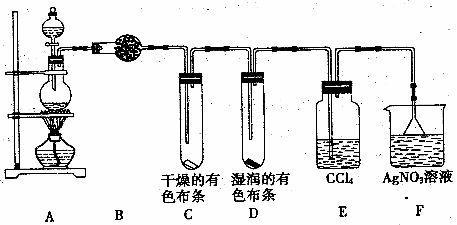
(1)ŹµŃéŹŅÖĘČ”ĀČĘųµÄ»Æѧ·½³ĢŹ½ŹĒ””””””””””””””””””””””””””””””””””””””””””””
(2) ¢Ł×°ÖĆB֊װČėµÄŹĒĪŽĖ®ĮņĖįĶ·ŪÄ©£¬Ęä×÷ÓĆŹĒ””””””””””””””””””””””””””””””””””
¢Ś×°ÖĆCŗĶD³öĻֵIJ»Ķ¬ĻÖĻóĖµĆ÷””””””””””””””””””””””””””””””””””””””””””
”””””” ¢Ū×°ÖĆFµÄ×÷ÓĆŹĒ””””””””””””””””””””””””””””””””””””””””””””””””””””””””
(3)ŅŅĶ¬Ń§ČĻĪŖ¼×Ķ¬Ń§µÄŹµŃéӊȱĻŻ£¬²»ÄÜČ·±£×īÖÕĶØČėAgNO3ČÜŅŗÖŠµÄĘųĢåÖ»ÓŠŅ»ÖÖ”£ĪŖĮĖČ·±£ŹµŃé½įĀŪµÄæÉææŠŌ£¬Ö¤Ć÷×īÖÕĶØČėAgNO3ČÜŅŗµÄĘųĢåÖ»ÓŠŅ»ÖÖ£¬ŅŅĶ¬Ń§Ģį³öŌŚÄ³Į½øö×°ÖĆÖ®¼äŌŁ¼ÓŅ»øö×°ÖĆ”£ÄćČĻĪŖøĆ×°ÖĆÓ¦¼ÓŌŚ”””””” Óė”””””””” Ö®¼ä(Ģī×°ÖĆ×ÖÄøŠņŗÅ)£¬øĆ×°ÖĆÖŠÓ¦·ÅČė”””””””””””””””” (ĢīŹŌ¼Į»ņĘäĖüĪļÖŹ)”£
16£®(9·Ö)·ÖĄąŹĒ»Æѧъ¾æÖŠ³£ÓƵķ½·Ø”£
(1)ĻĀĮŠ·ÖĄą·½·ØÖŠ£¬ÕżČ·µÄŹĒ”””””””””””””””””””” ””
A£®ŅĄ¾ŻĖį·Ö×Ó×é³ÉÖŠŗ¬ÓŠĒāŌ×ӵďżÄ棬½«Ėį·ÖĪŖŅ»ŌŖĖį”¢¶žŌŖĖįµČ
B£®ŅĄ¾ŻÓŠ·ńµē×Ó×ŖŅĘ£¬½«»Æѧ·“Ó¦·ÖĪŖŃõ»Æ»¹Ō·“Ó¦ŗĶ·ĒŃõ»Æ»¹Ō·“Ó¦
C£®ŅĄ¾ŻÄÜĮæµÄ±ä»Æ£¬½«»Æѧ·“Ó¦·ÖĪŖ·ÅČČ·“Ó¦ŗĶĪüČČ·“Ó¦
D£®ŅĄ¾Ż×é³ÉŌŖĖŲµÄÖÖĄą£¬½«“æ¾»Īļ·ÖĪŖµ„ÖŹŗĶ»ÆŗĻĪļ
(2)Na2CO3”¢FeSO4”¢Cu(NO3)2”¢ZnCl2ĖÄÖÖĪļÖŹÖŠÓŠŅ»ÖÖĪļÖŹµÄĄą±šÓėĘäĖüČżÖÖ²»Ķ¬£¬ÄćŃ”ŌńµÄŹĒ”””””””””””” £¬ÄćµÄøł¾ŻŹĒ”””””””””””””””””””””””””””””””””””””””” ”£
15£®ĻĀĮŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹéŠ“ÕżČ·µÄŹĒ”””””””””” (”””” )
A£®“ĪĀČĖįøĘČÜŅŗÖŠĶØČėÉŁĮæSO2ĘųĢå£ŗCa2++2ClO-+SO2+H2O=CaSO3”ż+2HClO
B£®³ĪĒåŹÆ»ŅĖ®ÓėÉŁĮæĖÕ“ņČÜŅŗ»ģŗĻ:Ca2++OH-+HCO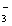 =CaCO3”ż+H2O
=CaCO3”ż+H2O
C£®½«1mol Cl2ĶØČėŗ¬ÓŠ1mol FeI2 µÄČÜŅŗÖŠ:2I-+Cl2=2Cl-+I2
D£®ĀČ»ÆĀĮČÜŅŗ¼ÓČė¹żĮæ°±Ė®:Al3++4NH3”¤H2O=AlO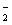 +4NH
+4NH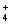 +2H2O
+2H2O
µŚ ¢ņ ¾ķ(¹²55·Ö)
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com