
13.下列实验结论,其中错误的是
A.往新配制的可溶性淀粉溶液中滴加碘水,溶液显蓝色,用CCl4不能从中萃取出碘。
B.当锌完全溶解后,铁与酸反应产生氢气的速率会显著减慢,此现象可作为判断镀锌铁皮中锌镀层是否完全被反应掉的依据。
C.制备硫酸亚铁铵晶体时,最后在蒸发皿中蒸发浓缩溶液时,只需小火加热至溶液表面出现晶膜为止,不能将溶液全部蒸干。
D.提取海带中碘元素时,为保证I-完全氧化为I2,加入的氧化剂(H2O2或新制氯水)均应过量。
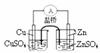
12.下列实验对应的结论正确的是
|
实验 |
 |
 |
 |
 |
|
结论 |
能组成 Zn、Cu原电池 |
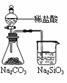
能证明非金属性 Cl>C>Si |
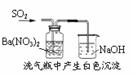
白色沉淀 为BaSO3 |
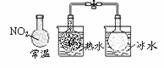
说明反应 2NO2  N2O4 △H>0 N2O4 △H>0(无色) |
|
选项 |
A |
B |
C |
D |
11.类推是在化学学习和研究中常用的思维方法,但类推出的结论最终要经过实践的检验才能决定其正确与否,下列几种类推结论中不正确的是
A.钠、镁都是活泼金属,金属钠和镁引起火灾都不能用干冰灭火器灭火
B.第二周期元素氢化物的稳定性顺序是:HF>H2O>NH3 ,则第三周期元素氢化物的稳定顺序也是:HCl>H2S>PH3
C.NH4Cl、NH4I结构相似,将两种固体分别加热,都分解生成HX和NH3
D.原电池中通常是活泼金属做负极,不活泼金属做正极,用铜和铝与浓硝酸构成原电池时,铝却是正极
10.向四只盛有一定量NaOH溶液的烧杯中通入不同量的CO2气体后,在所得溶液中逐滴加入盐酸至过量,并将溶液加热,产生的气体与加入盐酸的物质的量的关系如图:
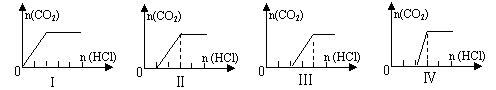
则下列分析都正确的组合是:
|
|
溶液组成主要成分 |
对应图象 |
溶液中离子浓度关系 |
|
A |
NaHCO3、Na2CO3 |
Ⅱ |
c(CO32-) <
c(HCO3-) |
|
B |
NaOH 、 Na2CO3 |
Ⅲ |
c(OH-)>c(CO32-) |
|
C |
Na2CO3 |
Ⅳ |
c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
|
D |
NaHCO3 |
I |
c(Na+) =
c(HCO3-) |
9.某温度下,在一密闭容器中发生如下可逆反应:2E(g)
 F(g)+xG(g);△H<0。若起始时E浓度为a
mol·L-1,F、G浓度均为0,达平衡时E浓度为O.5a mol·L-1;若E的起始浓度改为
2a mol·L-1,F、G浓度仍为O,当达到新的平衡时,下列说法正确的是
F(g)+xG(g);△H<0。若起始时E浓度为a
mol·L-1,F、G浓度均为0,达平衡时E浓度为O.5a mol·L-1;若E的起始浓度改为
2a mol·L-1,F、G浓度仍为O,当达到新的平衡时,下列说法正确的是
A.升高温度时,正反应速率加快、逆反应速率减慢
B.若x=l,容器体积保持不变,新平衡下E的体积分数为50%
C.若x=2,容器体积保持不变,新平衡下F的平衡浓度小于0.5a mol·L-1
D.若x=2,容器压强保持不变,新平衡下E的物质的量为a mol
8.在常温下10mL pH=10的KOH溶液中,加入pH=4的一元酸HA溶液至pH刚好等于7(假设反应前后体积不变),则对反应后溶液的叙述①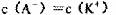
②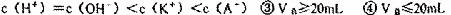 其中正确的是
其中正确的是
A.①④ B.①③ C.②④D.②③
 不定项选择题:每题有1-2个正确选项
不定项选择题:每题有1-2个正确选项
7. “假说”在化学科学的研究和发展中起到不可替代的作用。下列“假说”在化学科学发展过程中曾经起到一定的作用,从目前的化学理论看,仍然科学的是
A.道尔顿提出的“每一元素的原子以其原子质量为其特征”
B.阿伦尼乌斯提出的“电解质在溶液中会自发离解成带电的粒子”
C.贝采里乌斯提出的“不同原子带不同的电性,因而产生吸引力,由此形成化合物”
D.盖·吕萨克提出的“在同温同压下,相同体积的不同气体含有相同数目的原子”
6.不久前,日本某一材料研究所的科学家发明了一种“碳纳米管温度计”,这种温度计被认定为世界上最小的温度计。研究人员在长约10-6m,直径为10-7m的碳纳米管中充入液态的金属镓。当温度升高时,管中镓就会膨胀,通过电子显微镜就能读取温度值。这种温度计测量的范围可从18℃到490℃,精确度较高,所以它可用于检查电子线路是否异常,测量定毛细血管的温度等许多方面。根据以上信息判断下列推测中不正确的是
A.碳纳米管的体积在10℃至500℃之间随温度变化很小,可忽略不计
B.金属镓的体积在10℃至500℃之间随温度变化很小,可忽略不计
C.金属镓的体积在30℃至500℃之间随温度变化比较均匀
D.金属镓的熔点很低,沸点很高
5. 已知在酸性条件下能发生下列反应:Cu+→Cu+Cu2+(未配平)。NH4CuSO3与足量的 10 mol/L硫酸溶液混合微热,产生下列现象:①有红色金属生成;②有刺激性气味气体产生;③溶液呈蓝色。据此判断下列说法一定合理的是
A. 该反应显示硫酸具有酸性 B. NH4CuSO3中硫元素被氧化
C. 刺激性气味的气体是氨气 D. 反应中硫酸作氧化剂
4.X、Y、Z、M是4种短周期元素,其中X、Y位于同一主族,Y与M、X与Z位于同一周期。X原子最外层电子数是其电子层数的3倍。Z原子的核外电子数比X原子少1。M是同周期中半径最大的元素(除稀有气体元素外)。下列说法正确的是
A.工业上,Y元素氧化物对应水化物的浓溶液常用铝制或铁制容器盛装
B.Z和X组成的化合物可作为缺氧场所的供氧剂
C.X、Y、Z元素的气态氢化物中,Y的沸点最高
D.四种元素简单离子的半径由大到小依次为Y>Z>X>M
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com