
22(共6分,每空2分).从H+、Cu2+、Na+、SO42-、Cl-等五种离子中选择适当的离子组成电解质,使之符合下列要求。
(1)以碳棒为电极,电解时电解质质量减小,水量不变,应选用的电解质是________________________________;
(2)以碳棒为电极,电解时电解质质量不变,水量减少,应选用的电解质是________________________________;
(3)以碳棒为阳极,铁棒为阴极,电解时电解质质量和水量都减少,则应选用的电解质是_________________________________。
23.(共5分,每空1分)测得某溶液的pH = 6.5,且氢离子与氢氧根离子物质的量相等,此溶液呈_____性。测定温度______室温(填高于、低于或等于),其理由是 。 将此温度下pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合。
(1)若所得混合液为中性,则a︰b 。
(2)若所得混合液的pH=2,则a︰b 。
21.某二元酸(H2A)按下式发生电离:H2A = H++HA-;HA- H++A2-。关于下列四种溶液的说法正确的是
( )
①0.01mol/L的H2A溶液
②0.01mol/L的NaHA溶液
③0.02mol/L的HCl溶液与0.04mol/L的NaHA溶液等体积混合
④0. 02mol/L的NaOH溶液与0.02mol/L的NaHA溶液等体积混合
A.溶液①中粒子浓度大小顺序是:c(H2A)>c(H+)>c(HA-)>c(A2-)>c(OH-)
B.溶液②中有关离子浓度关系:c(HA-)+2c(A2-)+c(H2A)=c(Na+)
H++A2-。关于下列四种溶液的说法正确的是
( )
①0.01mol/L的H2A溶液
②0.01mol/L的NaHA溶液
③0.02mol/L的HCl溶液与0.04mol/L的NaHA溶液等体积混合
④0. 02mol/L的NaOH溶液与0.02mol/L的NaHA溶液等体积混合
A.溶液①中粒子浓度大小顺序是:c(H2A)>c(H+)>c(HA-)>c(A2-)>c(OH-)
B.溶液②中有关离子浓度关系:c(HA-)+2c(A2-)+c(H2A)=c(Na+)
C.四种溶液中c(HA-)浓度大小:③>①>②>④ D.溶液③中有关离子浓度关系:c(HA-)+c(A2-)+c(OH-)=c(Na+)+c(H+)
20.某一元酸在1mol/L的溶液中电离度为0.001%,则该溶液的导电能力接近于( )
A.1mol/L 的NaOH溶液 B.纯水 C.10-6mol/L的NaOH D.10-5mol/L的NaCl
19.用石墨电极在一定温度下电解K2SO4饱和溶液m g。当阴极产生a mol气体时,从溶液中析出n g无水晶体。则剩余溶液的溶质质量分数是 ( )
A. B.
B. C.
C. D.
D.
18.25℃时,pH=a的氨水与pH =b的盐酸等体积混合,恰好完全反应,则该氨水的电离度可表示为 ( )
A.10(a+b-12)% B.10(a+b-14)% C.10(12-a-b)% D.10(14-a-b)%
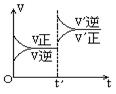
17.对达到平衡状态的可逆反应:X+Y 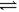 W+Z,在t℃时增大压强,则正逆反应速率变化如图所示(V代表速率,t代表时间)下列有关X、Y、Z、W的状态叙述正确的是: ( )
W+Z,在t℃时增大压强,则正逆反应速率变化如图所示(V代表速率,t代表时间)下列有关X、Y、Z、W的状态叙述正确的是: ( )
 A.X、Y、W为气体,Z不是气体
A.X、Y、W为气体,Z不是气体
B.X、Y为气体,W、Z中有一种是气体
C.W、Z为气体,X、Y中有一种是气体
|
16.若pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈酸性,其原因可能是( ) A.生成了一种强酸弱碱盐 B.弱酸溶液和强碱溶液反应 C.强酸溶液和弱碱溶液反应 D.一元强酸溶液和一元强碱溶液反应
15、某反应过程中体系的能量变化如图所示,下列说法错误的是 ( )
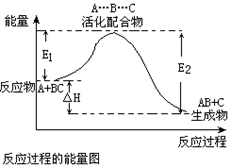 A.反应过程可表示为:A+BC-→[A…B…C] -→AB+C
A.反应过程可表示为:A+BC-→[A…B…C] -→AB+C
(反应物)(过渡态) (产物)
B.E1为反应物的平均能量与过渡态的能量差,称为正反应的活化能
C.正反应的热效应为△H=E1-E2,且E2>E1,所以正反应为放热反应
D.此图中逆反应的热效应△H=E1-E2,为吸热反应
14.下列离子方程式正确的是 ( )
A.H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O
B. FeBr2溶液中通入足量的Cl2:2Fe2++Cl2=2Fe3++2Cl-
C. AlCl3溶液中加入过量的浓氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O
D.等体积、等浓度的Ba(OH)2稀溶液与NH4HCO3稀溶液混合:
Ba2++2OH-+NH4++HCO3-=BaCO3↓+NH3·H2O+H2O
13. 已知当NH4Cl溶液的浓度小于0.1mol/L时,其pH>5.1。现用0.1mol/L的盐酸滴定10mL0.05mol/L的氨水,用甲基橙作指示剂达到终点时所用盐酸的量应是 ( )
A.10mL B.5mL C.大于5mL D.小于5mL
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com