
17ΓΔ(10Ζ÷) (1)ΓΓΓΓ 1.5/(t2-t1)mol/L.sΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
(2) ΓΓΓΓΓΓ2A+B⇌CΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΓΓΓΓΓΓ
(3)ΓΓΓΓ 0.25/(mol.L-)2ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
(4)ΓΓΓΓΓΓ ≤Μ±δΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
(5)ΓΓΓΓΓΓ Ζ≈»»ΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
16ΓΔ(10Ζ÷)≥ΐΒτœ¬Ν–Έο÷ ÷–ΒΡ‘”÷ Θ§ά®Κ≈ΡΎΈΣ‘”÷
|
ΓΓ |
Φ”»κ ‘ΦΝΜρΖΫΖ® |
άκΉ”ΖΫ≥Χ Ϋ |
|
CO2(HCl) |
±ΞΚΆΒΡΧΦΥα«βΡΤ»ή“Κ |
H++HCO3-=H2O+CO2Γϋ |
|
ΧΦΖέ(MnO2) |
≈®―ΈΥα |
MnO2+4H++2Cl-=Mn2++Cl2+2H2O |
|
Fe2O3(Al2O3) |
«β―θΜ·ΡΤ»ή“Κ |
Al2O3+2OH-=2AlO2-+H2O |
|
Na2CO3»ή“Κ(NaHCO3) |
«β―θΜ·ΡΤ»ή“Κ |
HCO3-+OH-=CO32-+H2O |
|
FeCl3(FeCl2) |
¬»Υ° |
2Fe2++Cl2=2Fe3++2Cl- |
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
C |
C |
A |
B |
B |
D |
B |
C |
C |
B |
|
11 |
12 |
13 |
14 |
15 |
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
|
BC |
C |
C |
C |
AC |
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
ΓΓ |
20ΓΔ(10Ζ÷)‘Ύ“ΜΙΧΕ®»ίΜΐΒΡΟή±’»ίΤς÷–Θ§±Θ≥÷“ΜΕ®ΧθΦΰœ¬Ϋχ––“‘œ¬Ζ¥”ΠΘΚX(g)+2Y(g)⇌3Z(g),“―÷ΣΦ”»κ1molXΚΆ3molY,¥οΒΫΤΫΚβΚσ…ζ≥…a mol Z .
(1)¥οΒΫΤΫΚβ ±Θ§Z‘ΎΖ¥”ΠΜλΚœΤχΧε÷–ΧεΜΐΖ÷ ΐ «ΓΓΓΓΓΓΓΓΓΓΓΓ
(2)‘ΎœύΆ§ Β―ιΧθΦΰœ¬Θ§»τ‘ΎΆ§“Μ»ίΤς÷–ΗΡΈΣΦ”»κ2mol XΚΆ6mol Y,¥οΒΫΤΫΚβΚσΘ§ZΒΡΈο÷ ΒΡΝΩΈΣΓΓΓΓΓΓ mol
(3)‘ΎœύΆ§ Β―ιΧθΦΰœ¬Θ§»τ‘ΎΆ§“Μ»ίΤς÷–ΗΡΈΣΦ”»κ2mol XΚΆ8mol Y,»τ“Σ«σZ‘ΎΖ¥”ΠΜλΚœΈο÷–ΧεΜΐΖ÷ ΐ≤Μ±δΘ§‘ρΜΙ–η“ΣΦ”»κZ ΓΓΓΓΓΓΓΓΓΓmol
(4)‘ΎœύΆ§ Β―ιΧθΦΰœ¬Θ§»τ‘ΎΆ§“Μ»ίΤς÷–Φ”»κ0.5mol X Θ§‘ρ–η“ΣΦ”»κ ΓΓΓΓΓΓmol Y, ΓΓΓΓΓΓΓΓΓΓmol Z,≤≈Ρή ΙΤΫΚβ ±ZΈΣ0.9a molΓΘ
 ¥πΑΗ
¥πΑΗ
19Θ°(11Ζ÷)“―÷ΣAΓΔBΓΔCΓΔDΓΔEΈε÷÷‘ΣΥΊΒΡ‘≠Ή”–ρ ΐ“ά¥Έ‘ω¥σΘ§AΓΔBΓΔCΨυΈΣΕΧ÷ήΤΎ‘ΣΥΊΘ§Τδ÷–A‘ΣΥΊ‘≠Ή”ΒΡΉνΆβ≤ψΒγΉ” ΐ «¥ΈΆβ≤ψΒΡ3±ΕΘ§AΓΔBΓΔC»ΐ÷÷‘ΣΥΊΒΡΦρΒΞάκΉ”ΕΦΨΏ”–œύΆ§ΒΡΒγΉ”≤ψΫαΙΙΘ§B”κC‘ΎΆ§“Μ÷ήΤΎΘ§«“Εΰ’ΏΒΡ‘≠Ή”ΉνΆβ≤ψΒγΉ” ΐ÷°ΚΆΒ»”Ύ4ΘΜDΈΣ≥ΘΦϊΒΡΫπ τ‘ΣΥΊΘ§”–»ΐ÷÷―θΜ·ΈοΘ§Τδ÷–ΝΫ÷÷‘Ύ≥ΘΈ¬œ¬ΈΣΚΎ…ΪΙΧΧεΘ§E‘ΣΥΊΒΡΒΞ÷ “Ή»ή”Ύ”–Μζ»ήΦΝ±ΫΘ§Τδ»ή“Κ≥ Ήœ…ΪΓΘ ‘ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
(1)ΓΓΓΓΓΓ C‘ΣΥΊΒΡάκΉ”ΫαΙΙ Ψ“βΆΦ_____________________ΓΘ
(2)ΓΓΓΓΓΓ A”κBΩ…–Έ≥…Μ·ΚœΈοB2AΘ§ ‘”ΟΒγΉ” Ϋ±μ ΨΤδ–Έ≥…Ιΐ≥Χ________________________ΓΘ
(3)ΓΓΓΓΓΓ E‘ΣΥΊ‘Ύ÷ήΤΎ±μ÷–ΒΡΈΜ÷ΟΘΚΒΎ______÷ήΤΎΒΎ_______ΉεΓΘ
(4)ΓΓΓΓΓΓ œ¬ΆΦ «”κ…œ ω‘ΣΥΊœύΙΊΒΡ≥ΘΦϊΈο÷ œύΜΞΖ¥”ΠΒΟΒΫΒΡ÷ς“Σ≤ζΈοΒΡΩρΆΦΘΚ(Ζ¥”ΠΧθΦΰ¥”¬‘)
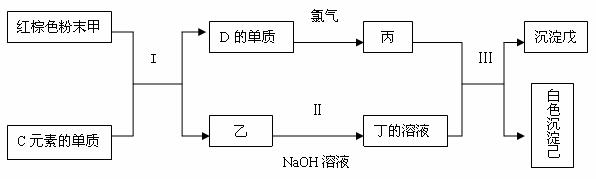
ΨίΆΦΜΊ¥πΘΚ
ΔΌΓΓΓΓ ≥ΝΒμΈλΒΡΜ·―ß Ϋ_____________ΓΘ
ΔΎΓΓΓΓ Ζ¥”ΠIΒΡΜ·―ßΖΫ≥Χ Ϋ___________________________________________ΓΘ
ΔέΓΓΓΓ Ζ¥”ΠIIΒΡάκΉ”ΖΫ≥Χ Ϋ___________________________________________ΓΘ
ΔήΓΓΓΓ ±ϊ”κΟςΖ·“Μ―υΘ§“≤Ω…ΉςΨΜΥ°ΦΝΘ§ΫαΚœάκΉ”ΖΫ≥Χ ΫΥΒΟς±ϊΒΡΨΜΥ°‘≠άμ_____________ΓΘ
18Θ°(10Ζ÷)÷–ΙζΓΑφœΕπ“ΜΚ≈Γ± ≥…ΙΠΒ«‘¬Θ§Υϋ Ι”ΟΒΡΆΤΫχΦΝ «“ΚΧ§«βΤχΚΆ“ΚΧ§―θΤχΓΘ“―÷Σ
H2(g)= H2(l)ΘΜΓςH=Θ≠0.92kJ/molΓΓΓΓΓΓ
O2(g)= O2(l)ΘΜΓςH=Θ≠6.84kJ/mol
H2O(l)= H2O(g)ΘΜΓςH=+44.00kJ/molΓΓΓΓ
H2(g)+ 1/2 O2(g)ΓΓ H2O(l)ΘΜΓςH=Θ≠285.80kJ/mol
(1)«κ–¥≥ω“ΚΧ§«βΤχΚΆ“ΚΧ§―θΤχ…ζ≥…ΤχΧ§Υ°ΒΡ»»Μ·―ßΖΫ≥Χ ΫΘΚ____________________ΓΘ
(2)«βΤχΓΔ―θΤχ≤ΜΫω»Φ…’ ±Ρή ΆΖ≈»»ΡήΘ§ΜΙΡή–Έ≥…‘≠Βγ≥ΊΫΪΤδΉΣΜ·ΈΣΒγΡήΘ§ΟάΙζΒΡΧΫ‘¬Ζ…¥§ΓΑΑΔ≤®¬όΚ≈Γ± Ι”ΟΒΡΨΆ ««β―θ»ΦΝœΒγ≥ΊΘ§ΒγΫβ÷ »ή“ΚΈΣH2SO4»ή“ΚΘ§Τδ’ΐΦΪΒΡΖ¥”Π ΫΈΣΘΚ_____________Θ§ΙΛΉς“ΜΕΈ ±ΦδΚσΘ§ΒγΫβ÷ »ή“ΚΒΡPHΫΪ_____(Χν‘ω¥σΓΔΦθ–ΓΓΔ≤Μ±δ)ΓΘ
(3)»τ”Ο«β―θ»ΦΝœΒγ≥ΊΆξ≥…‘ΎΧζ÷ΤΤΖ…œΕΤ–ΩΒΡ Β―ιΘ§Χζ÷ΤΤΖ”Π”κ«β―θ»ΦΝœΒγ≥ΊΒΡ_____(ΧνH2ΜρO2)ΒγΦΪœύΝ§Θ§―τΦΪΒΡΖ¥”Π ΫΈΣ_________Θ§ Β―ι÷–ΖΔœ÷“θΦΪ”–…ΌΝΩΤχΧε≤ζ…ζΘ§Ρψ»œΈΣΗΟΤχΧεΩ…Ρή «______(ΧνΜ·―ß Ϋ)ΓΘ
(4)»τΗΟ«β―θ»ΦΝœΒγ≥ΊΡήΝΩΉΣΜ·ΦΑΤδ‘ΎΗΟΕΤ–ΩΉΑ÷Ο÷–ΡήΝΩΒΡΉήάϊ”Ο¬ ΈΣ50%Θ§ΒγΕΤ“ΜΕΈ ±ΦδΚσΘ§Χζ÷ΤΤΖΒΡ÷ ΝΩ‘ωΦ”ΝΥ1.3gΘ§ΗΟ«β―θ»ΦΝœΒγ≥Ίάμ¬έ…œ÷Ν…Ό–ηœϊΚΡ‘Ύ±ξΉΦΉ¥Ωωœ¬ΒΡ«βΤχ_________ΚΝ…ΐΓΘ
 ΓΓ
ΓΓ
17Θ°(10Ζ÷)‘Ύ“ΜΟή±’»ίΤς÷–Φ”»κAΓΔBΓΔC»ΐ÷÷ΤχΧεΘ§‘ΎΈ¬Ε»T ΓφΚΆ(T+10)ΓφΒΡ≤ΜΆ§ ±ΩΧΘ§≤βΒΟΗςΈο÷ ΒΡ≈®Ε»»γœ¬±μΓΘ ΓΓΓΓΓΓΓΓ
|
Έ¬Ε» |
T Γφ |
(T+10)Γφ |
|||
|
≤βΕ® ±ΩΧ/s |
t1 |
t2 |
t3 |
t4 |
t5 |
|
c(A)/(molΓΛL-1) |
6 |
3 |
2 |
2 |
2.2 |
|
c(B)/(molΓΛL-1) |
5 |
3.5 |
3 |
3 |
3.1 |
|
c(C)/(molΓΛL-1) |
1 |
2.5 |
3 |
3 |
2.9 |
«κΜΊ¥πœ¬Ν–Έ ΧβΘΚ
 (1)TΓφ ±Θ§¥”t1ΒΫt2ΡΎΘ§“‘c(B)ά¥±μ ΨΒΡΤΫΨυΖ¥”ΠΥΌ¬ ΈΣ________ΓΘ
(1)TΓφ ±Θ§¥”t1ΒΫt2ΡΎΘ§“‘c(B)ά¥±μ ΨΒΡΤΫΨυΖ¥”ΠΥΌ¬ ΈΣ________ΓΘ
(2)ΗΟΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣΘΚ______________________________ (œΒ ΐ“‘ΉνΦρ’ϊ ΐ±»±μ Ψ)ΓΘ
(3)TΓφ ±Θ§ΗΟΖ¥”ΠΒΡΤΫΚβ≥Θ ΐK=__________________ΓΘ
(4)TΓφ ±Θ§ΗΟΖ¥”Π¥οΒΫΤΫΚβΚσΘ§‘ω¥σ―Ι«ΩΘ§ΤΫΚβ≥Θ ΐKΫΪ________(Χν‘ω¥σΓΔΦθ–ΓΓΔ≤Μ±δ)ΓΘ
(5)ΗΟΖ¥”ΠΒΡ’ΐΖ¥”ΠΈΣ____(ΧνΖ≈»»ΓΔΈϋ»»)Ζ¥”ΠΓΘ
16ΓΔ(10Ζ÷)≥ΐΒτœ¬Ν–Έο÷ ÷–ΒΡ‘”÷ Θ§ά®Κ≈ΡΎΈΣ‘”÷
|
ΓΓ |
Φ”»κ ‘ΦΝΜρΖΫΖ® |
άκΉ”ΖΫ≥Χ Ϋ |
|
CO2(HCl) |
ΓΓ |
ΓΓ |
|
ΧΦΖέ(MnO2) |
ΓΓ |
ΓΓ |
 Fe2O3(Al2O3) Fe2O3(Al2O3) |
ΓΓ |
ΓΓ |
|
Na2CO3»ή“Κ(NaHCO3) |
ΓΓ |
ΓΓ |
|
FeCl3(FeCl2) |
ΓΓ |
ΓΓ |
15ΓΔ≥ΘΈ¬œ¬Θ§0.1mol/L Na2CO3»ή“Κ÷–ΗςΈΔΝΘ≈®Ε»ΙΊœΒ’ΐ»ΖΒΡ «
AΘ°c(Na+)ΘΨc(CO32Θ≠)ΘΨc(HCO3Θ≠)ΘΨc(H2CO3)
BΘ°c(Na+)ΘΨc(CO32Θ≠)ΘΨc(H+)ΘΨc(OH-)
CΘ°c(Na+)+c(H+)ΘΫ2c(CO32Θ≠)+c(HCO3Θ≠)+c(OHΘ≠)
DΘ° c(Na+)ΘΫc(CO32Θ≠)+c(HCO3Θ≠)+c(H2CO3)
ΒΎΕΰΨμ(Ι≤50Ζ÷)
14ΓΔΡήΙΜ ΙΖ¥”ΠCu+2H2O=Cu(OH)2+H2ΓϋΖΔ…ζΒΡ «
AΘ°Ά≠Τ§Ής‘≠Βγ≥ΊΒΡΗΚΦΪΘ§ΧΦΑτΉς‘≠Βγ≥ΊΒΡ’ΐΦΪΘ§¬»Μ·ΡΤΉςΒγΫβ÷ »ή“Κ
BΘ°Ά≠–ΩΚœΫπ‘Ύ≥± ΣΩ’Τχ÷–ΖΔ…ζΒγΜ·―ßΗ· ¥
CΘ°”ΟΆ≠Τ§Ής“θΓΔ―τΒγΦΪΘ§ΒγΫβΝρΥαΡΤ»ή“ΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
DΘ°”ΟΆ≠Τ§Ής“θΓΔ―τΒγΦΪΘ§ΒγΫβΝρΥαΆ≠»ή“Κ
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com