
1.概念:分子间作用力又称 ,是广泛存在于分子与分子之间的较弱的电性引力,只有分子间充分接近时才有分子间的相互作用存在。
3.了解氢键及氢键对物质性质的影响
知识梳理
2.掌握影响分子间作用力的因素,了解分子间作用力对物质性质的影响
、 相同的分子具有相似的化学键特征,它们的许多性质是相近的,这叫做等电子原理。
试题枚举
[例1]关于化学键的下列叙述中,正确的是
A.离子化合物中可能含有共价键
B.共价化合物中可能含有离子键
C.离子化合物中只含离子键
D.共价键只能存在于化合物中
解析:离子键只存在于离子化合物中,共价键可存在于离子化合物、共价化合物以及某些单质中
答案: A
[例2]下列化合物中既存在离子键,又存在极性键的是
A.H2O B.NH4Cl C.NaOH D.Na2O2
解析:水分子中只有H-O键,是极性键,无离子键,排除A项;NH4Cl中NH4+和Cl-间是离子键,NH4+内N和H原子以极性键结合,B项正确;NaOH中Na+和OH-以离子键结合,OH-内H和O之间以极性键结合,C项正确;Na2O2中Na+和O22-以离子键结合,O22-内有非极性键,排除D项。
答案:B C。
[例3]下列分子中所有原子都满足最外层8电子结构的是
A.光气(COCl2) B.六氟化硫 C.二氟化氙 D.三氟化硼
解析:分子中的原子是否满足8电子结构,决定于中心原子的最外层电子数和形成共价键的数目
答案:A
[例4]对δ键的认识不正确的是( )
A.δ键不属于共价键,是另一种化学键
B.S-Sδ键与S-Pδ键的对称性相同
C.分子中含有共价键,则至少含有一个δ键
D.含有π键的化合物与只含δ键的化合物的化学性质不同
解析:共价键包括δ键和π键,δ键不管是S-Sδ键、S-Pδ键还是P-Pδ键都是轴对称的,π键不够稳定,必须与δ键共存
答案:A
[例5]下列分子中,键能最小的是
A.F2 B.Br2 C.Cl2 D.N2
解析:N2中含有一个三键,键能较大;F2、Br2、Cl2中只有一个单键,键能小,F2分子中电子“密度”大,F原子间斥力大,键能最小
答案:A
[例6]能够用键能解释的是( )
A.氮气的化学性质比氧气稳定
B.常温常压下,溴呈液体,碘为固体
C.稀有气体一般很难发生化学反应
D.硝酸易挥发,硫酸难挥发
解析:键能的大小影响键的稳定性,影响的是物质的化学性质(稳定性)
[例7]与NO3-互为等电子体的是( )
A.SO3 B.BF3 C.CH4 D.NO2
解析:等电子体要求原子总数相同、价原子总数相同,C、D原子总数不同,A价原子总数不同,选B
答案:B
分子间作用力与氢键
考点聚焦
1.掌握分子间作用力的本质及分子间作用力与化学键的区别
键参数包括 、 、 ;其中 、 是衡量共价稳定性的参数,通常键长越 ,键能越大,表明共价键越稳定;共价键具有 性, 是描述分子立体结构的重要参数,分子的立体结构还与 有一定的关系。
|
 非极性共价键: 元素的原子间形成的共价键,共用电子对
偏向任何一个原子,各原子都
,简称
非极性共价键: 元素的原子间形成的共价键,共用电子对
偏向任何一个原子,各原子都
,简称
极性共价键: 元素的原子间形成的共价键,共用电子对偏向电负性 较 的一方,简称
|
 δ键:δ键的特征:以形成化学键的两原子核的连线为轴作旋转操作,共价键电子云的图形不变,这种特征称为
。常见的δ键有“s-sδ键”、
、
。
δ键:δ键的特征:以形成化学键的两原子核的连线为轴作旋转操作,共价键电子云的图形不变,这种特征称为
。常见的δ键有“s-sδ键”、
、
。
π键:π键呈 对称,常见的有“ π键”
思考:如何判断δ键和π键?δ键和π键的稳定性如何?
2.写出下列微粒的电子式:Al Mg2+ O2- OH- NH4+ CaCl2 CO2
2、离子键与共价键比较
|
键型 |
离子键 |
共价键 |
|
(1)概念 |
|
|
|
(2)成键微粒 |
|
|
|
(3)形成条件 |
|
|
|
(4)用电子式表示形成过程 |
|
|
思考:1.离子键、共价键分别存在于哪些种类的物质中?
1、概念: ,叫做化学键,根据成键原子间的电负性差值可将化学键分为 和 。旧的化学键的断裂和新的化学键的生成是化学反应的本质,也是化学反应中能量变化的根本。
3.光谱:不同元素的原子发生跃迁时会吸收(基态→激发态)和放出(基态→激发态)能量,产生不同的光谱--原子光谱(吸收光谱和发射光谱)。利用光谱分析可以发现新元素或利用特征谱线鉴定元素。
试题枚举
[例1]下列有关电子云和原子轨道的说法正确的是( )
A.原子核外的电子象云雾一样笼罩在原子核周围,故称电子云
B.s能级的原子轨道呈球形,处在该轨道上的电子只能在球壳内运动
C.p能级的原子轨道呈纺锤形,随着能层的增加,p能级原子轨道也在增多
D.与s电子原子轨道相同,p电子原子轨道的平均半径随能层的增大而增大
解析: 电子云是对电子运动的形象化描述,它仅表示电子在某一区域内出现的概率,并非原子核真被电子云雾所包裹,故选项A错误。原子轨道是电子出现的概率约为90%的空间轮廓,它表明电子在这一区域内出现的机会大,在此区域外出现的机会少,故选项B错误。无论能层序数n怎样变化,每个p能级都是3个原子轨道且相互垂直,故选项C错误。由于按1p、2p、3p……的顺序,电子的能量依次增高,电子在离核更远的区域出现的概率逐渐增大,电子云越来越向更大的空间扩展,原子轨道的平均半径逐渐增大。
答案: D
[例2]下列有关认识正确的是( )
A.各能级的原子轨道数按s、p、d、f的顺序分别为1、3、5、7
B.各能层的能级都是从s能级开始至f能级结束
C.各能层含有的能级数为n-1
D.各能层含有的电子数为2n2
解析:各能层的能级都是从s能级开始,但不是至f能级结束,如L能层只有2s、2p两个能级,B错误;各能层含有的能级数与能层一致,以C不对;各能层最多容纳电子数为2n2,而不是必须含有的电子数2n2
答案:A
[例3]以下电子排布式表示基态原子电子排布的是( )
A.1s22s22p63s13p3 B.1s22s22p63s23p63d104s1 4p1
C.1s22s22p63s23p63d24s1 D.1s22s22p63s23p63d104s2 4p1
解析:A B C均不符合能量最低原理,选D
答案:D
[例4]人们常将在同一原子轨道上运动的,自旋方向相反的2个电子,称为“电子对”;将在同一原子轨道上运动的单个电子,称为“未成对电子”。以下有关主族元素原子的“未成对电子”的说法,错误的是( )
A.核外电子数为奇数的基态原子,其原子轨道中一定含有“未成对电子”
B.核外电子数为偶数的基态原子,其原子轨道中一定不含“未成对电子”
C.核外电子数为偶数的基态原子,其原子轨道中可能含有“未成对电子”
D.核外电子数为奇数的基态原子,其原子轨道中可能不含“未成对电子”
解析:s p d f 能级所含轨道数分别为1、3、5、7,均为奇数,而电子电子排布在同一能级的各个轨道时,优先占据不同的轨道,如两电子占据2p轨道分别占据两个轨道,形成两个未成对电子
答案: B D
[例5]以下是表示铁原子和铁离子的3种不同化学用语。
|
|
结构示意图 |
电子排布式 |
电子排布图(轨道表示式) |
|
铁原子 |
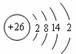 |
1s22s22p63s23p63d64s2 |
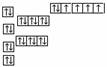 |
|
铁离子 |
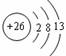 |
1s22s22p63s23p63d5 |
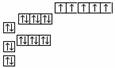 |
⑴铁原子最外层电子数为 ,铁在发生化学反应时,参加反应的电子可能是 。
⑵请你通过比较、归纳,分别说出3种不同化学用语所能反映的粒子结构信息。
答案:⑴2 4s上的2个电子或4s上的2个电子和3d上的1个电子
⑵结构示意图:能直观地反映核内的质子数和核外的电子层数及各能层上的电子数。
电子排布式:能直观地反映核外电子的能层、能级和各能级上的电子数。
轨道表示式:能反映各轨道的能量的高低及各轨道上的电子分布情况,自旋方向。
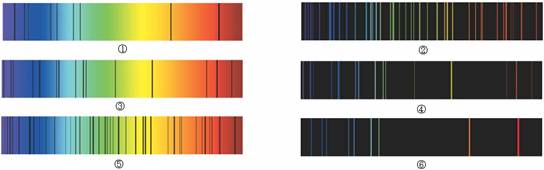
[例6]下图是锂、氦、汞的吸收光谱和发射光谱。其中图_____________是原子由基态转化为激发态时的光谱,图____________是原子由激发态转化为基态时的光谱。不同元素的原子光谱上的特征谱线不同,请在下图中用线段将同种元素的吸收光谱和发射光谱连接。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com