
14. 今有分子组成相差1个碳原子和若干个氢原子的两种单烯烃的混合物,若取该单烯烃混合物的质量为42g时,则其物质的量已大于1mol。在温度为120℃时向密闭容器中充入1mol混合烃和足量的氧气,引燃,待反应完全后,再恢复到120℃,容器内的压强比原来有所增大。
(1)试确定原混合烃中两种单烯烃的分子组成。
(2)为了使该混合烃对氧气的密度≥1.05g/cm3,且在上述条件下完全燃烧产生气体增加的物质的量≤0.3mol。通过计算,讨论两种烃的物质的量之比应满足什么条件。
分析:
(1)取单烯烃混合物为42g时,其物质的量>1mol。
∴混合烃的平均分子量≤42
∴该混合烃的组成C2H4和C3H6
(2)该混合烃的平均分子量≥33.6(1.05×32)
设混合烃中C3H6为x mol,C2H4为y mol
则 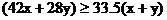
解得 
又∵燃烧产物增加的物质的量由C3H6燃烧所致

∴ 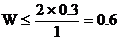
∴C2H4的物质的量≥0.4
∴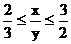
13. 向100g 25%的A醛溶液中加入B醛19g,B醛的分子式比A醛分子多一个CH2原子团。用2g这种混合醛溶液与足量的银氨溶液反应,析出了3.24g银,问A醛和B醛各是什么醛?
分析:解题的关键是抓住3.24g银的质量求出混合醛的物质的量,再根据混合醛的质量,求出混合醛的平均分子量,最后用不等式的讨论确定A醛和B醛。
设2g此溶液中A、B总的物质的量为xmol

2g混合溶液中含有A醛和B醛的质量为:
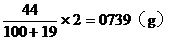
混合醛的平均分子量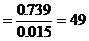
设A醛、B醛分子式分别为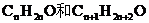 ,则A、B的分子量分别为14n+16、14n+30
,则A、B的分子量分别为14n+16、14n+30
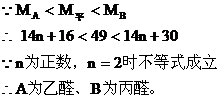
12. 80℃,101.3千帕下,用下图装置进行如下实验。A、C两筒内分别装有无色气体。它们可能是NH3、O2、N2、H2S、NO、CO2等气体,B管内装有固体。推动A的活塞使A筒中的气体缓缓地全部通过B进入C筒,C中的气体由无色变成红棕色,但其体积换算成同温同压下却并未变化。
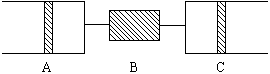
(1)C中发生的反应,其化学方程式是 。已知原C中的气体为单一气体,它是 。(若有多种可能答案,需一一列出。)将反应后C筒中的气体,用水吸收后,气体体积,减小一半,则与水反应前C中的气体是 。(若有多种答案需一一列出。)
(2)若实验开始前A、C中的气体体积(换算成标况)分别为1.40L和2.24L,且A中的气体经过B管后,B管增重1.40g,通过计算和推理可判定A中的气体是 ,其质量是 g。
分析:本题要求学生将分子量、物质的量、气体摩尔体积、化学方程式计算与元素及其化合物的性质结合起来,根据试题给出的条件,进行分析、推理和论证。
(1)由C筒中发生的化学现象气体由无色变为红综色,可判断C中发生的化学反应为:2NO+O2=2NO2;又根据C筒中的气体反应后并无体积变化,可知C中为NO,由B管进入C中气体为纯O2,反应后O2并未过量。与水反应后,气体体积减半,已知与水反应前C筒中的气体为NO2和NO的混合气。
(2)设与水反应前C筒中NO2的体积为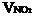 ,NO为
,NO为  ,根据题意列方程组:
,根据题意列方程组:
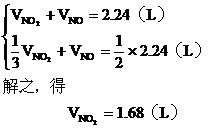
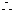 由B管进入C筒中的
由B管进入C筒中的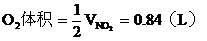
若0.84L O2全部由A筒中来,则A中除O2外,另一种气体的体积为1.40-0.84=0.56L,根据B管增重1.40g,该气体的mol尔质量为:

对照试题所给出的已知气体中没有一种气体的mol尔质量等于或大于56g/mol,因此该气体不是其中的一种,也不可能是其中两种或多种的混合气。由此可以确定C筒的O2可能全部或部分是由A中的某气体跟B管中的固体反应而得。已知气体能跟固体反应生成O2的只有CO2:

讨论:(1)若A中的气体全部是CO2(即进入C的O2全部由CO2和Na2O2反应而得。)根据反应方程式1.40L CO2与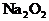 反应生成O2的体积为
反应生成O2的体积为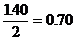 (L)这与进入C筒中O2的体积不符。(0.84 L)
(L)这与进入C筒中O2的体积不符。(0.84 L)
(2)若A中的气体是CO2和O2的混合气。设A中CO2和O2的体积分别为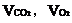 。
。
根据题意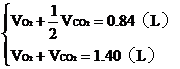
解题: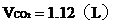
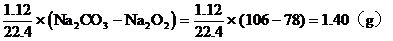
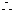 该结果与题设条件相符,所以A中的气体是CO2和O2的混合气体。
该结果与题设条件相符,所以A中的气体是CO2和O2的混合气体。
A中的气体的质量 。
。
11. 现有氧化铜和碳粉的混合物共Amol,将它在隔绝空气条件下加热,反应完全后,冷却,得到残留固体。
(1)写出可能发生反应的化学方程式
(2)若氧化铜在混合物中的量的比值为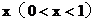
问:x为何值时,残留固体为何种物质?写出残留固体的物质的量与x值之间 的关系。将结果填入下表。
|
|
残 留 固 体 |
|
|
x值 |
分 子 式 |
物质的量 |
|
|
|
|
分析:(1)首先写出有关的化学反应方程式,根据化学方程式中有关物质间的物质的量的关系,分析当CuO恰好完全反应时,x值是多少?
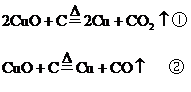
按①式反应,x值为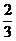 时,反应物恰好反应;按②式反应,x值为
时,反应物恰好反应;按②式反应,x值为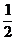 时,反应物恰好完全反应。
时,反应物恰好完全反应。
(2)当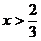 时,CuO过量,按C的量计算。
时,CuO过量,按C的量计算。
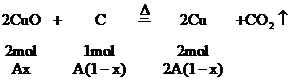
剩余CuO的物质的量
(3)当 不足量,按CuO的量计算,生成铜的量为Ax。
不足量,按CuO的量计算,生成铜的量为Ax。
(4)当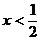 时,C过量,按②式中的CuO的量计算,生成铜为Ax,剩余C的物质的量为:
时,C过量,按②式中的CuO的量计算,生成铜为Ax,剩余C的物质的量为:
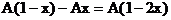
将所得结果的有关数值填入下表:
|
x 值 |
残 留 固 体 |
|
|
|
分 子 式 |
物 质 的 量 |
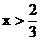 |
Cu CuO |
2A(1-x) A(3x-2) |
 |
Cu |
Ax(或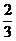 A) A) |
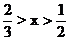 |
Cu |
Ax |
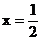 |
Cu |
Ax(或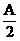 ) ) |
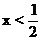 |
Cu C |
Ax A(1-2x) |
10. 两种烃的混合气体20mL,跟过量的氧气混合点燃,当产物通过浓H2SO4时,体积减小30mL,通过碱石灰后的体积又减少40mL(以上均换算成标准状况的体积),问该混合物的组成可能有几种?在各种可能组成中,每种烃各是多少?
分析:气态烃的碳原子数都小于4。20mL混合烃完全燃烧生成40mL CO2和30mL水蒸气,可知1mol混合烃平均含2mol C原子和3mol H原子,从而推知,该混合烃只能是C2H6和C2H2或C2H4和C2H2的混合物。
讨论:
(1)若混合烃含有x mL C3H6,则含有(20-x)mL C2H2
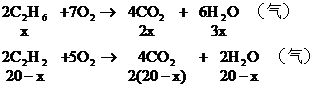
由题意可知:

C2H2:20-5=15(mL)
(2)若混合烃含有y mL C2H4,则含有 ,
,
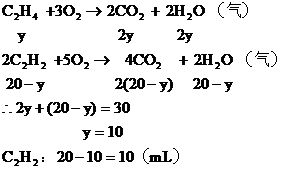
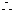 可能有两种组合
可能有两种组合
9. 混合两种未知物的溶液,生成1.25g沉淀,这个沉淀是二价金属盐。在1000℃灼烧,使沉淀完全分解,得到质量为0.70g的固体金属氧化物和另一种使石灰水变浑浊的无刺激性气味的气体。蒸发滤除沉淀后的溶液,得到2.0g干燥残渣。在200℃时慢慢加热残渣,使它分解仅得到两种产物:一种是气态氧化物,标况下的体积为0.56L,另一种是水,为0.90g,试确定未知物是什么,并写出有关推理,计算过程及化学方程式。
分析:能使石灰水变浑浊且无刺激性气味的气体应是CO2,故1.25g沉淀应为碳酸盐。
设碳酸盐的分子式为MCO3
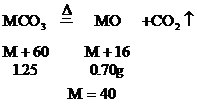
 此二价金属为Ca。
此二价金属为Ca。
 滤液蒸干后得2.0g残渣,受热分解为0.90g水和0.56L气态氧化物。
滤液蒸干后得2.0g残渣,受热分解为0.90g水和0.56L气态氧化物。
 此气态氧化物的mol尔质量为:
此气态氧化物的mol尔质量为:
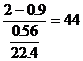 (g/mol)
(g/mol)
分解产物的mol尔比:
H2O∶RxOy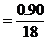 ∶
∶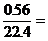 0.05∶0.025
0.05∶0.025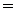 2∶1
2∶1
 分解产物为H2O和气态氧化物,分解温度为200℃,故此盐为铵盐,并不可能是碳酸铵或碳酸氢按(因分解产物是3种)
分解产物为H2O和气态氧化物,分解温度为200℃,故此盐为铵盐,并不可能是碳酸铵或碳酸氢按(因分解产物是3种)
 此盐只能是NH4NO3
此盐只能是NH4NO3
设其分解产物为H2O和NxOy
则对NxOy而言有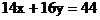
则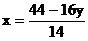
讨论,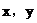 均为正整数,且只可能是1或2,
均为正整数,且只可能是1或2,
(1)若
(2)若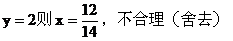
由此可肯定此盐为NH4NO3,热分解产物为H2O和N2O。
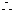 未知物是
未知物是
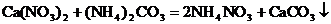
8.某金属R 7g跟足量的盐酸反应,在标准状况下,可得2.8L氢气;11.2g该金属可跟21.3g氯气完全反应,生成相应的氯化物,求该金属的原子量。
分析:设R的原子量为m,两种金属氯化物的分子式分别为RClx和RCly
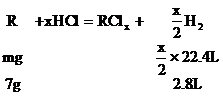
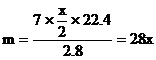 ………①
………①
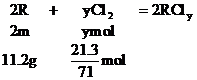
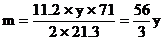 ………②
………②
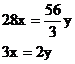
讨论:(1)当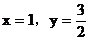 不合理
不合理
(2)当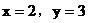 合理
合理
(3)当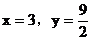 不合理
不合理
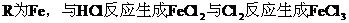
7.向含0.02mol Al3+的明矾溶液中,逐滴加入0.1mol/L的Ba(OH)2溶液时,产生沉淀的质量y(g)与Ba(OH)2溶液的体积x(mL)的关系如图所示。求图中:
V1=
V2=
m1=
m2=
分析:本题要从分析图中所体现的产生沉淀的质量与加入Ba(OH)2体积的函数关系求出V1、V2和m1、m2的值。
从图中可以看出,当加入V1mL的Ba(OH)2时,可得沉淀m1 g,沉淀为BaSO4和Al(OH)3,当加入V2mL Ba(OH)2时,Al(OH)3溶解,沉淀仅为BaSO4。
(1)含有0.02mol Al3+的明矾溶液中含有0.04mol的SO42-。
当加入V1mL Ba(OH)2时,
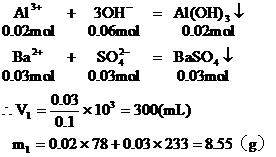
(2)当加入V2mL Ba(OH)2溶液时,
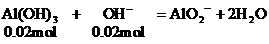
6. 将5.000gNaCl、NaBr、CaCl2的混合物溶于水,通入氯气充分反应,然后把溶液蒸干并灼烧,得残留物4.914g。灼烧后的残留物再溶于水,并加足量的Na2CO3溶液,所得沉淀经干燥后质量为0.270g。求混合物中各化合物的质量百分组成。
分析:根据题意可列出下图示,帮助审清题意,找出思路和解法。
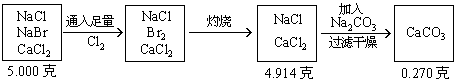
根据图示可分析:
(1)CaCO3的质量为0.270g,由它可求出CaCl2的质量。
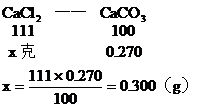
(2)混合物中通入Cl2
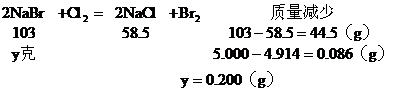
(3)NaCl的质量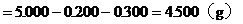
(4)各组分的百分含量
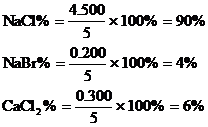
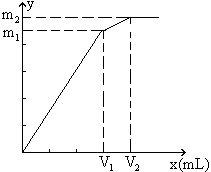
5. 氯气通入氨水中发生下列反应: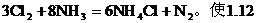 L氯、氮混合气(90%Cl2、10%的N2)通入浓氨水实验测得逸出气体在标况下为0.672L(50%的Cl2、50%的N2),问在反应中有多少g氨被氧化?
L氯、氮混合气(90%Cl2、10%的N2)通入浓氨水实验测得逸出气体在标况下为0.672L(50%的Cl2、50%的N2),问在反应中有多少g氨被氧化?
分析:设有xg氮气被氧化
由方程式可得出:
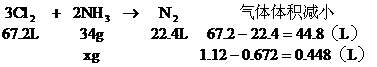
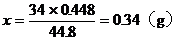
答:略。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com