
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
6.ЧтЦјдкТШЦјжаШМЩеЪБВњЩњВдАзЩЋЛ№бцЁЃдкЗДгІЙ§ГЬжаЃЌЦЦЛЕ1 molЧтЦјжаЕФЛЏбЇМќЯћКФЕФФмСПЮЊQ 1 kJ?ЃЌЦЦЛЕ1 molТШЦјжаЕФЛЏбЇМќЯћКФЕФФмСПЮЊQ2 kJЃЌаЮГЩ1 molТШЛЏЧтЦјЬхжаЕФЛЏбЇМќЪЭЗХЕФФмСПЮЊQ3 kJЁЃЯТСаЙиЯЕжае§ШЗЕФЪЧ(ЁЁЁЁ )ЁЁ
A.Q1+Q2>Q3ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ B.Q1+Q2>2Q3ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ C.Q1+Q2<Q3ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ D.Q1+Q2<2Q3ЁЁ
5.вбжЊ(1)H2(g)+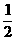 O2(g)==H2O(g)ЁЁ
O2(g)==H2O(g)ЁЁ
ІЄH1 =a kJЁЄmol-1?ЁЁ
(2)2H2(g)+O2(g)==2H2O(g)ЁЁ
ІЄH2 =b kJЁЄmol-1??ЁЁ
(3)H2(g)+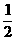 O2(g)==H2O(l)ЁЁ
O2(g)==H2O(l)ЁЁ
ІЄH3 =c kJЁЄmol-1??ЁЁ
(4)2H2(g)+O2(g)==2H2O(l)ЁЁ
ІЄH4 =d kJЁЄmol-1??ЁЁ
ЯТСаЙиЯЕЪНжае§ШЗЕФЪЧ(ЁЁЁЁ )ЁЁ
A.a<c<0 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ B.b>d>0 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ C.2a=b<0 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ D.2c=d>0
4.вбжЊЛЏбЇЗДгІ2C+O2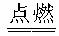 2COЃЌ2CO+O2
2COЃЌ2CO+O2 2CO2ЖМЪЧЗХШШЗДгІЃЌОнДЫХаЖЯЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ(ЁЁЁЁ )ЁЁ
2CO2ЖМЪЧЗХШШЗДгІЃЌОнДЫХаЖЯЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ(ЁЁЁЁ )ЁЁ
A. 12 gЬМЫљОпгаЕФФмСПвЛЖЈИпгк 28 g COЫљОпгаЕФФмСПЁЁ
B.56 g COКЭ32 g O2ЫљОпгаЕФзмФмСПДѓгк88 g CO2ЫљОпгаЕФзмФмСПЁЁ
C.12 g C КЭ32 g O2ЫљОпгаЕФзмФмСПДѓгк44 g CO2ЫљОпгаЕФзмФмСПЁЁ
D.НЋвЛЖЈжЪСПЕФCШМЩеЃЌЩњГЩCO2БШЩњГЩCOЪБЗХГіЕФШШСПЖрЁЁ
3.вбжЊдк25 ЁцЁЂ101 kPaЯТЃЌ1 g C8H18(аСЭщ)ШМЩеЩњГЩЖўбѕЛЏЬМКЭвКЬЌЫЎЪБЗХГі48.40 kJШШСПЃЌБэЪОЩЯЪіЗДгІЕФШШЛЏбЇЗНГЬЪНе§ШЗЕФЪЧ(ЁЁЁЁ )ЁЁ
A.C8H18(l)+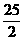 O2(g)==8CO2(g)+?9H2O(g)?ЁЁ
O2(g)==8CO2(g)+?9H2O(g)?ЁЁ
ІЄH =-48.40 kJЁЄmol-1?ЁЁ
B.C8H18(l)+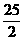 O2(g)==8CO2(g)+9H2O(l)ЁЁ
O2(g)==8CO2(g)+9H2O(l)ЁЁ
ІЄH=-5 518 kJЁЄmol-1?ЁЁ
C.C8H18(l)+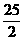 O2(g)==8CO2(g)+?9H2O(l)?ЁЁ
O2(g)==8CO2(g)+?9H2O(l)?ЁЁ
ІЄH =+5 518 kJЁЄmol-1?ЁЁ
D.C8H18(l)+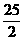 O2(g)==8CO2(g)+?9H2O(l)?ЁЁ
O2(g)==8CO2(g)+?9H2O(l)?ЁЁ
ІЄH =-48.40 kJЁЄmol-1?ЁЁ
2.вбжЊH-ClМќЕФМќФмЮЊ431.4 kJЁЄmol-1ЃЌЯТСаЙигкМќФмЕФа№Ъіе§ШЗЕФЪЧ(ЁЁЁЁ )ЁЁ
A.УПЩњГЩ2 mol H-ClМќЗХГі431.4 kJФмСПЁЁ
B.УПЩњГЩ1 mol H-ClМќЮќЪе431.4 kJФмСПЁЁ
C.УПВ№ПЊ1 mol H-ClМќЗХГі431.4 kJФмСПЁЁ
D.УПВ№ПЊ1 mol H-ClМќЮќЪе431.4 kJФмСПЁЁ
1.ЖдгкЗХШШЗДгІ2H2+O2 2H2OЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ(ЁЁЁЁ )ЁЁ
2H2OЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ(ЁЁЁЁ )ЁЁ
A.ВњЮяH2OЫљОпгаЕФзмФмСПИпгкЗДгІЮяH2КЭO2ЫљОпгаЕФзмФмСПЁЁ
B.ЗДгІЮяH2КЭO2ЫљОпгаЕФзмФмСПИпгкВњЮяH2OЫљОпгаЕФзмФмСПЁЁ
C.ЗДгІЮяH2КЭO2ЫљОпгаЕФзмФмСПЕШгкВњЮяH2OЫљОпгаЕФзмФмСПЁЁ
D.ЗДгІЮяH2КЭO2ОпгаЕФФмСПЯрЕШЁЁ
2.ШМСЯЪЙгУаЇТЪЕФЬсИп
ЁЁ ШМСЯГфЗжШМЩеЭЈГЃашвЊПМТЧСНЕуЃК
(1)зуЙЛЖрЕФПеЦјЃЛ
(2)ШМСЯгыПеЦјвЊгазуЙЛДѓЕФНгДЅУцЛ§ЁЃЁЁ
ЙЎЙЬСЗЯА
1.РћгУШШжЕКтСПШМСЯЭъШЋШМЩеЗХГіШШСПЕФЖрЩй
(1)ШМСЯЕФЭъШЋШМЩеЪЧжИЮяжЪжаКЌгаЕФЕЊдЊЫизЊЛЏЮЊN2(g)ЃЌЧтдЊЫизЊЛЏЮЊH2O(l)ЃЌЬМдЊЫизЊЛЏЮЊCO2(g)ЁЃ
(2)КтСПШМЩеЗХГіШШСПЕФДѓаЁЛЙПЩгУБъзМШМЩеШШЁЃдк101 kPaЕФбЙЧПЯТЃЌ1 molЮяжЪЭъШЋШМЩеЕФЗДгІШШНазіИУЮяжЪЕФБъзМШМЩеШШЁЃ
11.1 gЧтЦјдкбѕЦјжаШМЩеЩњГЩвКЬЌЫЎЃЌЗХГі142.9 kJЕФШШСПЃЌаДГіИУЗДгІШМЩеЕФШШЛЏбЇЗНГЬЪНЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
зЪСЯПЈЦЌ
ЩёУиЕФздШМЯжЯѓЁЁ
ДгЧАЃЌЙХТоТэЕлЙњЕФвЛжЇХгДѓДЌЖгвЋЮфбяЭўЕиГіКЃдЖеїЁЃДЌЖгЪЛНќКьКЃЃЌЭЛШЛЃЌвЛЫвзюДѓЕФИјбјДЌЩЯУАГіСЫЙіЙіХЈбЬЃЌекЬьБЮШеЁЃдЖеїЕФеНДЌЖгжЛКУЪеЗЋзЊЖцЃЌЗЕКНЛиИлЁЃЭГЫЇВЂВЛИЪаФЃЌЗбОЁаФЛњвЊВщГіИјбјДЌЦ№Л№ЕФдвђЁЃПЩВщРДВщШЅЃЌДгЫОСюЙйвЛжБВщЕНЛяЗђЃЌУЛгаШЮКЮШЫШЅЕуЛ№ЁЂЗХЛ№ЁЃетзЎРњЪЗЦцАИЛЙЪЧКѓРДЕФПЦбЇМвУЧбаОПГіСЫЦ№Л№ЕФдвђЁЃдРДЪЧИјбјДЌЕФЕзВеРяЖбЛ§ЕУбЯбЯЪЕЪЕЕФВнздЗЂШМЩеЦ№РДЕФЁЃетжжЯжЯѓНаздШМЁЃ
ЁЁ ЧсЫЩвЛЬтЃКЁЁ ВнЮЊЪВУДЛсздШМЃП
ЁЁ
Д№АИЃКЁЁ ИјбјДЌЕзВеЕФВнШћЕУУмВЛЭИЗчЃЌгаЕФПЊЪМЛКТ§ЕибѕЛЏЃЌетЪЕМЪЩЯЪЧвЛжжГйЛКЕФЁАШМЩеЁБЃЌЗХГіШШРДЃЌШШЩЂВЛГіШЅЃЌШШСПдНОлдНЖрЃЌЮТЖШЩ§ИпЃЌжегкДяЕНВнЕФзХЛ№ЕуЃЌОЭздЗЂЕизХЛ№СЫЁЃ ЁЁ
ЁЁ
ЁЁ здЮвЗДРЁЁЁ
ЁЁ ЕМбЇдАЕиЁЁ
?
ЕкЖўПЮЪБЁЁ ШМСЯШМЩеЪЭЗХЕФШШСП
ЕМбЇдАЕи
10.егЦјЕФжївЊГЩЗжЪЧCH4ЁЃ0.5 mol CH4ЭъШЋШМЩеЩњГЩCO2КЭвКЬЌH2OЪБЃЌЗХГі445 kJШШСПЁЃаДГіCH4ШМЩеЕФШШЛЏбЇЗНГЬЪНЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com