
题目列表(包括答案和解析)
7.除去溶解在苯中的少量苯酚,正确的方法是
A.用过滤器过滤
B.用分液漏斗分液
C.加入足量浓溴水后再过滤
D.加入适量NaOH溶液,反应后再分液
6.将肥皂溶于热的蒸馏水中,冷却后滴加盐酸,得到的白色固体是
A.氯化钠 B.甘油 C.硬脂酸钠 D.硬脂酸
5. 聚丙烯酸酯类涂料是目前市场上流行的墙面涂料之一,它具有弹性好、不易老化、耐擦洗、色泽亮丽等优点.下边是聚丙烯酸酯的结构简式,它属于
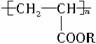
①无机化合物 ②有机化合物 ③高分子化合物 ④离子化合物 ⑤共价化合物
A.①③④ B.①③⑤ C.②③⑤ D.②③④
4. 下列说法正确的是
A.煤的干馏、石油的分馏分别是化学变化、物理变化
B.蚕丝、羊毛和淀粉分别属于纤维素、蛋白质和多糖
C.丁烷有3种同分异构体
D.油脂、淀粉、葡萄糖、蛋白质均能发生水解反应
3.在医院对某类病人的尿液进行检查时常把氢氧化钠溶液和硫酸铜溶液加入到其尿液中并加热,如果观察到产生红色沉淀,说明该尿液中含有
A.食醋 B.白酒 C.食盐 D.葡萄糖
2.下列物质中属于高分子化合物的是
A.脂肪 B.棉花 C.蔗糖 D.甘油
1.当前我国环保亟待解决的 “白色污染”,通常所指的是
A.冶炼厂的白色烟尘 B.石灰窑的白色粉尘
C.聚乙烯等塑料垃圾 D.白色建筑废料
28、(5分)在某温度下,将H2和I2各0.10mol 的气态混合物充入10L的密闭容器中,充分反应,达到平衡后,测得 c(H2) = 0.0080mol/L 。
(1)(2分)求该反应的平衡常数。
(2)(2分)在上述温度下,该容器中若通入H2和I2各1.0mol 的气态混合物,试求达到化学平衡状态时各物质的浓度。
(3)(1分)利用本题数据,请你说出关于化学反应速率或化学平衡的一点与数据有关的结论。
27、(12分)为了测定某浓硫酸样品的物质的量浓度,进行了以下实验操作:
A、冷却至室温后,在100mL容量瓶中定容配成100mL稀硫酸。
B、用某仪器量取20.00mL稀硫酸于锥形瓶中并滴入几滴指示剂。
C、将酸式滴定管和碱式滴定管用蒸馏水洗涤干净,并用各待盛溶液润洗。
D、将物质的量浓度为M mol/L的标准NaOH溶液装入碱式滴定管,调节液面记下开始读数为V1mL。
E、在锥形瓶下垫一张白纸,滴定至恰好反应为止,记下读数为V2mL。
F、把锥形瓶移到碱式滴定管下小心滴入NaOH标准溶液,边滴边摇动锥形瓶。
G、用某仪器准确量取浓硫酸样品10.00 mL,在烧杯中用蒸馏水溶解。
就此实验操作完成下列填空:
(1)正确操作步骤的顺序(用字母填写) → A → → → → → 。
(2)滴定中可选用的指示剂是 。滴定中,目光应注视 ;判断滴定恰好完成的依据是 ;
(3)某学生实验时用稀硫酸润洗了锥形瓶,测定的浓度会偏 。(填“大或小”)
(4)该浓硫酸样品纯度的计算式为 。
(5)若用0.1000 mol/L的NaOH溶液滴定20.00mL0.1000 mol/L的CH3COOH溶液,跟踪测试和记录的滴定过程中溶液PH的结果如下,ⅰ、请根据下表数据绘制PH随加入NaOH溶液的滴定曲线。(下图坐标中横坐标表示滴入CH3COOH溶液的体积,纵坐标表示PH值)
|
滴入HAc的体积 |
0.00 |
18.00 |
19.80 |
19.98 |
20.00 |
20.02 |
20.20 |
40.00 |
|
|
PH |
2.88 |
5.70 |
6.74 |
7.75 |
8.73 |
9.70 |
10.70 |
12.52 |
|
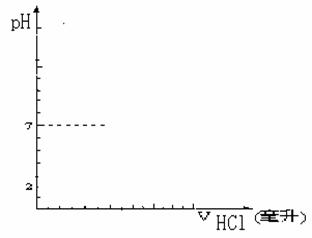
ⅱ、依据上表数据或滴定曲线可得出: ①CH3COOH是 (填“强”、“弱”或“非” )电解质。 ②在接近滴定终点(PH为7)时,一滴(约0.04mL)NaOH溶液就引起了溶液PH从 到 的突变。
26、(8分)结合以下表中信息,回答有关问题:
|
组号 |
反应温度 (℃) |
参加反应的物质 |
||||
|
Na2S2O3 |
H2SO4 |
H2O |
||||
|
V/ml |
c/mol·L- |
V/ml |
c/mol·L- |
V/ml |
||
|
A |
10 |
5 |
0.1 |
5 |
0.1 |
5 |
|
B |
10 |
5 |
0.1 |
5 |
0.1 |
10 |
|
C |
30 |
5 |
0.1 |
5 |
0.1 |
10 |
|
D |
30 |
5 |
0.2 |
5 |
0.2 |
10 |
(1)实验比较法是人们研究各类问题常用的方法,但在比较某一因素对实验产生的影响时,必须排除其他因素的变动和干扰,即需要控制好与实验有关的各项反应条件。
上述表中可以比较的组合有 。
(2)上述反应的离子方程式为
(3)上述反应速率最快的是 ,最慢的是 。
(4)判断上述反应速率快慢的实验现象可以是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com