
题目列表(包括答案和解析)
3.已知反应Ba(OH)2•8H2O+2NH4Cl =BaCl2+ 2NH3•H2O+8H2O为吸热反应,对该反应
的下列说法中正确的是
A.因该反应为吸热反应,故必需加热才能发生
B.Ba(OH)2•8H2O、NH4Cl的总能量一定低于BaCl2、NH3•H2O、H2O的总能量
C. Ba(OH)2•8H2O的能量一定低于BaCl2;NH4Cl的能量一定低于NH3•H2O
D.破坏Ba(OH)2•8H2O、NH4Cl中化学键所吸收的能量小于形成CaCl2、NH3•H2O、H2O中化学键所放出的能量
2. 将铁粉和硫粉混合后加热,待反应一发生即停止加热,反应仍可持续进行,直至
反应完全生成新物质硫化亚铁。该现象说明了
A.该反应是吸热反应 B.铁粉和硫粉在常温下能自发反应
C.该反应是放热反应
D.生成物硫化亚铁的总能量高于反应物铁粉和硫粉的总能量
1.下列说法中正确的是
A.熵增加且放热的反应一定是自发反应
B.非自发反应在任何条件下都不能实现
C.凡是放热反应都是自发的,吸热反应都是非自发的
D.自发反应一定是熵增大,非自发反应一定是熵减小或不变
25. 煤等化石燃料燃烧时产生的SO2会对大气造成污染。若某家庭取暖每天燃烧6.4kg 煤,煤中硫元素的质量分数为1%。假设煤中的硫全部转化为SO2,试计算每天产生的SO2的物质的量是多少?

 宿州市2010-2011学年度第一学期期中学业水平检测
宿州市2010-2011学年度第一学期期中学业水平检测
24、(10分)糖类、油脂、蛋白质能在人体中 (填“氧化” 或“还原” ),供给人体所需要的能量。其中 是含热能最高的营养物质。根据溶解性的不同,维生素B类属于 溶性维生素,维生素D 属于 溶性维生素。几百年前哥伦布船队船员长期食用面包,饼干,咸肉导致患坏血病,患病船员采食野果后,大多数能恢复健康,这是因为野果中含
23.(8分)人的胃液是一种无色液体,呈酸性,pH在0.9-1.5之间, 其中H+ 的浓度比血液中高几万倍,回答下列问题:
(1)胃液有帮助人体消化食物等多种功能,胃酸的主要成分是
(2)某品牌抗酸药的主要成分有糖衣、碳酸氢钠、氢氧化铝、淀粉。
①.写出该抗酸药发挥功效时的化学方程式:
②.淀粉在抗酸药中作填充剂、粘合剂,淀粉在人体内酶的催化作用下发生水解反应,最终转化为(写分子式)
22.(6分)(1)自来水厂用氯气进行消毒,改善水质,因为氯气与水反应会生成盐酸和次氯酸(HClO),次氯酸具有杀菌消毒作用,其反应化学方程式为: ___________________________________________________________
(2)高铁酸钾(K2FeO4)是新型、高效的水处理剂,其氧化性比氯气、臭氧等更强,且是一种无机絮凝剂,更重要的是整个过程不会引入对人体有害的有机氯等物质。
①高铁酸钾中铁元素的化合价为_______
②请再写一种能除去水中悬浮颗粒的絮凝剂的名称_______
21.(10分)请填写下列空白。
(1)在二氧化碳、二氧化硫、二氧化氮、氟利昂中,能引起温室效应的气体是_______;能造成臭氧层空洞的物质是_______;造成酸雨的主要因素是_______和二氧化硫含量的增加。
(2)某日空气中各种污染物的污染指数分别为:二氧化硫66,二氧化氮50,可吸入颗粒120。该地区的当日首要污染物是 ,当日空气污染指数是
20.低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:
2NH3(g)+NO(g)+NO2(g) 2N2(g)+3H2O(g)
2N2(g)+3H2O(g) 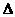 H<0
H<0
在恒容的密闭容器中,下列有关说法正确的是
A.平衡时,其他条件不变,升高温度可使该反应的平衡常数增大
B.平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小
C.单位时间内消耗1molNO同时消耗2molN2,则反应达到平衡状态
D.其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大

 宿州市十三所重点中学2010-2011学年度第一学期
宿州市十三所重点中学2010-2011学年度第一学期
19.对于反应2A(气)+xB(气)  4C(气)达到平衡时,C的浓度为1.2mol/L,当其它条件不变,把体积扩大1倍时,测得C的浓度为0.7mol/L,则x的值为
4C(气)达到平衡时,C的浓度为1.2mol/L,当其它条件不变,把体积扩大1倍时,测得C的浓度为0.7mol/L,则x的值为
A.1 B.2 C.3 D.4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com