
̀âÄ¿Áбí(°üÀ¨´đ°¸ºÍ½âÎö)
15£®ËµĂ÷¿ÉÄæ·´Ó¦A(g)+B(g) C(g)+D(g)ÔÚ̉»¶῭ơ¼₫ÏẨÑ´ïµ½»¯Ñ§Æ½
C(g)+D(g)ÔÚ̉»¶῭ơ¼₫ÏẨÑ´ïµ½»¯Ñ§Æ½
ºâ×´̀¬µÄÊÂʵÊÇ¡£¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
A£®ÈƯÆ÷ÄÚѹǿ²»Ëæʱ¼äµÄ±ä»¯¶ø±ä»¯¡¡¡¡¡¡ B£®ÈƯÆ÷ÄÚA¡¢B¡¢C¡¢DËÄƠß¹²´æ
C£®A¡¢DµÄÏûºÄËÙÂÊÏàµÈ¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡ D£®C¡¢DµÄÉú³ÉËÙÂÊÏàµÈ
14£®½«4 mol AÆø̀åºÍ2 mol BÆø̀åÔÚ2 LµÄÈƯÆ÷ÖĐ»́ºÏ²¢ÔÚ̉»¶῭ơ¼₫Ï·¢ÉúÈçÏ·´Ó¦£º 2A(g)+B(g)£½2C(g)¡£Èô¾2sºó£¬²âµĂCµÄŨ¶ÈΪ 0.6 mol¡¤L£1 £¬ÏÖÓĐÏÂÁĐ¼¸ÖÖ˵·¨£º
¢Ù ÓĂÎïÖÊ A ±íʾµÄ·´Ó¦µÄƽ¾ùËÙÂÊΪ 0.3 mol¡¤L£1¡¤s£1¡¡ ¢Ú ÓĂÎïÖÊ B±íʾµÄ·´Ó¦µÄ
ƽ¾ùËÙÂÊΪ 0.6 mol¡¤L£1¡¤s£1¡¡ ¢Û 2 s ʱÎïÖÊ A µÄת»¯ÂÊΪ70%¡¡ ¢Ü 2 s ʱÎïÖÊ B µÄŨ¶ÈΪ 0.7 mol¡¤L£1¡¡¡¡ ÆäÖĐƠưÈ·µÄÊÇ
A£®¢Ù ¢Û¡¡¡¡¡¡¡¡¡¡ B£®¢Ù ¢Ü¡¡¡¡¡¡¡¡ C£® ¢Ú ¢Û¡¡¡¡¡¡¡¡ D£®¢Û ¢Ü
13£®ÏÂÁĐĐđÊöƠưÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡ A£®ÓöèĐԵ缫µç½â±¥ºÍNaClÈÜ̉º£¬ÈôÓĐ1 molµç×Óת̉Æ£¬ỘÉú³É1 mol NaOH
¡¡ B£®ÓöèĐԵ缫µç½âNa2SO4ÈÜ̉º£¬̉ơÑôÁ½¼«²úÎïµÄÎïÖʵÄÁ¿Ö®±ÈΪ1¡Ă2
¡¡ C£®ÔÚÔµç³ØµÄ¸º¼«ºÍµç½â³ØµÄ̉ơ¼«É϶¼·¢Éúʧµç×ÓµÄÑơ»¯·´Ó¦
¡¡ D£®¶Æ²ăÆÆËđºó£¬¶ÆÎừú°å±È¶ÆĐ¿̀ú°å¸üÄ͸¯Ê´
12£®X¡¢Y¡¢Z¡¢M´ú±íËÄÖÖ½đÊôÔªËØ¡£½đÊôXºÍZÓõ¼ÏßÁ¬½Ó·ÅÈëÏ¡Ạ́ËáÖĐʱ£¬Z
¼«ÉÏÓĐH2·Å³ö£»Èôµç½âY2+ºÍZ2+¹²´æµÄÈÜ̉ºÊ±£¬YÏÈÎö³ö£»ÓÖÖªM2+µÄÑơ»¯ĐÔÇ¿ÓÚY2+¡£ỘƠâËÄÖÖ½đÊôµÄ»î¶¯ĐÔÓÉÇ¿µ½ÈơµÄ˳Đ̣Ϊ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ A£®X>Z>Y>M¡¡ ¡¡¡¡¡¡¡¡¡¡ B£®X>Y>Z>M¡¡ C£®M>Z>X>Y¡¡¡¡ ¡¡¡¡¡¡¡¡ D£®X>Z>M>Y
10£®¸ù¾Ư·´Ó¦Îª 2Cu+O2+CO2+H2O£½Cu2(OH)2CO3£¬
Éè¼ÆÈçÓ̉ͼËùʾԵç³Ø£¬ÏÂÁĐ˵·¨´íÎóµÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
A£®X¿É̉ÔÊÇ̉ø»̣ʯī
B£®µç×Ó´Ó͵缫¾Íâµç·Á÷Ị̈Xµç¼«
¡¡ C£®YÊÇẠ́ËáÍÈÜ̉º¡¡¡¡ ¡¡¡¡¡¡D£®X¼«Éϵĵ缫·´Ó¦Ê½Îª O2+2H2O+4e- = 4OH-
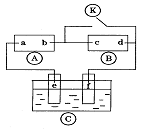 ¡¡
11£®Ó̉ͼ
¡¡
11£®Ó̉ͼ ΪֱÁ÷µçÔ´£¬
ΪֱÁ÷µçÔ´£¬ Ϊ½₫͸±¥ºÍÂÈ»¯ÄÆÈÜ̉ººÍ·Ó̀ªÊỔºµÄÂËÖ½£¬
Ϊ½₫͸±¥ºÍÂÈ»¯ÄÆÈÜ̉ººÍ·Ó̀ªÊỔºµÄÂËÖ½£¬ Ϊµç¶Æ²Û£®½Óͨµç·ºó·¢ÏÖ
Ϊµç¶Æ²Û£®½Óͨµç·ºó·¢ÏÖ ÉϵÄcµăÏÔº́É«£®ÎªÊµÏÖ̀úÉ϶ÆÍ£¬½Óͨ
ÉϵÄcµăÏÔº́É«£®ÎªÊµÏÖ̀úÉ϶ÆÍ£¬½Óͨ ºó£¬Ê¹c¡¢dÁ½µă¶̀·£®ÏÂÁĐĐđÊöƠưÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
ºó£¬Ê¹c¡¢dÁ½µă¶̀·£®ÏÂÁĐĐđÊöƠưÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡ A£®aΪֱÁ÷µçÔ´µÄ¸º¼«
¡¡ B£®c¼«·¢ÉúµÄ·´Ó¦ÎªO2+4e£+2H2O£½4OH£
¡¡ C£®fµç¼«Îª̀ú°å¡¡¡¡¡¡¡¡ D£®µç½âÖÊÈÜ̉º²»ÄÜÓĂCuCl2ÈÜ̉º
8£®ÏÂÁĐÓĐ¹Ø»¯Ñ§·´Ó¦ËÙÂʵÄ˵·¨ÖĐ£¬ƠưÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡ A£®100mL 2 mol¡¤L£1ÑÎËáÓëĐ¿·´Ó¦Ê±£¬¼ÓÈëÊÊÁ¿µÄÂÈ»¯ÄÆÈÜ̉º£¬Éú³ÉÇâÆøµÄËÙÂʲ»±ä
¡¡ B£®ÓẰúƬºÍÏ¡Ạ́Ëá·´Ó¦ÖÆÈ¡ÇâÆøʱ£¬¸ÄÓẰúƬºÍŨẠ́Ëá¿É̉Ô¼Ó¿́²úÉúÇâÆøµÄËÙÂÊ
¡¡ C£®¶₫Ñơ»¯Ạ́µÄ´ß»¯Ñơ»¯ÊÇ̉»¸ö·ÅÈÈ·´Ó¦£¬Ëù̉ÔÉư¸ßζȣ¬·´Ó¦ËÙÂʼơÂư
¡¡ D£®Æû³µÎ²ÆøÖеÄCOºÍNO¿É̉Ô»ºÂư·´Ó¦Éú³ÉN2ºÍCO2£¬¼ơĐ¡Ñ¹Ç¿£¬·´Ó¦ËÙÂʼơÂư¡¡¡¡ 9. ÓẰúƬÓëÏ¡Ạ́Ëá·´Ó¦ÖÆÈ¡ÇâÆøʱ£¬ÏÂÁĐ´ëÊ©²»ÄÜʹÇâÆøÉú³ÉËÙÂʼӴóµÄÊÇ
¡¡A. ¼ÓÈÈ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡B. ²»ÓĂÏ¡Ạ́Ëᣬ¸ÄÓĂ98%ŨẠ́Ëá
 ¡¡¡¡ C. µÎ¼ÓÉÙÁ¿CuSO4ÈÜ̉º¡¡¡¡ D. ²»ÓẰúƬ£¬¸ÄÓẰú·Û
¡¡¡¡ C. µÎ¼ÓÉÙÁ¿CuSO4ÈÜ̉º¡¡¡¡ D. ²»ÓẰúƬ£¬¸ÄÓẰú·Û
7£®ÔÚÀíÂÛÉϲ»ÄÜÓĂÓÚÉè¼ÆÔµç³ØµÄ»¯Ñ§·´Ó¦ÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡ A£®NaCl(aq)+ AgNO3(aq)= AgCl(s)+ NaNO3(aq )¡÷H£¼0
¡¡ B£®2CH3OH (l) +3O2 (g) = 2CO2 (g) + 4H2O (l)¡÷H£¼0
¡¡ C£®2FeCl3(aq)+Fe(s) = 3FeCl3(aq)¡¡ ¡÷H £¼ 0
¡¡ D£®2H2 (g) + O2 (g) = 2H2O (l)¡¡ ¡÷H £¼ 0
6£®ÓĂ²¬µç¼«(¶èĐÔ)µç½âÏÂÁĐÈÜ̉ºÊ±£¬̉ơ¼«ºÍÑô¼«ÉϵÄÖ÷̉ª²úÎï·Ö±đÊÇH2ºÍO2µÄÊÇ
A. Ï¡NaOHÈÜ̉º¡¡ B. HCIÈÜ̉º¡¡ C. NaClÈÜ̉º¡¡ D. ËáĐÔAgNO3ÈÜ̉º
5£®ÏÂÁĐ¹ØÓÚÄÜÔ´ºÍ×÷ΪÄÜÔ´µÄÎïÖÊĐđÊö´íÎóµÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡ ¡¡ A£®»¯Ê¯ÄÜÔ´ÎïÖÊÄÚ²¿Ồº×Å´óÁ¿µÄÄÜÁ¿¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡ ¡¡ B£®ẦÉ«Ö²Îï½øĐĐ¹âºÏ×÷ÓĂÊÇ£¬½«̀«ÑôÄÜת»¯Îª»¯Ñ§ÄÜ¡°Öü´æ¡±ÆđÀ´¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡ C£®ÎïÖʵĻ¯Ñ§ÄÜ¿É̉ÔÔÚ²»Í¬µÄ̀ơ¼₫ÏÂתΪÈÈÄÜ¡¢µçÄÜΪÈËÀàÀûÓĂ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡ ¡¡ D£®ÎüÈÈ·´Ó¦Ă»ÓĐÀûÓĂ¼ÛÖµ
4£®ÎªÁ˲ⶨËá¼î·´Ó¦µÄÖĐºÍÈÈ£¬¼ÆËăʱÖÁÉÙĐè̉ªµÄÊư¾ƯÊÇ£º¢ÙËáµÄŨ¶ÈºÍ̀å»ư£»¢Ú
¼îµÄŨ¶ÈºÍ̀å»ư£»¢Û±ÈÈÈÈƯ£»¢Ü·´Ó¦ºóÈÜ̉ºµÄÖÊÁ¿£»¢ƯÉú³ÉË®µÄÎïÖʵÄÁ¿£»¢̃·´Ó¦Ç°ºóζȱ仯£»¢ß²Ù×÷ËùĐèµÄʱ¼ä¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡ A£®¢Ù¢Ú¢Û¢̃¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ B£®¢Ù¢Û¢Ü¢Ư¡¡¡¡ C£®¢Û¢Ü¢Ư¢̃¡¡¡¡ D£®È«²¿
¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com