
题目列表(包括答案和解析)
17(10分)下表是A、B、C、D、E五种有机物的有关信息: www.k@s@5@ 高#考#资#源#网
|
A |
①能使溴的四氯化碳溶液褪色; ②比例模型为  ③能与水在一定条件下反应生成C2H5OH ③能与水在一定条件下反应生成C2H5OH |
|
B |
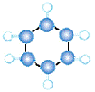 ①由C、H两种元素组成; ①由C、H两种元素组成;②球棍模型为 |
|
C |
①由C、H、O三种元素组成; ②能与Na反应; ③与E反应生成相对分子质量为88的酯 |
|
D |
①相对分子质量比C少2; ②能由C催化氧化得到 |
|
E |
①由C、H、O三种元素组成; ②其水溶液能使紫色石蕊试液变红 |
回答下列问题:
(1)A-E中,属于烃的是 (填字母)。
(2)A能使溴的四氯化碳溶液褪色,发生反应的化学方程式为______________。
(3) C催化氧化生成D的化学方程式为 。
(4) 有机物B具有的性质是 (填序号)。 ①无色无味的液体;②有毒;③不溶于水;④密度比水大;⑤能使酸性KMnO4溶液和溴水褪色
(5)E的水溶液能使紫色石蕊试液变红,说明E的水溶液显酸性,现设计一个实验来比较E与碳酸酸性的强弱,则该实验的原理是
(用化学方程式说明)。
18(10分)已知:A是衡量一个国家石油化工水平高低的重要有机化工原料,E是具有果香味的有机物,F是一种高聚物,可制成多种包装材料。
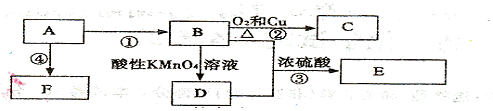
(1)A的结构简式是_______; 完全燃烧1mol的A消耗氧气的物质的量为______.
(2)D分子中的官能团名称是 ,请设计一种实验来验证D物质存在该官能团的方法是 ;
(3)写出反应③的化学方程式 _____.
 19(20分)已知A、B为气体单质,其中一种为黄绿色;D为常见金属单质,C为化合物,它们间有下列转化关系:
19(20分)已知A、B为气体单质,其中一种为黄绿色;D为常见金属单质,C为化合物,它们间有下列转化关系:
 (1)写出下列物质的化学式:A
;C
;
(1)写出下列物质的化学式:A
;C
;
(2)写出C的水溶液与D反应的离子反应方程式_________________________;
(3)F与D反应的离子反应方程式 _______ 。
(4)若对E溶液中的阳离子进行检验:
方法一:用NaOH溶液来检验E溶液中阳离子。①少取 置于试管中;②用胶头滴管取 加入试管中,现象为先产生白色沉淀,后变成灰绿色,最后变成红褐色;③结论:E溶液中含有某种阳离子。
方法二:请你参照“方法一”,用KSCN溶液来检验E溶液中的阳离子:
① ;②向试管中滴入KSCN溶液两滴,无明显现象;③ ___ ,现象为 ;④ 。
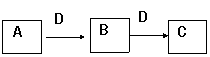 20(12分)在一定条件下进行下列化学反应,请根据以下的转化关系回答下列问题,
20(12分)在一定条件下进行下列化学反应,请根据以下的转化关系回答下列问题,
已知A、B、C中均含有同一种元素,D为非金属单质,能使带有火星的木条复燃。
⑴若A为气体单质,C与水反应所得的溶液呈酸性,则A的结构式为_________,常温常压下C的颜色为_____________。
⑵若A为固体单质,C为淡黄色固体,则C的电子式为____________,C含有的化学键有____________,A与水反应的离子方程式为_______________________.
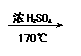 ⑶若A为日常生活中最常见的烃的衍生物,则A与C反应生成一种有水果香味的物质,则B物质的结构简式是_________________________.
⑶若A为日常生活中最常见的烃的衍生物,则A与C反应生成一种有水果香味的物质,则B物质的结构简式是_________________________.
21(12分)实验室制取乙烯的反应原理为 CH3CH2OH CH2 CH2↑+H2O,
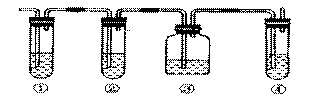 应时,常因温度过高而使乙醇和浓H2SO4反应产生大量的SO2,有人设计了下列实验确认上述混合气体中有乙烯和SO2。
应时,常因温度过高而使乙醇和浓H2SO4反应产生大量的SO2,有人设计了下列实验确认上述混合气体中有乙烯和SO2。
试回答下列问题:
(1)图中①②③④装置中盛放的试剂分别是(填标号):
① ② ③ ④
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性高锰酸钾溶液
(2)能说明SO2存在现象是 ___;
(3)使用装置②的目的是 ___;
(4)使用装置③的目的是 ___;
(5)确证乙烯存在的现象是 ___ 。
16.两种气态烃以任意比混和在105℃时,1L该混和气体与9L的氧气混和,充分燃烧后恢复到原况,所得气体仍是10L,则下列各组混和烃中相符合的是
A.CH4 C2H4 B.CH4 C3H6 C.C2H4 C3H4 D.C2H2 C3H6
15.对实验Ⅰ-Ⅳ的实验现象预测正确的是
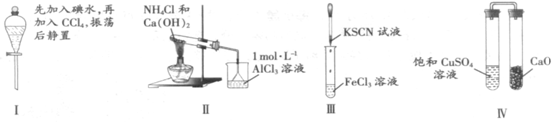
A.实验Ⅰ:液体分层,下层呈无色
B.实验Ⅱ:烧杯中先出现白色沉淀,后溶解
C.实验Ⅲ:试管中溶液颜色变为红色
D.实验Ⅳ:放置一段时间后,饱和CuSO4溶液中出现蓝色晶体
14. 某有机物的结构为 ,这种有机物不可能具有的性质是
A.不能跟NaOH溶液反应 B.能使酸性KMnO4溶液褪色
C.能发生酯化反应 D.能发生水解反应
13.在一定温度下,向aL密闭容器中加入1 mol X气体和2 mol Y气体,发生如下反应:X(g)+2Y(g)  2Z(g)此反应达到平衡的标志是
2Z(g)此反应达到平衡的标志是
A.容器内X、Y、Z的浓度之比为1:2:2 B.容器内各物质的浓度不随时间变化
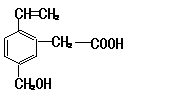 C.单位时间内消耗1molX同时消耗2molZ D.容器内气体密度不随时间变化
C.单位时间内消耗1molX同时消耗2molZ D.容器内气体密度不随时间变化
12.区别SO2与CO2可用的方法是( )
A、品红溶液 B、澄清石灰水 C、紫色石蕊试液 D、BaCl2溶液
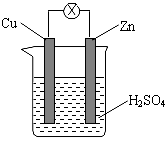
11.如图 甲把锌片和铜片用导线相连后插入稀硫酸溶液构成原电池。某实验兴趣小组做完实验后,在读书卡上的记录如图乙所示,则卡片上的描述合理的是
 卡片号:2009.3
卡片号:2009.3
 实验后的记录:
实验后的记录:
①Cu为负极,Zn为正极
②Cu极上有气泡产生
③SO42-向Cu极移动
④若有0.5mol电子流经导线,则可产生0.25mol气体
 ⑤电子流向是:Cu Zn
⑤电子流向是:Cu Zn
⑥正极反应式:Cu + 2e- = Cu2+
图甲 图乙
A.①②③ B. ②④ C. ④⑤⑥ D.③④⑤
10.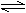 已知 2SO2+O2
2SO3为放热反应,对该反应的下列说法中正确的是( )
已知 2SO2+O2
2SO3为放热反应,对该反应的下列说法中正确的是( )
A.O2的能量一定高于SO2的能量 B.SO2和O2的总能量一定高于SO3的总能量
C.SO2的能量一定高于SO3的能量 D.该反应为放热反应,故不用条件就可发生
9.根据下列反应,判断氧化剂的氧化性强弱顺序为 ( )
H2S + Cl2 = S +2HCl 2NaI + Cl2 = 2NaCl + I2 Na2S + I2 = 2NaI + S
A Cl2>I2>S B Cl2>S>I2 C I2>Cl2>S D S>I2 >Cl2
8、短周期元素X,Y,Z在周期表中的位置如右图所示,则下列说法
中错误的是( )
A.X,Y,Z中X的单质最稳定 B.Y的氢化物为HY
C.X能生成HXO D.能发生Cl2+H2Z = Z+2HCl的反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com