
题目列表(包括答案和解析)
20、(1)① 。
② , ___ _ ;
 (2)
、
;
(2)
、
;
① ;
② 。
19、(1) ;
(2) ;
(3) , 。
18、① ;
② , ,
;
③ ;
④ , 。
17、(1) ;
(2) , ;
(3) ;(4) ;(5) 。
16、(1) ;
(2) , ;
(3) ; (4) , 。
15、(1) , ;
(2) ,
。
21、已知20℃时某些物质的溶解度如下(气体指1atm时1体积水中能溶解的气体体积)
|
物质 |
NaCl |
NaHCO3 |
NH4Cl |
NH3 |
CO2 |
|
溶解度 |
36.0g |
9.6g |
37.2g |
710 |
0.9 |
又知侯氏联合制碱法主要原理:NaCl(饱和)+ NH3 + CO2 + H2O = NaHCO3↓+ NH4Cl
(1)该反应能够成功进行的原因有① ,② ,
③ 。
(2)实际生产中先向饱和食盐水中通入NH3至饱和,再通入CO2气体至反应完全。为什么要先通NH3? 。
(3)20℃时将29.25g食盐投入109mL水中配成溶液,充分进行以上反应后理论上可析出NaHCO3固体 g(精确到0.1g)。
扬州中学高二化学期中试卷答卷纸

20、红矾钠(重铬酸钠:Na2Cr2O7·2H2O)是重要的基本化工原料,在印染工业、电镀工业和皮革工业中有重要用途,在化学工业和制药工业中也用作氧化剂,应用领域十分广泛。
(1)实验室中红矾钠可用铬铁矿(主要成分:FeO·Cr2O3)利用以下过程来制取。
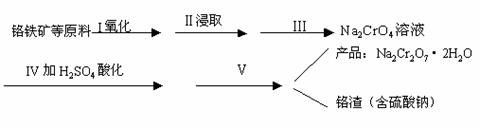
①步骤I中反应的化学方程式为:
4FeO·Cr2O3(s)+8Na2CO3(s)+7O2(g)
 8Na2CrO4(s)+2Fe2O3(s)+8CO2(g)
△H<0
8Na2CrO4(s)+2Fe2O3(s)+8CO2(g)
△H<0
该反应的化学平衡常数的表达式为 。
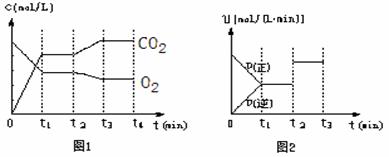
②图1、图2表示该反应在t1时达到平衡、在t2时因改变某个条件而发生变化的曲线:
由图1判断,反应进行至t2 min时,曲线发生变化的原因是 。
由图2判断,t2 min到t3 min 的曲线变化的原因可能是 (填编号)
a.升高温度 b.加了催化剂 c.将原料粉碎 d.缩小容器体积
 (2)步骤Ⅱ中所得溶液显碱性,其中除含有Na2CrO4外还含有铝、硅元素的化合物,它们的化学式可能是
、
。
(2)步骤Ⅱ中所得溶液显碱性,其中除含有Na2CrO4外还含有铝、硅元素的化合物,它们的化学式可能是
、
。
①步骤Ⅲ需将溶液的pH调至7~8并煮沸,其目的是 。
②步骤Ⅳ中发生反应的离子方程式为: 。
19、工业上常以废铜屑(含少量铁、油污)制取胆矾(CuSO4·5H2O),流程如下(已知Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)2]=8.0×10-16,Ksp[Fe(OH)3]=4.0×10-38):
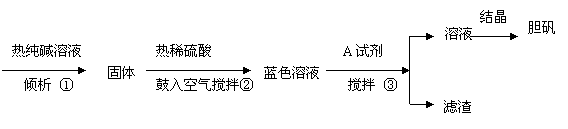
废铜屑
回答:(1)步骤①中纯碱的作用是 。
(2)步骤②中鼓入空气需足量,否则制得的胆矾晶体中会含杂质 。
(3)步骤③中A试剂可以是 ,作用是 。
18、(1)高炉炼铁中发生的基本反应之一为:FeO+CO Fe+CO2 △H>0,其平衡常数可表示为K=c(CO2)/c(CO),已知1373K时K=0.263。
Fe+CO2 △H>0,其平衡常数可表示为K=c(CO2)/c(CO),已知1373K时K=0.263。
①温度升高,化学平衡移动后,平衡常数K值 (填“增大”、“减少”或“不变”)
②1373K时测得高炉中c(CO2)=0.025mol/L,c(CO)=0.1mol/L,在这种情况下,该反应是否处于化学平衡状态 (填“是”或“否”)。此时,化学反应速率ν(正) ν(逆)(填“大于”、“等于”或“小于”),其原因是 。
(2)抽烟对人体有害,烟草不完全燃烧产生的一氧化碳被吸进肺里跟血液中的血红蛋白(用Hb表示)化合,发生下述反应CO+Hb•O2 O2+Hb•CO,实验表明,Hb•CO的浓度即使只有Hb•O2浓度的2%,已足以使人的智力受损,试回答:
O2+Hb•CO,实验表明,Hb•CO的浓度即使只有Hb•O2浓度的2%,已足以使人的智力受损,试回答:
③上述反应的平衡常数表达式为:K= 。
④已知37℃时,平衡常数K=220,抽烟后,测得吸入肺部的空气中的CO和O2的浓度分别为10-6mol/L和10-2mol/L,能否使人的智力受损 (填“能”或“否”),理由是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com