
7.“纳米材料”是指开发研究出的颗粒直径从几纳米至几十纳米的材料,若将“纳米材料”分散到液体分散剂中,所得混合物一定具有的性质是 ( )
A.该分散系属于悬浊液
B.能全部透过半透膜
C.一束光线通过该分散系时,有丁达尔现象
D.通地直流电,会发生电泳
6.在一定条件下,在体积为VL的密闭容器中发生反应:mA+nB pC。t秒末,A减少了1mol, B减少了1.25 mol, C增加了0.5mol。则m:n:p应为 ( )
pC。t秒末,A减少了1mol, B减少了1.25 mol, C增加了0.5mol。则m:n:p应为 ( )
A.4:5:2 B.2:5:4 C.1:3:2 D.3:2:1
5.下列实验操作,正确的是 ( )
①中和滴定时,用标准液润洗滴定管,用待测液润洗锥形瓶,并在锥形瓶内滴入1mL指示剂
②想制一定的物质的量浓度的溶液时,将称量好的溶质溶于盛有适量水的烧杯中,待溶解后立即倾入容量瓶中,继续进行洗涤和定容
③用NaOH溶液和可溶性铝盐溶液大量制取Al(OH)3
④制取Fe(OH)2时,吸取NaOH溶液的胶头滴管的末端应插入FeSO4溶液中,再逐渐注入NaOH溶液
⑤蔗糖加稀硫酸水解后,将水解液滴入银氨溶液,水浴加热后即可见银镜
A.①②③ B.②⑤ C.④ D.以上都不正确
4.已知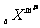 和
和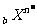 两种离子的电子层结构相同,则a等于 ( )
两种离子的电子层结构相同,则a等于 ( )
A.b+m+n B.b+m-n C.b-m+n D.b-m-n
3.下列气体不会造成大气污染的是 ( )
A.二氧化硫 B.氮气 C.一氧化碳 D.一氧化氮
2.下列说法中,正确的是 ( )
A.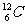 和
和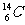 原子的中子数相等 B.纯水在20℃比在90℃时的pH值小
原子的中子数相等 B.纯水在20℃比在90℃时的pH值小
C.钢中碳的质量分数比生铁中的要大 D.次氯酸是一种强氧化剂,是一种弱酸
1.2008年北京奥运会火炬以中国传统祥云符号和纸卷轴为创意,由铝合金制成,使用的燃料为丙烷。下列说法不正确的是 ( )
A.丙烷与甲烷互为同系物 B.丙烷燃烧是吸热反应
C.铝柄有一层致密的氧化膜可防止其腐蚀 D.火炬燃料用丙烷比用煤油更环保
18.汽车内燃机工作时产生的高温会引起N2和O2的反应:N2(g)+O2(g)  2NO(g),是导致汽车尾气中含有NO的原因之一。某同学为控制污染,对该反应进行研究。
2NO(g),是导致汽车尾气中含有NO的原因之一。某同学为控制污染,对该反应进行研究。
(1)下图表示在T1、T2两种不同温度下,一定量的NO发生分解过程中N2的体积分数随时间变化的图像,根据图像判断反应N2(g)+O2(g)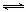 2NO(g)为 (填“吸热”或“放热”)反应。
2NO(g)为 (填“吸热”或“放热”)反应。
(2)2000℃时,向容积为2L的密闭容器中充入10molN2与5mol O2,达到平衡后NO的物质的量为2mol,则2000℃时该反应的平衡常数K= 。该温度下,若开始时向上述容器中充入N2与O2均为1 mol,则达到平衡后N2的转化率为 。
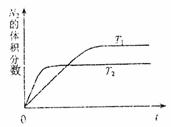
(3)为避免汽车尾气中的有害气体对大气的污染,给汽车安装尾气净化装置。净化装置里装有含Pd等过渡元素的催化剂,气体在催化剂表面吸附与解吸作用的机理如下图所示。
写出上述变化中的总化学反应方程式: 。
17.(1)联氨(N2H4)是一种无色可燃的液体,溶于水显碱性,其原理与氨相似,但其碱性不如氨强,写出其溶于水呈碱性的离子方程式: 。
(2)联氨(N2H4)是航天飞船常用的高能燃料。联氨可以采用尿素[CO(NH2)2]为原料制取,方法是在高锰酸钾催化剂存在下,尿素和次氯酸钠、氢氧化钠溶液反应生成联氨、另外两种盐和水,写出其反应的化学方程式 。
(3)火箭推进器中分别装有联氨和过氧化氢,当它们混合时即产生气体,并放出大量热。
已知:12.8g液态联氨与足量过氧化氢反应生成氮气和水蒸气,放出256.65kJ的热量;H2O(l)+H2O(g) △H=+44kJ·mol-1
2H2O2(l) = 2H2O(l)+O2(g) △H=-196.4kJ·mol-1
则写出表示联氨燃烧热的热化学方程式为 。
16.下图中,A、E、G在常温下为气态非金属单质,B、L为短周期金属单质,D、I分子中均含有10个电子,其中I是一种重要的能源,C是两种常见元素组成的化合物,K是一种由金属氧化物组成的耐高温材料,J是一种非常稀有的矿石,它由三种元素组成,原子个数比为3:1:6,在K电解时J能降低K的熔点。
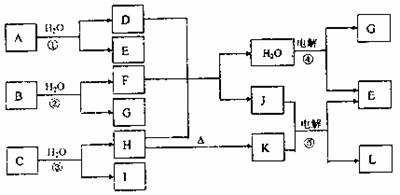
请按要求回答:
(1)在反应①②③中不属于氧化还原反应的是 ;
(2)写出C的化学式 ;
(3)反应④的化学方程式为 ;
(4)反应⑤的阳极反应式为 ;
(5)L可以和某种烃基形成通式为L(CnH2n+1)3的化合物,该物质可以与水发生爆炸式反应,生成H和I,写出CnH2n+1的电子式 ;
(6)若在酒精灯外焰上加热纯L的薄片(厚度为0.1mm),观察到的现象为L的薄片熔化,失去了光泽,熔化的薄片并不滴落;这一现象说明了 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com