
7.存一密闭容器中有CO、H2、O2共16.5g,用电火花弓l燃,使其完全燃烧.再将燃烧后的气体用Na2O2充分吸收,Na2O2增重7.5g,则原混合气体中O2的质量分数是
A.36% B.54.5% C.40% D.33.3%
6.通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可用于估算化学反应的反应热(△H)。化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。
|
化学键 |
H-H |
C1-Cl |
H-Cl |
|
生成1 mol化学键时放的能量 |
436 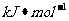 |
243 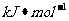 |
431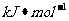 |
则下列热化学方程式不正确
A.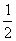 H2(g)+
H2(g)+ 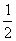 Cl2(g)
Cl2(g) HCl(g);
HCl(g);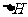 = -91.05
= -91.05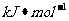
B. H2(g)+
Cl2(g) 2HCl(g);
2HCl(g);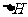 = -183
= -183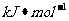
C.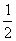 H2(g)+
H2(g)+ 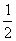 Cl2(g)
Cl2(g) HCl(g);
HCl(g);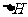 = +91.05
= +91.05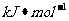
D.2HCl(g) H2(g)+ Cl2(g);
H2(g)+ Cl2(g);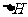 = +183
= +183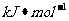
5.甲、乙两种物质的溶解度曲线如下图所示,下列说法一定正确的是
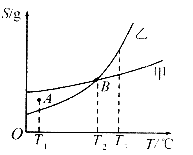
A.A点表示T1℃时甲的溶液已饱和.乙的溶液未饱和
B.B点表示T2℃时甲、乙两物质的溶液均达饱和且两溶液的物质的量浓度相等
C.将T3℃时甲、乙两物质的饱和溶液分别降温至T2℃,析出的乙比析出的甲多
D.若乙中含有少量的甲,可用重结晶的方法提纯乙
4.硝酸铵(NH4NO3)在不同条件下分解可以得到不同的产物。下列各组物质中肯定不可能是硝酸铵分解产物的是
A.N2O、H2O B.N2、O2、H2O
C.N2、HNO3、H2O D.NH3、NO、H2
3.下图中对实验仪器名称的标注或实验操作正确的是

2.八角茴香含有一种抗亚洲禽流感病毒的重要成分--莽草酸,其分子结构为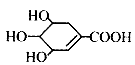 。下列关于莽草酸的说法错误的是
。下列关于莽草酸的说法错误的是
A.分子式为C7H10O5
B.遇FeCl3溶液能呈紫色
C.能使溴水褪色
D.能溶于水
1.由解放军总装备部军事医学研究所研制的小分子团水,解决了医务人员工作时的上厕所难题。新型小分子团水,具有饮用量少、渗透力强、生物利用度高、在人体内储留时间长、排放量少的特点。一次饮用125 mL小分子团水,可维持人体6h正常需水量。下列关于小分子团水的说法正确的是
A.水分子的化学性质改变
B.水分子中氢氧键键长缩短
C.水分子问作用力减小
D.水分子问结构、物理性质改变
22.某结晶水合物含有两种阳离子和一种阴离子。称取两份质量均为1.96g的该结晶水合物,分别制成溶液。一份加入足量Ba(OH)2溶液,生成白色沉淀,随即沉淀变为灰绿色,最后带有红褐色;加热该混合物,逸出能使湿润的红色石蕊试纸变蓝的气体;用稀盐酸处理沉淀物,经洗涤和干燥,得到白色固体2.33 g。另一份加入含0.001 molKMnO4的酸性溶液,MnO4-恰好完全被还原为Mn2+。
请回答以下问题:
(1)该结晶水合物中含有的两种阳离子是 和 ,阴离子是 。
(2)试通过计算确定该结晶水合物的化学式。
21.(10分)室温下,单质A、B、C分别为固体、黄绿色气体与无色气体,在合适条件下,它们可以按下面的流程进行反应。又知E溶液是无色的。请回答:
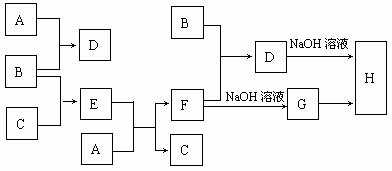
(1)写出下列物质的化学式:
A 、B 、C 。
(2)写出G→H的化学方程式 。
(3)写出B+F→D的离子方程式 。
20.(11分)某钠盐溶液可能含有阴离子NO3-、CO32-、SO32-、SO42-、Cl-、Br-、I-、为鉴别这些离子,分别取少量溶液进行以下实验:
①测得混合液呈碱性;
②加HCl后,生成无色无味气体,该气体能使饱和石灰水溶液变浑浊;
③加CCl4后,滴加少量氯水,振荡后,CCl4后层未变色;
④加BaCl2溶液产生白色沉淀,分离,在沉淀中加入足量盐酸,沉淀不能完全溶解;
⑤加HNO3酸化后,再加过量AgNO3,溶液中析出白色沉淀。
(1)分析上述5个实验,写出每一步实验鉴定离子的结论与理由。
实验① ;
实验② ;
实验③ ;
实验④ ;
实验⑤ ;
(2)上述5个实验不能确定是否存在的离子是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com