
6.下列离子组中,能大量共存且无色透明是 ( )
A.c ( H + ) = 10-14mol · L-1的溶液:Na+、CO32-、S2-、SO42-
B.pH = 0的溶液:Fe2+、NO3-、SO42-、I-
C.强碱性溶液:Mg2+、Ba2+、NO3-、Cl-
D.使紫色石蕊试液变红的溶液:K+、Na+、Ca2+、HCOO-
5.设NA为阿伏加德罗常数,下列叙述不正确的是 ( )
A.5.8g 丙酮所含的共价键为NA
B.标准状况下,22.4L 氮气和氦气所含原子数均为2NA
C.2.9g 的2CaSO· H2O 含有结晶水分子数为0 .0l NA
D.室温下,42g 乙烯与丙烯的混合气体中含碳原子数为3NA
4. X、Y、Z、W 是原子序数依次增大的四种常见元索。W 和Y 元素形成的化合物W3Y4具有磁性。X 的单质在Y2中燃烧可生成XY 和XY2两种气体。Z 的单质是一种金属,该金属在XY2中剧烈燃烧生成黑、白两种固体。下列说法错误的是 ( )
A.W3Y4的化学式为Fe3O4
B.W 在地壳中的含量居第四位
C.XY 和XY2分别是NO 和NO2
D.Z 在XY2中燃烧生成的白色固体是一种氧化物
3.下列有关HF、HCl、HBr、HI 的说法错误的是 ( )
A.均为直线型极性分子 B.熔、沸点依次增大
C.稳定性依次减弱 D.还原性依次增强
2.下列化学用语表达正确的是 ( )
A.碳一12 的原子符号: 127C B.次氯酸的结构式:H一Cl一O
C.Mg原子结构示意图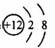 D.乙酸的分子比例模型
D.乙酸的分子比例模型
1.化学与环境、工农业生产等密切相关,下列叙述正确的是 ( )
A.光化学烟雾与大量排放碳氢化合物和氮氧化合物有关
B.将草木灰和硫铵混合施用,肥效更高
C.棉花、蚕丝和锦纶的主要成分都是纤维素
D.为了防止中秋月饼等富脂食品氧化变质,延长保质期,可在包装袋中放人生石灰
23.(8分)在隔绝空气的条件下,某同学将一块部分被氧化的钠块用一张已除去氧化膜、并用针刺一些小孔的铝箔包好,然后放入盛满水且倒置于水槽中的容器内。待钠块反应完全后,在容器中仅收集到1.12 L氢气(标准状况),此时测得铝箔质量比反应前减少了0.27 g,水槽和容器内溶液的总体积为2.0 L,溶液中NaOH的浓度为0.050 mol·L-1(忽略溶液中离子的水解和溶解的氢气的量)。
(1)写出该实验中发生反应的化学方程式。
(2)试通过计算确定该钠块中钠元素的质量分数。
22.(共9分)物质A、D及F的水溶液均呈黄色,D是单质,F的溶液遇苯酚显紫色,A是一种重要工业生产中的主要原料。且A、C、D均含有某一非金属元素,C的相对分子质量与过氧化氢的相对分子质量相等。反应过程中生成的水等与转化无关的物质已经略去。这些物质有以下转化关系。试回答以下问题:
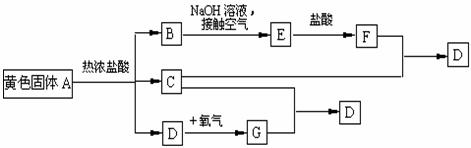
(1)A是 ,C是 ,F是 (均填化学式)。
(2)A与热盐酸反应的离子方程式为 ,
(3)写出该框图中由B→E的化学方程式 ,
。
四:计算题
21.(共8分)
某河道两旁有甲乙两厂.它们排放的工业废水中,共含K+、Ag+、Fe3+、Cl-、OH-、NO3-六种离子。
(1)甲厂的废水中明显呈碱性,故甲厂废水中所含的三种离子是 、 、 。
(2)乙厂的废水中含有另外三种离子是 、 、 。
(3)有一种设想是将甲厂和乙厂的废水按适当的比例混合,可以使废水中的 (填离子符号)转化为沉淀.经过滤后的废水主要含 ,可用来灌溉农田。
20.(共8分)
为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
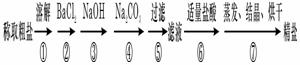
(1)判断BaCl2已过量的方法是 ____ __ 。
(2)第④步中,相关的离子方程式 。
(3)若先用盐酸调pH值再过滤,将对实验结果产生影响,其原因是_______________。
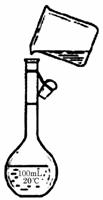
(4)为检验精盐纯度,需配制150 mL.0.2 mol/L NaCl(精盐)溶液,下图是该同学转移溶液的示意图,图中的错误是__________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com