
23.向淀粉溶液中加入少量的稀硫酸,加热使之发生水解,为测定水解程度,需要加入下列试剂中的① NaOH溶液;② 银氨溶液;③ 新制的Cu(OH)2悬浊液;④ 碘水;⑤ BaCl2溶液,组合正确的是
A.①⑤ B.②④ C.①②④ D.②③④
22.把NaOH溶液和CuSO4溶液加入某病人的尿液中,微热时,如果观察到红色沉淀,说明该尿液中含有
A.食醋 B.白酒 C.食盐 D.葡萄糖
21.葡萄糖是一种单糖的主要原因是
A.结构简单
B.不能水解为最简单的糖
C.分子中含羟基和醛基的个数少
D.分子中含碳原子个数少
21. (16分)有如下化学反应:2A(g)+B(g) 2C(g),△H<0。
2C(g),△H<0。
(1)若将4 mol A和2 mol B在2 L的容器中混合,经2 s后测得C的浓度为0.6 mol/L,用物质A表示的平均反应速率为____________________________;2s时物质B的浓度为____________________;
(2)若把a mol A和b mol B充入一密闭容器中,达到平衡时它们的物质的量满足:n(A)+n(B)=n(C),则A的转化率为_________________;
(3)若将4 mol A和2 mol B加入体积可变的等压容器中,一定温度下达到平衡状态,测得气体总物质的量为4.2 mol。此时,混合气体中C的体积分数为_____________;若再通入少量B气体,体系中A的体积分数_________(填“增大”、“减小”或“不变”),若要使A的体积分数再达到与原平衡状态相同,可采取的措施有__ __ 。
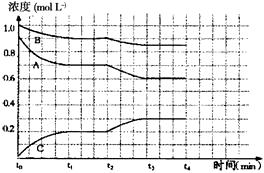
(4)下图是一定条件下该反应过程中,体系内各物质浓度的变化情况。反应处于平衡状态的时间是___________,t2时曲线发生变化的原因是_______________________________ ,若在t4时将B的浓度增大0.l mol·L-1,请在下图中画出各物质浓度的变化情况。
20.(10分)在一个固定体积的密闭容器中,保持一定温度进行以下反应:
Br2(g)+ H2(g) 2HBr(g),已知加入1mol H2和2molBr2时,达到平衡后生成amolHBr(见下表已知项)在相同条件下,且保持平衡时各组分的体积分数不变,对下列编号①-③的状态,填写表中的空白:
2HBr(g),已知加入1mol H2和2molBr2时,达到平衡后生成amolHBr(见下表已知项)在相同条件下,且保持平衡时各组分的体积分数不变,对下列编号①-③的状态,填写表中的空白:
|
已知编号 |
起始状态的物质的量n/mol |
平衡时HBr的物质的量n/mol |
||
|
H2 |
Br2 |
HBr |
|
|
|
1 |
2 |
0 |
a |
|
|
① |
2 |
4 |
0 |
|
|
② |
|
|
1 |
0.5a |
|
③ |
m |
|
g(g≥2m) |
|
19.(14分)在一定温度下,将2molA和2molB两种气体相混合于容积为2L的某密闭容器中,发生如下反应:3A(g)+B(g) xC(g)+2D(g),2min末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:
xC(g)+2D(g),2min末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:
(1)x值等于
(2)A的转化率为
(3)生成D的反应速率为
(4)如果增大反应体系的压强,则平衡体系中C的质量分数 (填“增大”、“减小”、或“不变”)
(5)在此温度下,该化学反应的平衡常数为___________________________
(6)如果上述反应在相同条件下从逆反应开始进行,开始加入C和D各4/3mol,要使平衡时各物质的质量分数与原平衡时完全相等,则还应加入 物质 mol
18.(8分)(1)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式 。若1g水蒸气转化成液态水放热2.444kJ,则反应H2(g)+1/2O2(g)==H2O(l)的△H=___________ kJ/mol。
(2)0.3mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,其热化学方程式是__________________。
又知:H2O(l)==H2O(g);△H= +44 kJ/mol,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时放出的热量是_______________kJ。
17.(4分)在101kPa时,一定量的CO在1.00mol O2中完全燃烧,生成2.00molCO2,放出566.0kJ热量,CO的燃烧热为△H=__________________,表示CO燃烧热的热化学方程式为:______________________________________________________。
16.在某温度下,反应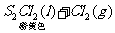

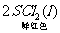 ;ΔH=-5016 kJ/mol,在密闭容器中达到平衡,下列说法错误的是
;ΔH=-5016 kJ/mol,在密闭容器中达到平衡,下列说法错误的是
A.温度不变,增大容器的体积,液体的颜色变浅
B.温度不变,减少容器的体积,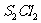 的转化率降低
的转化率降低
C.压强不变,升高温度,液体的颜色变浅
D.体积不变,降低温度,氯气的转化率升高
第II卷(非选择题,共52分)
15.在一个容积为6L的密闭容器中,放入3LX(g)和2LY(g),在一定条件下发生下列反应:4X(g)+3Y(g) 2Q(g)+nR(g),达到平衡后,容器内温度不变,混合气体的压强比原来增加5%,X的浓度减小1/3,则该反应方程式中的n值是
2Q(g)+nR(g),达到平衡后,容器内温度不变,混合气体的压强比原来增加5%,X的浓度减小1/3,则该反应方程式中的n值是
A.6 B.5 C.4 D.3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com