
25.(12分)现有mg某气体,它由四原子分子构成,它的摩尔质量为Mg·mol-1,则:
(1)该气体的物质的量为 mol。
(2)该气体中含有原子总数为 个。
(3)该气体在标准状况下的体积为 L。
(4)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为 。
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为 mol·L-1。
24.(10分)某中学有甲、乙两个探究性学习小组,他们拟用小颗粒状铝硅合金与足量稀硫酸的反应测定通常状况(约20℃,1atm)下气体摩尔体积的方法。
(1)甲组同学拟选用下列实验装置完成实验:
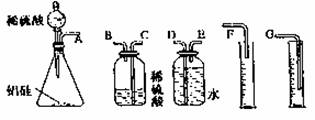
①该组同学必须选用的装置的连接顺序是A接( )( )接 ( )( )接( )(填接口字母,可不填满)。
②实验开始时,先打开分液漏斗上的口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸不能顺利滴入锥形瓶。请你帮助分析原因 。
③实验结束时,该组同学应怎样测量实验中生成氢气的体积? 。
(2)乙组同学仔细分析甲组同学的实验装置后,认为:稀硫酸滴入锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积偏大;实验结果时,连接广口瓶和量筒的导管中有少量水存在,使所测氢气体积偏小。于是他们设计了如图所示的实
验装置。
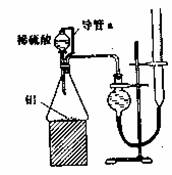
①装置中导管a的作用是
②实验中准确测得4个数据:实验前铝硅合金的质量m1g,实验后残留固体的质量m2g,实验前后碱式滴定管中液面读数分别为V1mL、V2mL。则通常状况时气体摩尔体积Vm= L·mol-1.
23.(10分)A、B、C、D是按原子序数由小到大排列的第二、三周期元素的单质。B、E均为组成空气的成分。F的焰色反应呈黄色。在G中,非金属元素与金属元素的原子个数比为1:2。在一定条件下,各物质之间的相互转化关系如图(图中部分产物未列出):
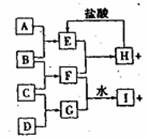
(1)A是 ,C是 。
(2)H与盐酸反应生成E的化学方程式是 。
(3)E与F反应的化学方程式是 。
(4)F与G的水溶液反应生成I和D的离子方程是 。
22.(12分)有一化合物X,其水溶液为浅绿色,可发生如下的转化关系(部分反应物、生成物从略)。其中B、D、E、F均为无色气体,W、K为常见的金属单质,C为难溶于水的红褐色固体。在混合液中加入BaC12溶液可生成不溶于稀盐酸的白色沉淀,H和W可放出大量的热。
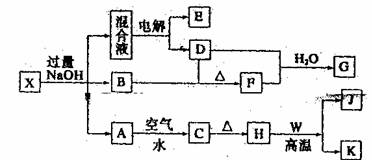
请回答下列问题:
(1)B气体的检验方法为 。
(2)电解混合液时能产生O2的阳极反应式为 。
(3)按要求写出上述转化关系中有关反应的化学方程式:
①含有K元素的化合反应 。
②含有K元素的置换反应 。
(4)K与过量G的稀溶液反应的离子方程式为 。
(5)物质X的化学式为 。
21.(8分)完成下列反应的离子方程式:
(1)向NaHCO3溶液中滴入少量Ca(OH)2溶液: 。
(2)向NaHCO3溶液中滴入过量Ca(OH)2溶液: 。
(3)向10L 0.1mol·L-1的NaHCO3溶液中滴入含有0.5mol Ba(OH)2的溶液: 。
(4)向(3)所得溶液中加入等体积同浓度的Ba(OH)2溶液: 。
20.正在火星上工作的美国“勇气号”“机遇号”近代测车的一个重要任务就是收集有关Fe2O3及硫酸盐的信息,以证明火星上存在或曾经存在过H2O。以下叙述正确的是 ( )
A.铝热剂就是把Fe2O3粉和A1粉的混合物
B.检验红砖中的红色物质是否是Fe2O3的操作步骤为:样品→粉碎→加水溶解→过滤→向滤液中滴加KSCN溶液
C.分别还原a mol Fe2O3所需H2、A1、CO物质的量之比为3:2:3
D.明矾含有结晶水,是混合物
19.在稀硫酸中加入铜粉,铜粉不溶解,再加入不列固体粉末:①FeC12;②Fe2O3;③Zn;④KNO3,铜粉可溶解的是 ( )
A.①② B.②④ C.②③ D.①④
18.某化学兴趣小组欲研究H2SO4、NaC1、KC1、Na2CO3、FeC13、NaOH的性质,对于如何研究,他们设计了两种研究方案
方案①:将它们按照酸、碱、盐分类,然后分别溶于得到溶液,进行实验;
方案②:将它们按照钠盐、钾盐、铁盐和其他化合物分类,然后分别溶于水得到溶液,进行实验。
下列说法正确的是 ( )
A.常温时少量铜粉分别投入上述溶液中,按照方案①的分类,能够完全溶解铜粉的只有酸(H2SO4)溶液和盐(FeC13)溶液
B.设计方案②的同学取某种溶液,在其中加入上述的钾盐溶液,有白色沉淀生成,再加入稀硝酸,沉淀不消失,则该溶液中可能含有Ag
C.按照方案①的分类,属于碱的有Na2CO3、NaOH
D.这两组同学在研究物质时只使用了实验方法、观察法
17.用下图所示方法,检验某固体中是否含有C1。关于溶液①和溶液②,下列说法正确的是 ( )
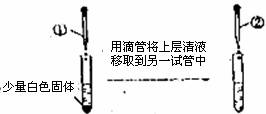
A.①是BaC12溶液,②是稀盐酸
B.①是稀盐酸,②是BaC12溶液
C.①是稀HNO3,②是AgNO3溶液
D.①是稀H2SO4,②是AgNO3溶液
16.设NA为阿伏加德罗常数的数值,下列说法中不正确的是 ( )
A.标准状况下22.4L C12和H2混合气体的原子数为2NA
B.1 mol Na2O2和足量的水完全反应,转移的电子数为NA
C.电解食盐水若产生2g氢气,则转移的电子数目为2NA
D.0.2 mol ·L-1的Ba(OH)2溶液中含 0.4mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com