
13.在标准状况下有22.4L氯气和氢气的混合气体,在一密闭容器中充分反应后,将此气体冷却与1L1 mol/L的NaOH溶液充分反应,最后此溶液 ( )
A.一定显酸性 B.一定显碱性
C.可能显酸性,可能显碱性,可能显中性
D.以上答案均不正确
12.某无色气体可能含HCl、HBr、SO2、CO2中的一种或几种。将该气体通入到适量氯水中,恰好完全反应,不再剩余气体。将所得到的无色溶液分别装在两支试管中,分别加入酸化的AgNO3溶液、酸化的BaCl2溶液,均产生白色沉淀。则下列判断正确的是( )
A.原气体中一定有SO2,一定没有HBr
B.原气体中可能有SO2
C.原气体中一定有HCl
D.不能确定有无HCl和HBr,但一定没有CO2
11.下列叙述正确的是 ( )
A.液态氟化氢中存在氢键,所以其分子比氯化氢更稳定
B.阴离子的核外电子排布一定与上一周期稀有气体原子核外排布相同
C.甲烷、二氧化碳都是非极性分子,因此它们分子的空间结构相同
D.ⅡA某元素离子的核外电子排布一定与上一周期稀有气体原子核外排布相同
10.目前,人类已经发现的非金属元素除稀有气体元素外有16种,下列对这16种非金属元素的判断不正确的是 ( )
①原子的最外层电子数大于3; ②单质在反应中都只能作氧化剂;
③对应的含氧酸都是强酸;④氢化物常温下都是气态,所以又叫气态氢化物。
A.只有①② B.全部 C.只有①②③ D.只有①②④
9.溶质相同、质量分数为a%和b%的两份溶液质量分别为mg、ng,将两份溶液混合并蒸发去xg水,所得溶液的物质的量浓度为cmol/L。欲求溶质的摩尔质量,仍缺少一个数据,该数据是 ( )
A.蒸发后所得溶液的密度(ρ) B.混合前两份溶液的物质的量浓度(c)
C.蒸发前混合液的体积(V) D.溶质的溶解度(S)
8.一定能在指定环境中大量共存的是 ( )
A.c(H+)=1×10-2mol·L-1的溶液:Na+、NH4+、CO32-、SO42-
B.在由水电离出的c(H+)=1×10-12mol/L的溶液中:Fe3+ ClO- Na+ SO42-
C.在pH=1的溶液中:NO3- SO42- Na+ Fe2+
D.含有大量SO42-的溶液:K+、Cu2+、Cl-、NO3-
7. NA代表阿伏加德罗常数的值,下列说法正确的是 ( )
A.标准状况下,11.2L四氯化碳所含分子数为0.5NA
B.pH=2、体积为1L的醋酸溶液中含醋酸分子的数目为0.01NA
C.7.8g Na2O2中阴、阳离子总数为0.4NA
D.4.5g SiO2晶体中含有的硅氧键数目为0.3NA
6.锂和镁在元素周期表中有特殊“对角线”关系,它们的性质相似。下列有关锂及其化合物叙述正确的是 ( )
A.Li2SO4难溶于水 B.Li与N2反应产物是Li3N
C.LiOH易溶于水 D.LiOH与Li2CO3受热都很难分解
5.A和M为两种元素,已知A位于短周期,且A2-与M+的电子数之差为8,则下列说法正确的是 ( )
A.A和M原子的电子总数之和可能为11
B.A和M的原子序数之差为8
C.A和M原子的最外层电子数之和为8
D.A和M原子的最外层电子数之差为7
4.有m1
gKCl饱和溶液,其溶质的质量分数为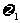 ,改变温度或蒸发水后析出m3
gKCl晶体,母液质量为m2g,其溶质的质量分数为
,改变温度或蒸发水后析出m3
gKCl晶体,母液质量为m2g,其溶质的质量分数为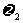 。则下列关系一定正确的是 ( )
。则下列关系一定正确的是 ( )
A.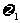 一定大于
一定大于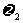 B.m1-m3=m2
B.m1-m3=m2
C.m1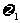 -m2
-m2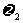 =m3
D.原条件下KCl的溶解度等于100
=m3
D.原条件下KCl的溶解度等于100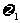 g
g
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com