
8.配合物A是1936年由Jensen合成的,它的化学式为Ni[P(C2H5)3]2Br3。化合物呈顺磁性,有极性,但难溶于水,易溶于苯,其苯溶液不导电,试画出配合物A所有可能的几何异构体。若存在对映体,请标明对映关系。
7.化合物的种类繁多,一个重要的因素是许多化合物存在同分异构现象(isomerism),试画出(Me2PCH2CH2PMe2)2Fe(CO)的所有可能的立体异构体。(Me = CH3)。
|
在结构式中Me2PCH2CH2PMe2可简化成 |
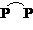 |
(双齿配体) |
6.十九世纪末,化学家发现了镍(Ni)细粉与一氧化碳反应,生成Ni(CO)4。Ni原子的价电子与CO配体提供的电子数等于18--EAN规则(或18电子规则),请回答下列问题:
(1) 用EAN规则预言Fe(0)和Cr(0)的二元羰基化合物的分子式?
(2) 用EAN规则预言最简单的二元铬(o)-亚硝基化合物应具有什么组成?
(3) 解释为什么Mn(0)和Co(0)不生成所谓单核中性羰基化合物,而生成有金属-金属键的化合物?
(4) V(CO)6以及(1)、(2)问中提出的化合物是顺磁性还是反磁性?
(5) 18电子规则对铬和苯合成的化合物也适用,写出此配合物的结构式。
5.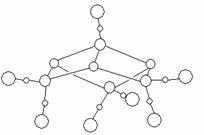 在腌肉时,加入亚硝酸钠,能产生NO,NO与由蛋白质中解离出来的硫和铁结合,生成[Fe4S3(NO)7]-,后者有抑菌,防腐作用。X-射线结构分析表明该离子的结构如下图所示:
在腌肉时,加入亚硝酸钠,能产生NO,NO与由蛋白质中解离出来的硫和铁结合,生成[Fe4S3(NO)7]-,后者有抑菌,防腐作用。X-射线结构分析表明该离子的结构如下图所示:
(1) 请把图上的所有铁原子涂黑,并从上至下用Fe(A)、Fe(B)、Fe(C)、Fe(D)标记。
(2) 已知铁的平均氧化数为0.5,试确定每个Fe的氧化数。
(3) 设在配合物里的每个铁原子都采取sp3杂化,指出每个铁原子中3d电子的数目。
(4) [Fe4S3(NO)7]-离子可以被还原,生成一个含Fe2S2环的化合物,表示为[Fe2S2(NO)4]2-,请回答下列各问题:
(I) 写出阴离子[Fe2S2(NO)4]2-的结构式;
(II) 用阿拉伯数字给出每个铁原子的氧化态;
(III) [Fe2S2(NO)4]2-会转化为[Fe2(SCH3)2(NO)4]n,它是一种致癌物。
下列三种物种中,哪一个被加到S原子上?
( i ) CH3+ , ( ii ) CH3 , ( iii ) CH3- ,n = ?
4.用EAN规则,完成下列各反应,填写下列反应系列中相应化合物的结构式
|
Fe(CO)5 + |
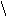 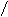  |
 –nCO –nCO |
A |
 –CO –CO |
B |
–H 二聚 二聚 |
C |
3.用EAN规则画出下列各分子的结构式
(1) [HRu(Pph3)3]+ (2) [H3Re3(CO)10]2–
(3) Mo(CO)2(C5H5)4 (4) H4Co4(C5H5)4
(5) [Ni3(CO)2(C5H5)3]+ (6) Re(CH3)2(C5H5)(C5H5CH3)
2.下列各配合物或配离子中,哪些符合EAN规则?哪些不符合EAN规则?
(1) Cr(CO)5 (2) Mn(CO)6 (3) (ph3P)2Fe(CO)3
(4) [Fe(CN)6]4– (5) [Co(NH3)5Cl]+
1.写出下列各配合物或配离子的化学式
(1) 硫酸四氨合铜(II) (2) 二氰合银酸根离子
(3) 二羟基·四水合铝(III)离子 (4) 三氯·(乙烯)合铂(II)酸钾
(5) 四硫氰·二氨合铬(III)酸铵 (6) 顺式-二氯二氨合铂(II)
26.

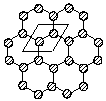 2003年3月日本筑波材料科学国家实验室一个研究小组发现首例带结晶水的晶体在5K下呈现超导性。据报道,该晶体的化学式为 Na0.35CoO2 • 1.3H2O,具有……-CoO2-H2O-Na-H2O-CoO2-H2O-Na-H2O-……层状结构;在以“CoO2”为最简式表示的二维结构中,钴原子和氧原子呈周期性排列,钴原子被4个氧原子包围,Co-O键等长。以 代表氧原子,以 代表钴原子,画出CoO2层的结构,用粗线画出两种二维晶胞。可参考的范例是:石墨的二维晶胞是右图中用粗线围拢的平行四边形。
2003年3月日本筑波材料科学国家实验室一个研究小组发现首例带结晶水的晶体在5K下呈现超导性。据报道,该晶体的化学式为 Na0.35CoO2 • 1.3H2O,具有……-CoO2-H2O-Na-H2O-CoO2-H2O-Na-H2O-……层状结构;在以“CoO2”为最简式表示的二维结构中,钴原子和氧原子呈周期性排列,钴原子被4个氧原子包围,Co-O键等长。以 代表氧原子,以 代表钴原子,画出CoO2层的结构,用粗线画出两种二维晶胞。可参考的范例是:石墨的二维晶胞是右图中用粗线围拢的平行四边形。
25.约三分之二金属晶体采取密堆积结构。每一个原子尽可能地被邻近的金属原子包围。结构中的所有原子在结构上是等同的(identical),可以看作是等径圆球。
(1) 用圆球画出密置的二维模型。在这种模型中,有哪几类空隙?试推出球数与空隙数的比例关系。
(2) 将二维模型改变成三维模型,将出多少种堆积方式?每个原子的配位数多大?
下图的排列称为面心立方(cubic-F):(见图1)
(3) 请在图1上画出密堆积层。
(4) 计算图1的空间利用率,它是简单立方堆积的多少倍?并与简单立方堆积对比。
(5) 画出面心立方密堆积结构中的四面体空隙和八面体空隙。推出球数与空隙数的比例关系。
(6) 试计算当阳离子-阴离子和阴离子-阴离子相互接触时,四面体排列的理想半径比rM / rX。(见图2)
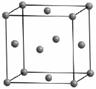
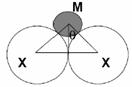
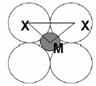
图1 图2 图3
(7) 试计算阳离子-阴离子和阴离子-阴离子相互接触时,八面体排列的理想半径比rM / rX。(见图3)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com