
ЕкЖўПЮЪБ
[в§Шы] ЩЯНкПЮЮвУЧИДЯАСЫдзгНсЙЙЕФжЊЪЖЃЌБОНкПЮЮвУЧИДЯАдкДЫЛљДЁЩЯЙщФЩГіРДЕФдЊЫижмЦкТЩКЭдЊЫижмЦкБэЕФгаЙижЊЪЖЁЃ
[ЬжТл]1ЁЂдЊЫиаджЪЕФжмЦкадБфЛЏЕФЪЕжЪЪЧдЊЫидзгКЫЭтЕчзгХХВМЕФжмЦкадБфЛЏЕФБиШЛНсЙћЁЃ
2ЁЂЫижмЦкТЩжївЊАќРЈФФаЉФкШнЃП
Д№ЃКЫцзХдзгађЪ§ЕФЕндіЃК1ЁЂдзгзюЭтВуЕчзгЪ§гЩ1-2Лђ1-8ГЪжмЦкадБфЛЏЃЛ
21ЁЂЖЬжмЦкдЊЫиXЁЂYЁЂZзщГЩЕФЛЏКЯЮяY2XКЭZX2ЁЃY2XШмгкЫЎаЮГЩЕФШмвКФмгыZX2ЗДгІЩњГЩвЛжжЛЏКЯЮяY2ZX3ЁЃвбжЊШ§жждЊЫидзгЕФжЪзгзмЪ§ЮЊ25ЃЌЧвZКЭXЕФдзгађЪ§жЎКЭБШXЕФдзгађЪ§2БЖЛЙЖр1ЃЌдзгЕФзюЭтВуЕчзгЪ§ЪЧДЮЭтВуЕчзгЪ§ЕФ2БЖЁЃЪдЛиД№ЃК (1)XЁЂYЁЂZдЊЫиЕФУћГЦМАЗћКХЁЃ
(2)аДГіZX2ЕФЛЏбЇЪНЁЃ
(3)Y2XЖдгІЫЎЛЏЮяЕФЕчзгЪНЮЊЁЁЁЁЁЁЁЁЁЁ ЃЌЦфжаДцдкЕФЛЏбЇМќгаЁЁЁЁЁЁЁЁ ЁЃ
(4)аДГіY2XШмгкЫЎЕФШмвКгыZX2ЗДгІЕФЛЏбЇЗНГЬЪНЁЃ
[аЁНс] БОНкПЮЮвУЧИДЯАСЫдзгНсЙЙЃЌдзгКЫЭтЕчзгХХВМЕФЙцТЩМАгыжЎУмЧаЯрЙиЕФвЛаЉИХФюЁЃ
19ЁЂЯТЫЕЗЈВЛе§ШЗЕФЪЧ(D)
A.ЪЙИЩБљЗЂЩњЮяРэБфЛЏашПЫЗўЗЖЕТЛЊСІ
B.ЪЙИЩБљЗЂЩњЛЏбЇБфЛЏжївЊЪЧЦЦЛЕЙВМлМќ
C.ЪЙТШЛЏФЦОЇЬхЗЂЩњЛЏбЇЗДгІашЦЦЛЕРызгМќ
D.ЛЏбЇМќДцдкгкдзгжЎМфЃЌвВДцдкгкЗжзгжЎМф
[змНсгыАхЪщ]

[Р§Ьт]20ЁЂЭЦЖЯЯТСаЮЂСЃЕФУћГЦЃЌВЂгУЕчзгЪНБэЪОЦфаЮГЩЙ§ГЬ
(1)РызгЛЏКЯЮяABЃЌбєРызгБШвѕРызгЖрвЛИіЕчзгВуЃЌ1molABжаКЌ12molЕчзгЃЌдђИУЛЏКЯЮяУћГЦЁЁЁЁ ЁЁЁЁаЮГЩЙ§ГЬЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)гЩЕкШ§жмЦкдЊЫиЕФАыОЖзюДѓЕФбєРызгКЭАыОЖзюаЁЕФвѕРызгаЮГЩЕФЛЏКЯЮяЁЁ ЃЌУћГЦЮЊЁЁЁЁЁЁЁЁ ЃЌаЮГЩЙ§ГЬЁЁЁЁЁЁЁЁ ЁЃ
18ЁЂдкHFЁЂH2OЁЂNH3ЁЂCS2ЁЂCH4ЁЂN2Зжзгжа
ЂйвдЗЧМЋадМќНсКЯЕФЗЧМЋадЗжзгЪЧЁЁ N2ЁЁЁЁ
ЂквдМЋадМќНсКЯЃЌжБЯпаЭНсЙЙЕФЗЧМЖадЗжзгЪЧЁЁЁЁ CS2ЁЁЁЁЁЁ
ЂлвдМЋадМќНсКЯЃЌОпгае§ЫФУцЬхНсЙЙЕФЗЧМЖадЗжзгЪЧЁЁ CH4ЁЁЁЁ
ЂмвдМЋадМќНсКЯЃЌОпгаШ§НЧзЖаЮНсЙЙЕФМЋадЗжзгЪЧЁЁЁЁ NH3ЁЁЁЁЁЁ
ЂнвдМЋадМќНсКЯЃЌОпгаVаЮНсЙЙЕФМЋадЗжзгЪЧЁЁЁЁ H2OЁЁЁЁЁЁ ЁЁ
ЂовдМЋадМќНсКЯЃЌЗжзгМЋадзюДѓЕФЪЧЁЁЁЁЁЁ HFЁЁЁЁЁЁЁЁ
17ЁЂМлЛЏКЯЮяжадЊЫиЛЏКЯМлгае§ИКЕФжївЊдвђЪЧ(C)
AЁЂЕчзггаЕУЪЇЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЁЂЙВгУЕчзгЖдгаЦЋвЦ
CЁЂЕчзгМШгаЕУЪЇгжгаЕчзгЖдЦЋвЦЁЁЁЁЁЁ DЁЂгаН№ЪєдЊЫиЕФДцдк
16ЁЂЯТСаЫЕЗЈжаВЛе§ШЗЕФЪЧ(B)
AЁЂ ЙВМлЛЏКЯЮяжавВПЩФмКЌРызгМќ
BЁЂ ЗЧН№ЪєжЎМфаЮГЩЕФЛЏКЯЮявЛЖЈЪЧЙВМлЛЏКЯЮя
CЁЂ КЌЙВМлМќЕФЛЏКЯЮяВЛвЛЖЈЪЧЛЏКЯЮя
DЁЂКЌРызгМќЕФЛЏКЯЮявЛЖЈЪЧРызгЛЏКЯЮя
15ЁЂРызгМќгыЙВМлМќЕФБШНЯ
|
ЛЏбЇМќ |
ГЩМќЗНЪН |
ГЩМќЮЂСЃ |
ОйР§ |
|
РызгМќ |
ЁЁ |
ЁЁ |
ЁЁ |
|
ЙВМлМќ |
ЁЁ |
ЁЁ |
ЁЁ |
[СЗЯА]
[ЬжТл]1ЁЂзщГЩдзгЕФСЃзггаФФаЉЃПЫќУЧдѕбљЙЙГЩдзгЃП
[АхЪщ]

2ЁЂЬжТлЭъГЩЯТБэЃК
|
Ъєад |
ОіЖЈЮЂСЃ |
гаЙиЕФЙиЯЕЪН |
|
дзгађЪ§ |
жЪзг |
дзгађЪ§=КЫЕчКЩЪ§=жЪзгЪ§ |
|
дЊЫиЕФжжРр |
жЪзг |
ЁЁ |
|
ЭЌвЛдЊЫиЕФВЛЭЌКЫЫи |
жазг |
ЁЁ |
|
дЊЫиЕФЛЏбЇаджЪ |
Ечзг |
ЁЁ |
|
КЫЫиЕФжЪСП |
жЪзгКЭжазг |
жЪСПЪ§=жЪзгЪ§+жазгЪ§ жЪСПЪ§=дзгЕФНќЫЦдзгжЪСПЁЃ |
|
дзгЕФДјЕчСПЁЃ |
жЪзгКЭЕчзг |
жЪзгЪ§=ЕчзгЪ§+ДјЕчКЩЪ§ |
[АхЪщ]1.ЙЙГЩдзгМАдзгКЫИїСЃзгЕФИХФюМАЯрЛЅжЎМфЕФЙиЯЕЃК
(1)дзгађЪ§=КЫЕчКЩЪ§=жЪзгЪ§=КЫЭтЕчзгЪ§(жааддзгЛђЗжзг)
(2)КЫЕчКЩЪ§=жЪзгЪ§=КЫЭтЕчзгзмЪ§+ЫљДјЕчКЩЪ§(дзгЁЂЗжзгЛђРызг)
(3)жЪСПЪ§(A)=жЪзгЪ§(Z)+ жазгЪ§(N)ЁЃ
(4)жЪСПЪ§(A)=ИУдзгЯрЖддзгжЪСПЕФНќЫЦећЪ§жЕЁЃ
[ЙщФЩ]дкЖЬжмЦкдЊЫижаЃЌаэЖрдЊЫиЕФЯрЖддзгжЪСПДѓдМЪЧдзгађЪ§ЕФ2БЖЁЃ
[СЗЯА]3ЁЂФГШ§МлбєРызгЃЌОпга28ИіЕчзгЃЌжЪСПЪ§ЮЊ70ЃЌКЫФкжазгЪ§ЪЧ
AЁЂ28ЁЁЁЁЁЁЁЁЁЁ BЁЂ31ЁЁЁЁЁЁЁЁЁЁ CЁЂ39ЁЁЁЁЁЁЁЁЁЁ DЁЂ42
[Р§Ьт]4ЁЂвбжЊдЊЫиXЁЂYЕФКЫЕчКЩЪ§ЗжБ№ЪЧaКЭbЃЌЫќУЧЕФРызгXm+КЭYn-ЕФКЫЭтЕчзгХХВМЯрЭЌЃЌдђЁЁЁЁЁЁЁЁЁЁЁЁ .
[Р§Ьт]5ЁЂКЫФкжазгЪ§ЮЊNЕФR2+ЃЌжЪСПЪ§ЮЊAЃЌдђЫќЕФngбѕЛЏЮяжаЫљКЌжЪзгЕФЮяжЪЕФСПЪЧ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
[АхЪщ]2.КЫЫигыЭЌЮЛЫиЃЌдЊЫиЕФдзгСПЕШИХФюЕФРэНтМАгаЙиЕФХаЖЯ
[Р§Ьт]6ЁЂ11HЁЂ21HЁЂ31HЁЂH+ЁЂH2ЪЧ(ЁЁ )
A.ЧтЕФЮхжжЭЌЮЛЫиЁЁЁЁЁЁ B.ЮхжжЧтдЊЫиЁЁЁЁЁЁ C.ЧтдЊЫиЕФЮхжжВЛЭЌСЃзгЁЁЁЁ D.ЮхжжКЫЫи
[Р§Ьт]7ЁЂHЁЂDЁЂTЗжБ№ПЩвдЕУЕНЁЁ жжВЛЭЌЕФЧтЗжзгЃЌЦфЛЏбЇЪНКЭЯрЖдЗжзгжЪСПЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
[Р§Ьт]8ЁЂгаЙи3517Cl-СЃзгЃЌЛиД№ЯТСаЮЪЬтЃК
(1)ЁЁЁЁЁЁ КЌжЪзгЪ§ ЁЁ17 ЃЛжазгЪ§ 18ЁЁ ЃЛЕчзгЪ§ЁЁ 18 ЁЁЃЛжЪСПЪ§ 35ЁЁ ЁЃ
(2)ЁЁЁЁЁЁ ИУСЃзгЕФНсЙЙЪОвтЭМЁЁ (Тд)ЁЁЁЁ ЃКЕчзгЪНЁЁ (Тд) ЁЃ
(3)ЁЁЁЁЁЁ Ыќгы3517ClЁЂ3717ClжЎМфЕФЙиЯЕЪЧ ЫќгыЪЧ3517ClЭЌжждзгЃЛгы3717ClЛЅЮЊЭЌЮЛЫиЁЃЃЛ
(4)ЁЁЁЁЁЁ Ыќгы3517ClЕФАыОЖДѓаЁЕФЙиЯЕЪЧ ЧАепДѓгкКѓепЁЁ .
(5)ЁЁЁЁЁЁ вбжЊClдЊЫиЕФЯрЖддзгжЪСПЮЊ35.5ЃЌПЩжЊдзгдкздШЛНчЕФдзгжЪСПЗжЪ§жЎБШЮЊЁЁ 3ЃК1 ЁЃ
[Р§Ьт]9ЁЂЩшФГдЊЫиФГдзгКЫФкЕФжЪзгЪ§ЮЊmЃЌжазгЪ§ЮЊnЃЌдђЯТЪіТлЖЯе§ШЗЕФЪЧ(ЁЁ )
AЃЎВЛФмгЩДЫШЗЖЈИУдЊЫиЕФЯрЖддзгжЪСП
BЃЎетжждЊЫиЕФЯрЖддгкжЪСПЮЊm+n
CЃЎШєЬМдгкжЪСПЮЊWgЃЌДЫдзгЕФжЪСПЮЊ(m+n)WgЃЛ
DЃЎКЫФкжазгЕФзмжЪСПаЁгкжЪзгЕФзмжЪСП.
[Р§Ьт]10ЁЂвбжЊЃЌФГдЊЫиЕФвЛжжКЫЫиЕФnИідзгЕФжЪСПЮЊWgЃЌЦфФІЖћжЪСПЮЊM g/molЃЛдђТШдЊЫиЕФвЛжжКЫЫи35ClЕФвЛИідзгЕФжЪСПЪЧЁЁЁЁЁЁЁЁ ЁЃ
[Й§ЖЩ]дЊЫиЕФаджЪгыдЊЫидзгЕФКЫЭтЕчзгХХВМУмЧаЯрЙиЁЃвђДЫЃЌСЫНтдЊЫидзгКЫЭтЕчзгХХВМЕФЙцТЩЪЧбЇЯАЛЏбЇБиаыЕФЁЃ
[ЙщФЩ]дзгКЫЭтЕчзгХХВМЕФвЛАуЙцТЩгаФЧаЉЃП

[АхЪщ]3.КЫЭтЕчзгХХВМЙцТЩМАНсЙЙЪОвтЭМЃК
[СЗЯА]11ЁЂЗжВуХХВМЙцТЩЃКЁАвЛЕЭЫФВЛГЌЁБЕФФкШнЪЧЁЁЁЁЁЁЁЁ ЃЌЁЁЁЁЁЁЁЁЁЁ ЃЌ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
[Р§Ьт]12ЁЂЯТСаЫЕЗЈЛђЗћКХжаЃЌе§ШЗЕФЪЧЃКЂйдзгЕФЕчзгдЦЭМжаЃЌаЁКкЕуЕФЪшУмБэЪОЕчзгЪ§ЕФЖрЩйЃЛЂкNЕФдзгНсЙЙЪОвтЭМЮЊ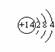 ЃЛЂлШЮКЮдЊЫиЕФдзгЖМгЩжЪзгЁЂжазгКЭКЫЭтЕчзгЙЙГЩЕФЃЛЂмН№ЪєдЊЫиЕФЕчзгЪ§вЛАуЩйгк4ИіЃЛЂнОпгаЯржЪзгЪ§ЕФСЃзгЪєгкЭЌвЛжждЊЫиЃЛЂоыЎдзгНсЙЙЪОвтЭМЮЊ
ЃЛЂлШЮКЮдЊЫиЕФдзгЖМгЩжЪзгЁЂжазгКЭКЫЭтЕчзгЙЙГЩЕФЃЛЂмН№ЪєдЊЫиЕФЕчзгЪ§вЛАуЩйгк4ИіЃЛЂнОпгаЯржЪзгЪ§ЕФСЃзгЪєгкЭЌвЛжждЊЫиЃЛЂоыЎдзгНсЙЙЪОвтЭМЮЊ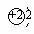 ЃЛЂпФГAдзгКЫФкжЪзгЪ§гыжазгЪ§ЯрЕШЃЌдђдЊЫиЕФЯрЖддзгжЪСПЪЧжЪзгЪ§ЕФ2БЖЁЃ(ЁЁЁЁ )
ЃЛЂпФГAдзгКЫФкжЪзгЪ§гыжазгЪ§ЯрЕШЃЌдђдЊЫиЕФЯрЖддзгжЪСПЪЧжЪзгЪ§ЕФ2БЖЁЃ(ЁЁЁЁ )
A.жЛгаЂйЂкЂмЂпЁЁЁЁ B.жЛгаЂмЂпЁЁЁЁЁЁЁЁЁЁ C.ШЋВПе§ШЗЁЁЁЁЁЁЁЁЁЁ D.ШЋВПДэЮѓ
[СЗЯА]13ЁЂФГдЊЫидзгЕФКЫЭтЕчзгЪ§ЪЧЕчзгВуЪ§ЕФ5БЖЃЌЦфжЪзгЪ§ЪЧзюЭтВуЕчзгЪ§ЕФ3БЖЃЌИУдЊЫиЕФдзгНсЙЙЪОвтЭМЪЧЁЃ
[НВНт]гЩгкдЊЫидзгЕФзюЭтВуЩЯЕФЕчзгЪ§гыдЊЫиЕФЛЏбЇаджЪУмЧаЯрЙиЃЌЫљвдЮЊСЫМђБуЦ№МћЃЌЮвУЧв§ШыСЫЕчзгЪНЕФИХФюЁЃдзгЁЂРызгЕФЖМПЩвдгУНсЙЙМђЭМКЭЕчзгЪНРДБэЪОЁЃЕчзгЪНЛЙПЩвдгУгкБэЪОЛЏКЯЮяЕФаЮГЩЙ§ГЬЁЃ
[Й§ЖЩ]дзгдкВЮМгЛЏбЇЗДгІЪБЃЌЖМгаЪЙздМКЕФзюЭтВуЕчзгаЮГЩЮШЖЈНсЙЙЕФЧуЯђЃЌдзгКЭдзгЯргіЗЂЩњЗДгІЪБЃЌБиаЮГЩЛЏбЇМќЁЃ
[АхЪщ]ЖўЁЂЛЏбЇМќ
[ЬжТл]14ЁЂдзгКЭдзгЭЈГЃЭЈЙ§ЪВУДЗНЪНЪЙздМКЧїЯђгкЮШЖЈНсЙЙФиЃПаЮГЩдѕбљЕФЛЏбЇМќЃП
39. (60Зж)
(1)ЕиЪЦЕЭЦНЃЛЮТДјКЃбѓадЦјКђЃЌЕиДІЮїЗчДјЃЌШЋФъЪЂааЮїЗчЁЃ(8Зж)
(2)ГЪВЈЖЏ(2Зж)ЩЯЩ§ЧїЪЦЁЃ(2Зж)
(3)КгКўВЙИјМѕЩйЃЛ(2Зж)ЪЊЕиКЭВнГЁЭЫЛЏЃЌЩњЮяЖрбљадМѕЩйЃЛ(2Зж)МгОчСЫИЩКЕЕШЦјЯѓджКІЁЂЩњЮя(ВЁГцКІЁЂЪѓКІ)джКІЃЛ(2Зж)ЃЛЛФФЎЛЏУцЛ§МгДѓЃЌЩњЬЌЛЗОГНјвЛВНЖёЛЏ(2Зж)ЕШЁЃ
(4)ЧїЯђЃКгЩЗЂДяЙњМвзЊЯђЗЂеЙжаЙњМвЁЃ(3Зж)двђЃКЗЂДяЙњМвРЉДѓКЭЭиеЙаТЕФЪаГЁЃЛНЕЕЭЩњВњГЩБОЃЌНЋЮлШОНЯДѓЕФЙЄвЕзЊвЦЕНЛЗОГГЩБОНЯЕЭЕФЕиЗНЃЛЮЊСЫГфЗжРћгУЧЈШыЕиЧјСЎМлЕФРЭЖЏСІзЪдДЁЃ(9Зж)
(5)ЙХДњЛЗБЃвтЪЖЧПЕїЖдздШЛзЪдДгаЯоЖШЕФРћгУЃЛЯжДњЛЗБЃвтЪЖЧПЕїПЩГжајЗЂеЙЃЌздШЛзЪдДМШвЊТњзуЕБДњШЫЕФашвЊЃЌгжвЊЮЊзгЫяКѓДњдьИЃЁЃ(8Зж)
(6)ЂйжїЙлФмЖЏадЪЧШЫРрЬигаЕФФмСІКЭЛюЖЏЃЌе§ШЗЗЂЛгжїЙлФмЖЏадФмЭЦЖЏШЫУЧгааЇЕиШЯЪЖКЭИФдьЪРНчЁЃ(3Зж)
ЂкЙцТЩЪЧПЭЙлЕФЃЌЗЂЛгжїЙлФмЖЏадвЊздОѕАДПЭЙлЙцТЩАьЪТЁЃзёбХЉвЕЩњВњЙцТЩЃЌПЦбЇПЙКЕМѕЧсджКІЫ№ЪЇЁЃ(3Зж)
ЂлжїЙлФмЖЏадЕФЗЂЛгЛЙвЊЪмЕНПЭЙлЬѕМўЕФжЦдМЃЌвЊЖдЬѕМўНјааОпЬхЗжЮіЃЌзіЕНЧїРћБмКІЁЃИїЕиРћгУЯжгаЕФПЦММЁЂЮязЪЁЂШЫСІзЪдДЃЌКЯРэзщжЏЃЌвдШЗБЃПЙКЕШЁЕУзюДѓГЩЙћЁЃ(3Зж)
ЂмжїЙлФмЖЏадЕФЗЂЛгашвЊвЛЯЕСаЕФжїЙлвђЫиЁЃУцЖдКЕЧщЃЌеўИЎвЊБОзХЖдШЫУёИКд№ЕФОЋЩёЃЌЪїСЂеНЪЄРЇФбЕФОіаФЃЌЯраХШКжкЁЂвРППШКжкЃЌШЗБЃПЙКЕГЩЙІЁЃ(3Зж)
(7)ЂйИљОнЪЕМЪЧщПіЃЌжЦЖЈе§ШЗЕФПЙКЕМЦЛЎгыеўВпЃЌв§ЕМПЙКЕааЖЏПЦбЇКЯРэНјааЁЃ(2Зж)
ЂкМгЧПзщжЏаЕїЙмРэЃЌДгШЋОжГіЗЂЃЌМгЧПЖЏдБВПЪ№ЃЌЗЂЛгИїЗНУцЕФЛ§МЋадЃЌБЃжЄПЙКЕгаађНјааЁЃ(2Зж)
ЂлЪїСЂЗўЮёвтЪЖЃЌЬсЙЉММЪѕаХЯЂЗўЮёЃЌзщжЏПЦММШЫдБКЭзЈМвжИЕМПЙКЕЃЌПЊеЙХЉвЕПЦММХрбЕЃЌБЃжЄПЙКЕЙЄзїЫГРћНјааЁЃ(2Зж)
ЂмМгЧПМрЖНМьВщЃЌМгЧПЙЄзїЖНЕМЃЌБЃжЄХЉгУЮязЪЕФжЪСПЁЂЪаГЁжШађЕФЮШЖЈвдМАеўВпЕФТфЪЕЁЃ(2Зж)
(зЂЃКЮФПЦзлКЯжїЙлЬтФкШнШчгаЦфЫћБэЪіЃЌбджЎГЩРэЃЌПЩзУЧщИјЗж)
38.(32Зж)
(1)ВФСЯвЛЗДгГГіЮвЙњХЉДхОгУёКЭГЧеђОгУёШЫОљДПЪеШыВЛЖЯдіМгЃЌЦфдіГЄЫйЖШГЪЯжЩЯЩ§ЧїЪЦЁЃЕЋХЉУёЪеШыдіГЄЫйЖШЛКТ§ЃЌВЛМАГЧеђОгУёЪеШыдіГЄПьЁЃ(3Зж)ЫЕУїНќФъЮвЙњГЧЯчШЫУёЩњЛюЫЎЦНЕУЕНЬсИпЃЌЕЋГЧЯчЪеШыВюОрНЯДѓЁЃЭГГяГЧЯчЗЂеЙЪЧЕГКЭЙњМвЕФЕФживЊШЮЮёЁЃ(3Зж)
(2)ЂйвЊМсГжКЭЭъЩЦАДРЭЗжХфЮЊжїЬхЁЂЖржжЗжХфЗНЪНВЂДцЕФЗжХфжЦЖШЃЌМцЙЫаЇТЪгыЙЋЦНЃЌзпЙВЭЌИЛдЃЕФЕРТЗЁЃ(2Зж)
ЂкМгПьЕїећЙњУёЪеШыЗжХфИёОжЃЌж№ВНЬсИпРЭЖЏБЈГъдкГѕДЮЗжХфжаЕФБШжиЁЂОгУёЪеШыдкЙњУёЪеШыЗжХфжаЕФБШжиЃЌЬсИпГЧЯчОгУёЪеШыЃЌЫѕаЁаавЕжЎМфЪеШыВюОрЁЃ(2Зж)
ЂлМгДѓВЦеўЁЂЫАЪедкЙњУёЪеШыГѕДЮЗжХфКЭдйЗжХфжаЕФЕїНкзїгУЃЌМгДѓВЦеўжЇГіСІЖШЃЌвдЫѕаЁЕиЧјВюОрКЭГЧЯчВюОрЁЃ(2Зж)
ЂмНјвЛВНЙцЗЖЪеШыЗжХфжШађЃЌЁАДђЗЧЁЂЕїИпЁЂРЉжаЁЂЬсЕЭЁБЃЌХЄзЊЪеШыВюОрРЉДѓЕФЧїЪЦЁЃ(2Зж)
ЂнНЁШЋЩчЛсБЃеЯЬхЯЕЃЌдкЩњВњЗЂеЙЛљДЁЩЯж№ВНЬсИпБЃеЯЫЎЦНЃЌБЃеЯКУЫћУЧЕФЛљБОЩњЛюКЭЛљБОШЈвцЁЃ(2Зж)
ЦРЗжЫЕУїЃКЕк(2)ЮЪД№ГівдЩЯШЮвт4ЕуПЩИј8ЗжЃЌзюИпЕУЗж8ЗжЁЃ
(3)ЂйЪТЮяЪЧЦеБщСЊЯЕЕФЃЌвЊЙизЂЪТЮяжЎМфПЭЙлДцдкЕФСЊЯЕЁЃзщГЩећЬхЕФВПЗжжЎМфКЯРэгаађзщКЯЃЌЛсЪЙећЬхЙІФмЕУЕНИќКУЗЂЛгЁЃгЩЁАН№зжЫўаЭЁБЕФЗжХфНсЙЙЯђЁАщЯщаЭЁБЪеШыЗжХфНсЙЙзЊБфЃЌЪЕЯжЕиЧјЁЂГЧЯчЁЂаавЕжЎМфЕФКЯРэЗжХфЃЌгажњгкЩчЛсЮШЖЈЁЂОМУЗЂеЙЁЃ(4Зж)
ЂкгЩЁАН№зжЫўаЭЁБЕФЗжХфНсЙЙЯђЁАщЯщаЭЁБЪеШыЗжХфНсЙЙзЊБфЃЌЬхЯжСЫЪТЮязмЬхЪ§СПВЛБфЃЌЕЋФкВПНсЙЙЗЂЩњБфЛЏЃЌвВЛсв§Ц№жЪЕФБфЛЏЃЌЭЈЙ§ЗжХфжЦЖШИФИяЃЌРэЫГЗжХфЙиЯЕЃЌДйНјЩчЛсЙЋЦНЃЌПЩвдДйНјОМУЗЂеЙЁЃ(4Зж)
(4)ЂйжаЙњЙВВњЕГвЊвдШЫЮЊБОЃЌМсГжПЦбЇжДеўЁЂУёжїжДеўЁЂвРЗЈжДеўЃЌЪЙЕГЕФеўВпГфЗжДњБэЙуДѓШЫУёЕФвтжОЃЌБЃеЯШЫУёЕБМвзїжїЁЃ(3Зж)
ЂкМгЧПЩчЛсжївхеўжЮЮФУїНЈЩшЃЌНЈСЂКЭЭъЩЦШЫУёДњБэДѓЛсжЦЖШЃЌЭъЩЦЛљВуУёжїжЦЖШЃЌМсГжУёжїМЏжажЦЃЌБЃеЯЙЋУёгаађВЮМгУёжїбЁОйЁЂУёжїОіВпЁЂУёжїЙмРэЁЂУёжїМрЖНЁЃ(3Зж)
ЂлЙњМвБЃеЯЙЋУёвРЗЈЯэгаЯмЗЈЗЈТЩЙцЖЈЕФИїЯюеўжЮШЈРћКЭздгЩЃЌНЁШЋМрЖНЬхЯЕЃЌШУЙЋУёИвЫЕЛАЃЌЫЕецЛАЁЃ(2Зж)
ДэЮѓЃЁЮДевЕНв§гУдДЁЃЙЋУёвЊгаЗЈжЦвтЪЖЃЌдкЙњМвЗЈТЩеўВпЗЖЮЇФкЃЌЭЈЙ§КЯЗЈКЯРэЧўЕРБэДяздМКРћвцЫпЧѓЃЌдкЪЙздМКЫпЧѓЕУвдЪЕЯжЕФЭЌЪБЮЌЛЄЩчЛсЮШЖЈЁЃ(2Зж)
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com