
17.(12分)有关元素X、Y、Z、W的信息如下:
|
元素 |
信息 |
|
X |
所在主族序数与所在周期序数之差为4 |
|
Y |
最高价氧化物对应的水化物,能电离出电子数相等的阴、阳离子 |
|
Z |
单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏 |
|
W |
基态原子核外5个能级上有电子,且最后的能级上只有1个电子 |
请回答下列问题:
(1)W的单质与Y的最高价氧化物对应的水化物反应的离子方程式为
(2)铜片、碳棒和ZX3溶液组成原电池,写出正极发生的电极反应方程式
(3)向淀粉碘化钾溶液中滴加几滴ZX3的浓溶液,现象为 ,Z3+离子的电子排布式为 ,它有 个未成对电子。
(4)以上述所得WX3溶液为原料制取无水WX3,先制得WX3·6H2O晶体,主要操作包括 ,在 条件下加热WX3·6H2O晶体,能进一步制取无水WX3,其原因是(结合离子方程式简要说明) 。
16.关于下列图示的说法中正确的是A.用图①所示实验可比较硫、碳、硅三种元素的非金属性强弱 ( )
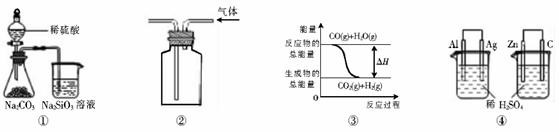
A.用图①所示实验可比较硫、碳、硅三种元素的非金属性强弱
B.用图②所示实验装置排空气法收集CO2气体
C.图③表示可逆反应CO(g)+H2O(g) CO2(g)+H2(g)的△H大于0
D.图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量也相同
第Ⅱ卷 (非选择题 共5 2分)
15.CaCO2溶于盐酸生成CO2,则下列说法中正确的是 ( )
A.该反应的离子方程式为CO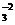 +2H+====CO2↑+H2O
+2H+====CO2↑+H2O
B.与同浓度盐酸反应,块状大理石的反应速率比粉末状的快
C.CaCO2溶于盐酸是因为H+破坏了CaCO2的沉淀溶解平衡,使CaCO3的Ksp增大
D.CaCO2与适量的盐酸恰好完全反应所得溶液中c(H+)=c(OH)+2c(CO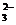 )+
)+
c(HCO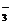 )
)
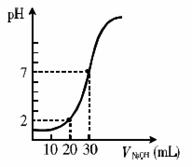
14.右图为室温下20 mL一定物质的量浓度的盐酸,用一定物质的量浓度的NaOH溶液滴定的图示,据图推出盐酸和NaOH溶液的物质的量浓度(mol·L-1)分别是 ( )
|
|
A |
B |
C |
D |
|
c(HCl)(mol·L-1) |
0.06 |
0.04 |
0.03 |
0.09 |
|
c(NaOH)(mol·L-1) |
0.04 |
0.06 |
0.09 |
0.03 |
13.电子层数相同的短周期元素X、Y、Z、W,其中X的最外层电子数比K层少1,Y的最外层电子数比K层多l,Z的单质常用于制造太阳能电池,w的原子半径是同周期中最小的。下列推断中正确的是 ( )
A.Z的氢化物的热稳定性强于w的氢化物
B.z的氧化物与水反应可制得相应的含氧酸
C.X、Y、W的原子半径依次减小,对应的离子半径依次增大
D.X、Y、W的最高价氧化物对应水化物之间互相都能发生反应
12.Li-SO2电池具有输出功率高和低温性能好等特点,其电解质是LiBr,溶剂是碳酸丙
烯酯和乙睛,电池反应为2Li+2SO2 Li2S2O4。下列说法正确的是 ( )
A.该电池反应为可逆反应
B.放电时,Li+向负极移动
C.充电时,阴极反应式为Li++e-===Li
D.该电池的电解质溶液可以换成LiBr的水溶液
11.盖斯定律认为能量总是守恒的,化学反应过程一步完成或分步完成,整个过程的热效应是相同的。
己知:①H2O(g)=====H2O(l) △H1===Q1kJ·mol-1
②C 2H 5OH(g)====C2H 5OH(l) △H2====Q 2 kJ·mol-1
③C 2 H 5 OH(g)+3O2(g)--2CO2(g)+3 H 2 O(g) △H3====Q 3 kJ·mol-1
若使23g液态酒精完全燃烧,最后恢复到室温,则放出的热量为(kJ)
A.Q1+Q2+Q3 B.1.5Q1-0.5Q2+0.5Q3
C.0.5Q1-1.5Q2+0.5Q3 D.0.5(Q1+Q2+Q3)
10.下列关于有机物的说法中,不正确的是 ( )
A.糖类、油脂和蛋白质在一定条件下都能发生水解反应
B.2,5一二甲基己烷的核磁共振氢谱中会出现三组峰
C.甲烷、苯、乙醇和乙酸在一定条件下都能发生取代反应
D.分子式为C5H12的有机物只有三种,它们属于同分异构体
9.下述实验不能达到预期目的的是 ( )
|
编号 |
实验内容 |
实验目的 |
|
A |
将SO2通入酸性KMnO4溶液中 |
证明SO2具有漂白性 |
|
B |
将Cl2通入NaBr溶液中,然后加入CCl4,振荡、静置 |
比较氯与溴的氧化性强弱 |
|
C |
将铜片分别与浓、稀硝酸反应 |
探究浓、稀硝酸氧化性的相对强弱 |
|
D |
向盛有20g蔗糖的烧杯中加入几滴水,搅拌均匀。再加入少许浓硫酸,迅速搅拌。 |
探究浓硫酸的脱水性 |
8.下列溶液中有关物质的量浓度关系和计算不正确的是 ( )
A.pH相等的NaOH、CH3COONa和NaHCO3三种溶液,则有c(NaOH)<c(NaHCO3)
<c(CH3COONa)
B.已知25°C时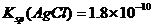 ,则在0.1mol·L-1AlCl3溶液中,Ag+的物质
,则在0.1mol·L-1AlCl3溶液中,Ag+的物质
的量浓度最大可达到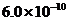 mol·L-1
mol·L-1
C.25°时,0.1mol·L-1Na2CO3溶液中水电离出来的OH-浓度大于0.1mol·L-1NaOH溶
液中水电离出来的OH-浓度
D.室温下,0.1mol·L-1NaHA溶液的pH=4,则有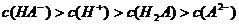
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com