
题目列表(包括答案和解析)
24.(8分) 已知在0.1mol/L的NaHSO3溶液中有关粒子浓度由大到小的顺序为:
c(Na+)>c(HSO3-)>c(SO32-)>c(H2SO3)
(1) 该溶液中c(H+) _________c(OH-)(填“<”、“>”、“=”),
简要说明理由_____________________________________________。
(2) 现向NH4HSO3溶液中,逐滴加入少量含有酚酞的NaOH溶液,可观察到的现象是_________________________,
写出该反应的离子方程式______________________________________________。
23. (12分) 已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测其离子浓度大小顺序有以下几种
①c(Cl-)>c(NH4+)>c(H+)>c(OH-) ②c(Cl-)>c(NH4+)>c(OH-)>c(H+)
③c(NH4+)>c(Cl-)>c(OH-)>c(H+) ④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
则⑴上述关系一定不正确的是 (填序号)
⑵若溶液中只有一种溶质,则该溶质为 ,该溶液中离子浓度的大小关系为 (填序号)
⑶若关系③正确,则溶液中溶质为 。
⑷若四种离子浓度关系有c(NH4+)=c(Cl-),则该溶液显 (填“酸性”、“碱性”、“中性”)。
⑸25℃,pH=a的盐酸VamL与pH=14-a的氨水VbmL混合,若溶液显中性,则Va Vb(填“>”、“<”、“=”、“无法确定”)
22. (9分) 按要求完成下列各小题:
⑴、写出NaHCO3溶液和NaHSO4溶液混合的离子方程式:__________________________________________________
⑵、写出Na2S水解的离子方程:__________________________________________________
⑶、写出Al2(SO4)3溶液和NaHCO3溶液混合的离子方程式:___________________________________________________________
(4) 把AlCl3 溶液蒸干后再灼烧,最后得到的主要固体产物是 ,其理由是(用化学方程式表示,并配以必要的文字说明)_________________________________
21.
(10分)恒温恒容下,将2 mol A气体和2
mol B气体通入体积为2L的密闭容器中发生下列反应:2 A(g)+2
B(g) 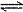 x C(g) + 2 D(s) 2min时反应达到平衡状态,此时剩余1.2mol
B ,并测得C的浓度为1.2 mol/L.
x C(g) + 2 D(s) 2min时反应达到平衡状态,此时剩余1.2mol
B ,并测得C的浓度为1.2 mol/L.
(1) 从开始反应到达到平衡状态,生成C的平均反应速率为________________.
(2) x=____________.
(3) A的准化率与B的转化率之比为________________.
(4) 下列各项中可作为该反应达到平衡标志的是______________(填字母)
A压强不再变化 B气体密度不再变化 C 气体平均相对分子质量不在变化 D A的消耗速率与B的消耗速率之比为2:1
(5) 若向原平衡混合物的容器里再充入2 mol A气体和2 mol B气体,在原温度下达到新的平衡,此时B的物质的量n(B)=________________
20. 把0.1mol/L的醋酸钠溶液20mL和0.1mol/L的盐酸溶液10mL混合后,溶液呈酸性,则混合溶液中粒子浓度关系正确的是( )
A c(CH3COO-)=c(Cl-)>c(H+)>c(CH3COOH)
B c(CH3COO-)+c(Cl-)= c(Na+)+c(H+)
C c(CH3COO-)>c(Cl-)> c(H+)> c(CH3COOH)
D c(CH3COO-)>c(Cl-)> c(CH3COOH)>c(H+)
第Ⅱ卷 (非选择题,共60分)
19. 下列各溶液中,微粒的物质的量浓度关系不正确的是( )
A、0.2mol/L CH3COONa溶液与0.2mol/LCH3COOH等体积混合:
c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
B、c(NH4+)相等的(NH4)2SO4溶液、(NH4)2CO3溶液和NH4Cl溶液:
c(NH4Cl)> c[(NH4)2CO3]>c[(NH4)2SO4]
C、0.1mol/L pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-)
D、在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-)
18. 在一密闭容器中,反应aA(g) 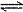 bB(g) 达到平衡后,保持温度不变,将容器的体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则( )
bB(g) 达到平衡后,保持温度不变,将容器的体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则( )
A 平衡向逆反应方向移动了 B 物质A的转化率减少了
C 物质B的质量分数增加了 D a >b
17. 在一定温度下,相同pH的硫酸和硫酸铝溶液中由水电离出来的c(H+)分别是1×10-a moL/L 和1×10-b moL/L ,此温度下,水的离子积常数Kw=( )
A 1×10-2a B 1×10-2b C 1×10-(7+a) D 1×10-(a+b)
16. 有①Na2CO3溶液、②CH3COONa溶液、③NaOH溶液各25mL,物质的量浓度均为0.1moL/L,下列说法中正确的是( )
A 3种溶液pH的大小关系是③>②>①
B 若将三种溶液稀释相同的倍数,pH变化最大的是②
C 若分别加入25mL 0.1moL/L的盐酸后,pH最大的是①
D 若3种溶液的pH均为9,则物质的量浓度大小顺序是③>①>②
15. 已知0.1mol/L的二元酸H2A溶液的pH=4.0,则下列说法中正确的是( )
A 在Na2A、NaHA两溶液中,离子的种类不相同
B 在溶质的物质的量浓度相同的Na2A、NaHA两溶液中,阴离子的数目前者大
C 在NaHA溶液中一定有c(Na+)+c(H+)=c(HA-)+c(A2-)+c(OH-)
D 在Na2A溶液中一定有c(Na+)> c(A2-)> c(H+)> c(OH-)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com