
题目列表(包括答案和解析)
19、(6分)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式 __________________________________________________。若1g水蒸气转化成液态水时放热2.444kJ,则H2的燃烧热△H=_________ kJ·
18、 (11分)某学生欲用已知物质的量浓度的盐酸来滴定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂。请填写下列空白:
(1)用标准的盐酸溶液滴定待测的氢氧化钠溶液时,判断滴定终点的方法为____________ ______________________________________________
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是_______________
 A. 酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
A. 酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B. 滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗
净后没有干燥
C. 酸式滴定管在滴定前有气泡,滴定后气泡消失
D. 读取盐酸体积时,滴定结束时俯视读数
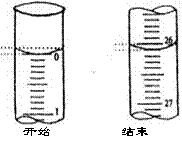
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示:
则起始读数为_________mL,终点读数_____________mL;
(4)某学生根据三次实验分别记录有关数据如下:
|
滴定次数 |
待测氢氧化钠溶液的体积/mL |
0.1000mol/L盐酸的体积(mL) |
||
|
滴定前刻度 |
滴定后刻度 |
溶液体/mL |
||
|
第一次 |
25.00 |
0.00 |
26.11 |
26.11 |
|
第二次 |
25.00 |
1.56 |
30.30 |
28.74 |
|
第三次 |
25.00 |
0.22 |
26.31 |
26.09 |
|
|
17、(8分)(填序号)(1)下列物质能导电的是____________,(2)属于强电解质的是_____________
(3)属于弱电解质的是________________,(4)属于非电解质的是__________________。
①铝片 ②石墨 ③KNO3晶体 ④盐酸 ⑤蔗糖
⑥CO2 ⑦Na2O ⑧冰醋酸 ⑨BaSO4 ⑩氨水
16、将2molA和1molB混合装入容积可变的密闭容器中,发生反应:
2A(s)+bB(g)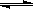 cC(g)
cC(g)
达到化学平衡后,C的物质的量浓度为amol·L-1。若在温度一定的条件下,将密闭容器容积变为原来的1/2后,C的物质的量浓度为2amol·L-1,且始终不变。则b、c关系是( )
A.b+2=c B.b=c C.b+2>c D.b<c
15、体积相同、pH相同的HCl溶液和CH3COOH溶液,与NaOH溶液中和时两者消耗NaOH的物质的量( )。
A. 相同 B. 中和HCl的多 C. 中和CH3COOH的多 D. 无法比较
14、下列叙述正确的是( )
A.95℃纯水的pH<7,说明加热可导致水呈酸性
B.pH=3的醋酸溶液,稀释至10倍后pH=4
C.0.2mol/L的盐酸,与等体积水混合后pH=1
D.由强酸、强碱等物质的量反应得到的溶液pH=7
13、常温下,在水电离出的c(H+)=10-14mol/L的溶液中,一定能大量共存的( )
A.K+、Na+、HCO3-、Cl- B.K+、Br-、AlO2-、Cl-
C.SO42-、Na+、NO3-、Cl- D.SO42-、NH4+、Al3+、Cl-
|
12、下列溶液一定呈中性的是( )
A. PH=7的溶液 B. c(H+)=c(OH-)的溶液
C. 由强酸、强碱等物质的量反应得到的溶液 D. 非电解质溶于水得到的溶液
11、醋酸溶液中存在电离平衡:CH3COOH 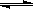 H++CH3COO-,下列叙述不正确的是( )
H++CH3COO-,下列叙述不正确的是( )
A. 醋酸溶液中离子浓度的关系满足:c(H+)=c(OH-)+c(CH3COO-)
B. 0.10mol/L的CH3COOH溶液加水稀释,溶液中c(OH-)减小
C. CH3COOH溶液中加入少量的CH3COONa固体,平衡逆向移动
D. 常温下,pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后,溶液的pH<7
10、为达到预期的实验目的,下列操作正确的是( ) A.用待测液润洗滴定用的锥形瓶 B.中和滴定时右手操作滴定管,左手摇动锥形瓶,眼睛注视滴定管液面的变化 C.用酸式滴定管量取20.00 mL KMnO4溶液 D.为减小中和滴定误差,锥形瓶必须洗净并烘干后才能使用
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com