
题目列表(包括答案和解析)
4.能用分液漏斗分离的两种物质是
A.苯和苯酚 B.溴苯和水 C.乙醇和溴水 D.乙醇和乙酸
2.居室空气污染的主要来源之一是人们使用的装饰材料、胶合板、内墙涂料释放出的一种
刺激性气味的气体,该气体是
A.CH4 B.NH3 C.HCHO D.SO2
 3.下列化学用语表示正确的是
3.下列化学用语表示正确的是
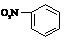
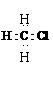 A.乙烯的结构简式:CH2CH2 B.硝基苯的分子式:
A.乙烯的结构简式:CH2CH2 B.硝基苯的分子式:
C.一氯甲烷的电子式: D.乙醇的结构简式:C2H5OH
1.石油价格的波动直接影响第三世界经济发展。下列关于石油的说法正确的是
A.石油属于可再生矿物能源 B.石油主要含有碳、氢两种元素
C.石油的裂化是物理变化 D.石油分馏的各馏分均是纯净物
24.(8分)(8,9,10班学生做)将2molH2O和2molCO置于1L容器中,在一定条件下,加热至高温,发生如下可逆反应:2H2O(g) 2H2+O2 2CO+O2
2H2+O2 2CO+O2 2CO2
2CO2
(1)当上述体系达到平衡时,欲求其混合气体的平衡组成,则至少还需要知道两种气体的平衡浓度,但这两种气体不能同时是__________________和________________,或___________和__________(填它们的化学式)。
(2)若平衡时O2和CO2的物质的量分别为n (O2)平=a mol,n(CO2)平=b mol,试求n(H2O)平=__________(用含a、b的代数式表示)。
24.(8分)90℃时,水的离子积常数KW=1×10-12,在此温度下,将V1mLpH=8的NaOH溶液和V2mLpH=4的H2SO4溶液相混合,所得混合溶液的pH=7,求V1︰V2。
23.(8分)按要求写出298K、101 kPa时下列反应的热化学方程式:
(1)3mol NO2(g)与1 mol H2O(1)反应生成HNO3(aq)和NO(g),放热138kJ:____________。
(2)1 mol HgO(s)分解为液态汞和氧气,吸热90.7kJ:___________________。
(3)①下图是一定量丙烷完全燃烧生成CO2和1 mol H2O(l)过程中的能量变化图,请在附图中的括号内填入“+”或“-”。
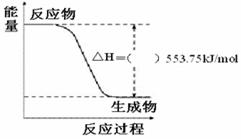
②写出表示丙烷燃烧热的热化学方程式:_______________________________________。
22.(8,9,10班学生做) 由碳的氧化物直接合成乙醇燃料已进入大规模生产。
Ⅰ.目前工业上可以用CO2来生产CH3CH2OH。反应为:2CO2(g)+6H2(g) CH3CH2OH(g)+H2O(g),在一定压强下,该反应的一些实验数据如下表:
CH3CH2OH(g)+H2O(g),在一定压强下,该反应的一些实验数据如下表:
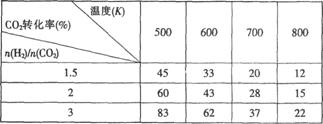
根据表中数据分析:
(1)该反应的正反应是_________(选填“吸热”或“放热”)反应。
(2)提高氢碳比n(H2)/n(CO2),对生成乙醇 _______(选填“不利”、“有利”或“无影响”)。
(3)在体积为1L的恒容密闭容器中,充入1molCO2和3molH2,下列措施中能使c(CH3CH2OH)增大的是_______(填字母,下同)。
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离出来 D.再充入1molCO2和3molH2
Ⅱ.工业上还采取以CO和H2为原料合成乙醇,其化学反应方程式为:
2CO(g)+4H2(g) CH3CH2OH(g)+H2O(g)
CH3CH2OH(g)+H2O(g)
(4)请写出该反应的化学平衡常数表达式K= ___________。
(5)一定温度下,在一个容积可变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是___________。
A.c(CO)=c(H2) B.v正(CO)=v逆(H2O)
C.容器中的压强不变 D.消耗2molCO的同时生成1molCH3CH2OH
(6)在相同条件下,由CO制取CH3CH2OH的平衡常数远远大于由CO2制取CH3CH2OH的平衡常数。则由CO制取CH3CH2OH的优点是______________________,由CO2制取CH3CH2OH的优点是____________。(写出一点即可)
22.(10分)现有浓度均为0.1 mol/L的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸铵、⑦硫酸氢铵,⑧氨水,请回答下列问题:
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)________。
(2)④、⑤、⑥、⑦、⑧五种溶液中NH4+浓度由大到小的顺序是(填序号)_________。
(3)将③和④等体积混合后,混合液中各离子浓度由大到小的顺序是___________。
(4)已知t℃,KW=1×10-13,则t℃(填“>”或“<”或“=”)________25℃。在t℃时将pH=11的NaOH溶液a L与pH=1的H2SO4的溶液b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则a∶b= ___________________。
21.(12分)氯水中存在如下平衡:Cl2 + H2O ⇌ HCl+ HClO。向氯水中加入下列物质,回答各问题:
(1)加入少量CaCO3(s),发生反应的离子方程式表示为__________________,平衡向________移动(填“正向”、“逆向”或“不”,下同),HClO的浓度______(填“增大”、“减小”或“不变”,下同)。
(2)加入少量NaCl(s),平衡向_________移动,HClO的浓度___________。
(3)加入少量NaOH(s),平衡向__________移动,HClO的浓度____________。
(4)加入少量NaBr溶液,发生反应的离子方程式表示为____,HCl的物质的量_____。
(5)加入少量浓品红试液,实验现象为_____________,HCl的物质的量___________。
(6)加蒸馏水稀释,HClO的浓度__________。
20.(6分)在物理和化学中,有些原理、定律具有相似性。如物理中有机械守恒定律,化学中有质量守恒定律。比较它们有助于我们的学习。
(1)1834年,物理学家楞次(1840年-1865年)概括了各种实验结果,得到如下结论:感应电流具有这样的方向,就是感应电流的磁场总要阻碍引起电流的磁通量变化。这就是楞次定律。请写出与楞次定律相似的化学原理或定律:______________________________;
其内容是_______________________________________________________________________
____________________________________________________________________________。
(2)在物理学的匀变速直线运动中常用图来分析速度、时间和位移相当于如图甲中阴影部分所占的面积。

现在容积为2L的密闭容器中进行某一可逆反应: ,其中B物质的正反应速率
,其中B物质的正反应速率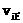 逆反应速率
逆反应速率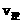 随时间变化的关系如右图乙所示,则图中阴影部分的面积表示的意义为:___________________
随时间变化的关系如右图乙所示,则图中阴影部分的面积表示的意义为:___________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com