
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
23£Æ∏«Àπ∂®¬…‘⁄…˙≤˙∫Õø∆—ß—–æø÷–”–∫‹÷ÿ“™µƒ“‚“°£”––©∑¥”¶µƒ∑¥”¶»»À‰»ªŒfi∑®÷±Ω”≤‚µ√£¨µ´ø…Õ®π˝º‰Ω”µƒ∑Ω∑®£¨”¶”√∏«Àπ∂®¬…≤‚∂®°£œ÷∏˘æ›œ¬¡–3∏ˆ»»ªØ—ß∑¥”¶∑Ω≥Ã Ω£∫
°° Fe2O3(s)+3CO(g)== 2Fe(s)+3CO2(g)°°°°°°°° °˜H£Ω ®D25 kJ/mol
°° 3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g)°°°°°° °˜H£Ω ®D47 kJ/mol
FeO(s)+CO(g)== Fe(s)+CO2(g)°°°°°°°°°°°° °˜H£Ω ®D11 kJ/mol
–¥≥ˆCO∆¯Ãªπ‘≠Fe3O4πÃõ√µΩFeO πÃÃÂ∫ÕCO2∆¯Ãµƒ»»ªØ—ß ∑¥”¶∑Ω≥Ã Ω£∫
∑¥”¶∑Ω≥Ã Ω£∫
_________________°°°°°°°°°°°°
 °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
22. 250C°¢101kPa ±£¨____________¥øŒÔ÷ ÕÍ»´»º…’…˙≥…Œ»∂®µƒªØ∫œŒÔ ±À˘∑≈≥ˆµƒ»»¡ø£¨Ω–◊ˆ∏√ŒÔ÷ µƒ»º…’»»°£
21£Æµ±“ª∏ˆø…ƒÊ∑¥”¶¥ÔµΩ∆Ω∫‚◊¥Ã¨∫Û£¨»Áπ˚∏ƒ±‰______°¢_______°¢______µ»∑¥”¶µƒÃıº˛£¨‘≠¿¥µƒ_______ª·±ª∆∆ªµ,ªØ—ß∆Ω∫‚ª·∑¢…˙“∆∂Ø°£
20. “—÷™œ¬¡–¡Ω ∏ˆ»»ªØ—ß∑Ω≥Ã Ω£∫
∏ˆ»»ªØ—ß∑Ω≥Ã Ω£∫
H2(g)+ 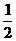 °°O2(g)=H2O(1)£ª °˜H= £≠285£Æ8 kJ°§mol£≠1
°°O2(g)=H2O(1)£ª °˜H= £≠285£Æ8 kJ°§mol£≠1
C3H8(g)+5O2(g)=3CO2(g)+4H2O(1)£ª°˜H= £≠2220 kJ°§mol£≠1
µ—È≤‚µ√H2∫ÕC3H8µƒªÏ∫œ∆¯ÃÂπ≤5 mol£¨ÕÍ»´»º…’ ±∑≈»»3847 kJ£¨‘ÚªÏ∫œ∆¯ÃÂ÷–H2”ÎC3H8µƒÃª˝±» «(°° )°£°°
A£Æ1°√1°°°° B£Æ1°√3°°°° C£Æ3°√1°°°° D£Æ1°√4°°
µ⁄¢ÚæÌ(∑«—°‘Ò °°π≤50∑÷)
19£Æ“—÷™£∫
(l)H2(g)+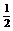 O2(g)=H2O(g)°°°°°°°°°°
°˜H1£Ωa kJ°§
O2(g)=H2O(g)°°°°°°°°°°
°˜H1£Ωa kJ°§ °°
°°
(2)2H2(g)+ O2(g)=2H2O(g)°°°°°°°°
°˜H2£Ωb kJ°§
(3)H2(g)+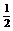 O2(g)=H2O(l)°°°°°°°°°°
°˜H3£Ωc kJ°§
O2(g)=H2O(l)°°°°°°°°°°
°˜H3£Ωc kJ°§ °°
°°
(4)2H2(g)+ O2(g)=2H2O(l)°°  °°°°°°°˜H4£Ωd kJ°§
°°°°°°°˜H4£Ωd kJ°§
œ¬¡–πÿœµ Ω÷–’˝»∑µƒ «°°
A£Æ°° a£ºc £º0°°°°°°°°°°°°°°°° B£Æb£æd£æ0 °°°°°° C£Æ2a£Ωb£º0°°°° °°°°°°°°°° D£Æ2c£Ωd£æ0
18.∏flŒ¬œ¬£¨ƒ≥∑¥”¶¥ÔµΩ∆Ω∫‚£¨∆Ω∫‚≥£ ˝K=°°°°°°°°°°°° °°∫„»› ±£¨Œ¬∂»…˝∏fl£¨H2≈®∂»ºı–°°£œ¬¡–Àµ∑®’˝»∑µƒ «°°°°°°°°°°°°°°°°°° °°°°°°°°°°°°°°°°°°°°
°°A£Æ∏√∑¥”¶µƒÏ ±‰Œ™’˝÷µ°°°°°°°°
B£Æ∫„Œ¬∫„»›œ¬£¨‘ˆ¥Û—π«ø£¨H2≈®∂»“ª∂®ºı–°
|
|
 °°CO2+H2
°°CO2+H217.œ¬¡–πÿ”⁄≈–∂œπ˝≥õƒ∑ΩœÚµƒÀµ∑®’˝»∑µƒ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
°°°°°°°°°°°° A£ÆÀ˘”–◊‘∑¢Ω¯––µƒªØ—ß∑¥”¶∂º «∑≈»»∑¥”¶
°°°°°°°°°°°° B£Æ∏flŒ¬∏fl—πœ¬ø…“‘ π ؃´◊™ªØŒ™Ω∏’ Ø «◊‘∑¢µƒªØ—ß∑¥”¶
°°°°°°°°°°°° C£Æ”…ƒ‹¡ø≈–æ›∫ÕÏÿ≈–æ›◊È∫œ∂¯≥…µƒ∏¥∫œ≈–曣¨Ω´∏¸ ∫œ”⁄À˘”–µƒπ˝≥Ã
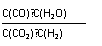 °°°°°°°°°°°°
°°°°°°°°°°°°  D£ÆÕ¨“ªŒÔ÷ µƒπð¢“∫°¢∆¯»˝÷÷◊¥Ã¨µƒÏÿ÷µœ‡Õ¨
D£ÆÕ¨“ªŒÔ÷ µƒπð¢“∫°¢∆¯»˝÷÷◊¥Ã¨µƒÏÿ÷µœ‡Õ¨
16. ∂‘ƒ≥“ªø…ƒÊ∑¥”¶¿¥Àµ, π”√¥flªØº¡µƒ◊˜”√ «°°°°°°°°°°°°°°°°°°°°°°°°°°
°°°°°°°°°°°° A£Æ÷∏fl∑¥”¶ŒÔµƒ∆Ω∫‚◊™ªØ¬ °°°° B£Æ“‘Õ¨—˘≥Ã∂»∏ƒ±‰’˝ƒÊ∑¥”¶µƒÀŸ¬
C£Æ‘ˆ¥Û’˝∑¥”¶ÀŸ¬ £¨ºı–°ƒÊ∑¥”¶ÀŸ¬ °°°° D£Æ∏ƒ±‰∆Ω∫‚ªÏ∫œŒÔµƒ◊È≥…
15. “—÷™£∫(1)Zn(s)+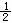 O2(g)=ZnO(s)°° °˜H£Ω£≠348.3kJ°§mol£≠1
O2(g)=ZnO(s)°° °˜H£Ω£≠348.3kJ°§mol£≠1
°° 2Ag(s)+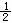 O2(g)=Ag2O(s)°˜H£Ω£≠31.0kJ°§mol£≠1
O2(g)=Ag2O(s)°˜H£Ω£≠31.0kJ°§mol£≠1
°° ‘ÚZn(s)+Ag2O(s)£ΩZnO(s)+2Ag(s)µƒ°˜Hµ»”⁄°°°°°°°°
°° A£Æ£≠317.3kJ°§mol£≠1 B£Æ£≠379.3kJ°§mol£≠1
°° C£Æ£≠332.8kJ°§mol£≠1°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° D£Æ+317.3kJ°§mol£≠1
14.œ¬¡–πÿ”⁄»»ªØ—ß∑¥”¶µƒ√Ë ˆ÷–’˝»∑µƒ «
A£ÆHCl∫ÕNaOH∑¥”¶µƒ÷–∫Õ»»¶§H£Ω£≠57.3kJ/mol£¨‘ÚH2SO4∫ÕCa(OH)2∑¥”¶µƒ÷–∫Õ»»¶§H£Ω2°¡(£≠57.3)kJ/mol
B£ÆCO(g)µƒ»º…’»» «283.0kJ/mol£¨‘Ú2CO2(g) £Ω2CO(g)+O2(g)∑¥”¶µƒ
¶§H£Ω+2°¡283.0kJ/mol
C£Æ–Ë“™º”»»≤≈ƒ‹∑¢…˙µƒ∑¥”¶“ª∂® «Œ¸»»∑¥”¶
D£Æ1molº◊ÕÈ»º…’…˙≥…∆¯Ã¨ÀÆ∫Õ∂˛—ıªØúÀ˘∑≈≥ˆµƒ»»¡ø «º◊Õȵƒ»º…’»»
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒfi÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com