
题目列表(包括答案和解析)
15.下列有关说法正确的是( )
A.Zn(s)+CuSO4(aq)=ZnSO4(aq)+Cu(s);△H=-216KJ·mol,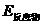 >
>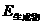
B.SO2(g)=S(s)+O2(g); △H>0,△S<0该反应能自发进行
C.已知热化学方程式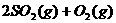
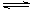 2SO3(g); △H=-QKJ·mol(Q>0)则将2molSO2(g)和1molO2(g)置于一密闭空器中充分反应后放出QKJ热量。
2SO3(g); △H=-QKJ·mol(Q>0)则将2molSO2(g)和1molO2(g)置于一密闭空器中充分反应后放出QKJ热量。
D.1molNaOH分别和1molCH3COOH、1molHNO3反应,后者比前者放出的热量少。
14.在101Kpa和25℃时,有关反应的热化学方程式如下( )
C(s)+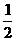 O2(g)=CO(g);△H1=-110.5KJ/mol
O2(g)=CO(g);△H1=-110.5KJ/mol
H2(g)+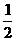 O2(g)=HO(g);△H2=-241.7KJ/mol
O2(g)=HO(g);△H2=-241.7KJ/mol
H(g)+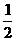 O2(g)=HO(l);△H3=-285.8KJ/mol
O2(g)=HO(l);△H3=-285.8KJ/mol
下列说法正确的( )
A.C(s)+H2O(g)=CO(g)+H2(g) △H=-131.2KJ/mol
B. H2燃烧热的化学方程式为:2H2(g)+O2(g)=2HO(l);△H=-571.6KJ/mol
C.2H2O(g)=2H2(g)+O2(g);△H=-483.4KJ/mol
D.H2O(g)=H2O(l);△H=-44.1KJ/mol
13.已知热化学方程式H2O(g)=H2O(l);△H=-44kJ/mol,C2H2(g)+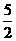 O2(g)=2CO2(g)+H2O(g);
O2(g)=2CO2(g)+H2O(g);
△H=-1256KJ/mol,下列说法正确的是( )
A. 乙炔的燃烧热为1256KJ/mol
B. 若转移10mol电子,则消耗2.5molO2
C. 若生成2mol液态水,则△H=-2512KJ/mol
D.若生成4mol碳氧共用电子对,则放出的热量为2512KJ
12. 右图是反应A2 +B2 2AB
在不同温度和压强下,AB体积分数(AB%)的变化情况,其中a、b 曲线为相同压强、不同温度时的变化情况,c 曲线在保持与b 相同温度时从时间t3
开
2AB
在不同温度和压强下,AB体积分数(AB%)的变化情况,其中a、b 曲线为相同压强、不同温度时的变化情况,c 曲线在保持与b 相同温度时从时间t3
开
始增大压强的情况,则下列叙述正确的是( )

A.A2 、B2 、AB 均为气体,正反应放热
B.AB 为气体,A2 、B2 中最少有一种为非气体,正反应放热
C. AB 为气体,A2 、B2 中最少有一种为非气体,正反应吸热
D.AB 为固体,A2 、B2 中最少有一种为气体,正反应吸热
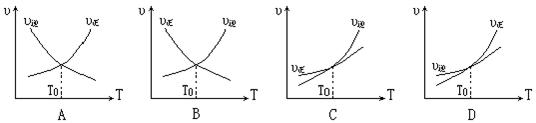
11. 对于可逆反应:CO(g) + NO2(g) 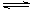 CO2(g) + NO(g);△H<0,T0℃是该反应达到平衡时的温度,当升高温度时,正、逆反应曲线是下图中的( )
CO2(g) + NO(g);△H<0,T0℃是该反应达到平衡时的温度,当升高温度时,正、逆反应曲线是下图中的( )
10. 下列叙述不是可逆反应:A(g)
+ 3B(g)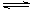 2C(g) 在恒温恒容下反应达到平衡状态标志的是
2C(g) 在恒温恒容下反应达到平衡状态标志的是
( )
①C生成的速率与C分解的速率相等 ②单位时间内生成a mol A,同时生成3a mol B
③A、B、C的浓度不再变化 ④A、B、C的质量分数不再变化
⑤混合气体的总压强不再变化 ⑥混合气体的密度不再变化
⑦混合气体的平均相对分子质量不再变化 ⑧A、B、C的分子数之比为1 : 3 : 2
A.①②⑥ B.②④⑥ C.②⑥⑧ D.③⑦⑧
9. 一定温度下,有可逆反应:2A(g)+2B(g) C(g)+3D(g);ΔH<0。现将2 mol A和2 mol B充入体积为V的甲容器,将2 mol C和6 mol D充入乙容器并使乙容器在反应开始前的体积为2V(如图1)。
C(g)+3D(g);ΔH<0。现将2 mol A和2 mol B充入体积为V的甲容器,将2 mol C和6 mol D充入乙容器并使乙容器在反应开始前的体积为2V(如图1)。
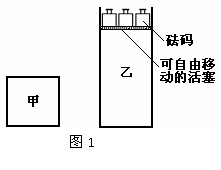
关于两容器中反应的说法正确的是( )
A.甲容器中的反应先达到化学平衡状态
B.两容器中的反应均达平衡时,平衡混合物中各组份的体积百分组成相同,混合气体的平均相对分子质量却不相同
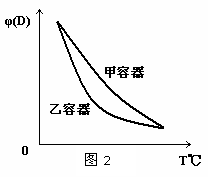
C.两容器达平衡后升高相同的温度,两容器中物质D的体积分数随温度变化如图2 所示
D.在甲容器中再充入2 mol A和2 mol B,平衡后甲中物质C的浓度是乙中物质C的浓度的2倍
8. 在4L密闭容器中充入6molA气体和5molB气体,在一定条件下发生反应:
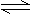 3A(g)+B(g) 2C(g)+xD(g),达到平衡时,生成了2molC,经测定D的浓度
3A(g)+B(g) 2C(g)+xD(g),达到平衡时,生成了2molC,经测定D的浓度
为0.5mol·L-1,下列判断正确的是( )
A.x=1
B.B的转化率为20%
C.平衡时A的浓度为1.50mol·L-1
D.达到平衡时,在相同温度下容器内混合气体的压强是反应前的85%
7. 禽流感是禽流行性感冒的简称,它是一种由甲型流感病毒的一种亚型(也称禽流感病毒)引起的传染性疾病,被国际兽疫局定为甲类传染病。10月25日国家禽流感参考实验室确诊,湘潭县射埠镇湾塘村出现了H5N1亚型高致病性禽流感疫情,在疫区村民家里到处都洒满了石灰,甚至是低矮树木的叶子上都洒上了石灰,很是醒目。根据有关化学知识,判断下列说法不正确的是( )
A.石灰之所以可以杀灭H5N1亚型高致病性禽流感病毒,是由于石灰与水产生的氢氧化钙显碱性,病毒为蛋白质,可以使蛋白质变性,而使病毒失去活性
B.饱和石灰水中加入生石灰,在温度不变的情况下,pH不变
C.饱和石灰水中加入生石灰,在温度不变的情况下,Ca2+的物质的量不变
D.给饱和石灰水溶液升高温度,c(OH-)的浓度降低
6. 下列离子一定能大量共存的是( )
A. 在含大量Fe3+的溶液中:NH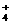 、
、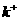 、SO
、SO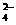 、SCN-
、SCN-
B.在PH=1的溶液中:Na+、Fe2+、C1-、NO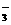
C.在PH=14的溶液中:K+、S2-、SO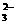 、SO
、SO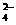
D.水溶液中:Na+、Al3+、CL-、AlO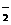
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com