
题目列表(包括答案和解析)
5、电解硫酸溶液时,放出25mL(标况)O2,若以等量的电量在同样条件下电解盐酸溶液,所放出的气体的体积最接近下列数据中的 ( )
A.45mL B.50mL C.75mL D.100mL
4、电解CuCl2和NaCl的混合溶液,最先在阴极和阳极上析出的物质是 ( )
A.H2和Cl2 B. Cu和Cl2 C. H2和O2 D.Cu和O2
3、下列反应达到化学平衡后,加压或降温都能使化学平衡向逆反应方向移动的是 ( )
A.2NO2
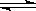 N2O4 △H<0 B.C(S)+CO2
N2O4 △H<0 B.C(S)+CO2 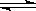 2CO △H>0
2CO △H>0
C.N2+3H2 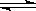 2NH3
△H<0
D.H2S
2NH3
△H<0
D.H2S 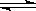 H2+S(s) △H>0
H2+S(s) △H>0
2、某课外活动小组,为研究金属的腐蚀和防护的原理,做了以下实验:将剪下的一块镀锌铁片,放入锥形瓶中,并滴入少量食盐水将其浸湿,再加数滴酚酞试液,按如右图所示的装置进行实验,过一段时间后观察,下列现象不可能出现的是 ( )
A.B中导气管中产生气泡 B.B中导气管里形成一段水柱
C.金属片剪口变红 D.锌被腐蚀
1、下列对化学反应的认识错误的是 ( )
A.会引起化学键的变化 B.会产生新的物质
C.必然引起物质状态的变化 D.必然伴随着能量的变化
25.(10分)在t℃时,在稀硫酸和盐酸混合液中,c(H+)=10-a mol·L-1,c(OH-)=10-b mol·L-1,已知a+b=12。向20 mL该混合酸溶液中逐滴加入pH=11 Ba(OH)2溶液,生成BaSO4的量如图所示,当加入60 mL Ba(OH)2溶液时,C点溶液的pH=6(体积变化忽略不计),试计算:
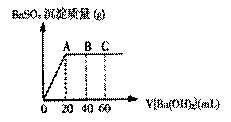
(1)最初混合酸溶液中c(H2SO4)=_______________, c(HCl)=____________;
(2)A点pH=______;
(3)B点比最初混合酸的pH增加多少(写出计算过程)?(1g3=0.48)
24.(12分)某草酸亚铁样品(FeC2O4·xH2O)中含有少量硫酸亚铁。现用滴定法测定该样品中FeC2O4的含量。滴定反应是:
5Fe2++5C2O42-+3MnO4-+24H+==5Fe3+ +10CO2↑+3Mn2++12H2O
实验方案设计为:
 ①将准确称量的a g草酸亚铁样品置于250 mL锥形瓶内,加入适量2 mol/L的H2SO4溶液,使样品溶解,加热至70℃左右,立即用浓度为0.02000 mol/L的高锰酸钾标准溶液滴定至终点,记下滴定管内液面读数为b mL
①将准确称量的a g草酸亚铁样品置于250 mL锥形瓶内,加入适量2 mol/L的H2SO4溶液,使样品溶解,加热至70℃左右,立即用浓度为0.02000 mol/L的高锰酸钾标准溶液滴定至终点,记下滴定管内液面读数为b mL
②向上述滴定混合液中加入适量的Zn粉和过量的2 mol/L的H2SO4溶液,煮沸5-8min,经检验溶液合格后,继续用0.02000 mol/L的高锰酸钾标准溶液滴定至终点,记下滴定管内液面读数为c mL
③ 。
④数据处理。
(提示:锌和Fe3+反应、Fe2+和酸性高锰酸钾反应的方程式为:
(Zn+2Fe3+=Zn2++2Fe2+ 5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O)
请回答下列问题:
(1)上述实验方案中的步骤③是 。
(2)洁净的酸式滴定管在滴定前必须进行的操作是:
Ⅰ.检验活塞是否漏水。
Ⅱ. 。
Ⅲ.加入高锰酸钾标准溶液,赶走尖嘴部位的气泡,调节起始读数。
(3)步骤②中检验溶液是否合格的操作是:取1滴煮沸后的溶液滴入装有
_______ ___溶液的试管中,如 _________ ,则说明溶液合格。
(4)某小组的一次测定数据记录如下:
|
a/g |
起始读数/mL |
b/mL |
c/mL |
|
0.1970 |
0.00 |
31.30 |
42.40 |
根据数据计算0.1970g 样品中:n(Fe2+)= ;
FeC2O4 的质量分数为 (精确到0.01%)
23.(16分)常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表,请回答:
|
实验编号 |
HA物质的量浓度(mol·L-1) |
NaOH物质的量浓度 (mol·L-1) |
混合溶液的pH |
|
甲 |
0.2 |
0.2 |
pH=a |
|
乙 |
c |
0.2 |
pH=7 |
|
丙 |
0.2 |
0.1 |
pH>7 |
|
丁 |
0.1 |
0.1 |
pH=9 |
(1)不考虑其它组的实验结果,单从甲组情况分析,如何用a (混合溶液的pH)来说明HA是强酸还是弱酸_______________________________。
(2)不考虑其它组的实验结果,单从乙组情况分析,C是否一定等于0.2________ (选填“是”或“否”)。混合液中离子浓度c(A-)与 c(Na+)的大小关系是________________。
(3)丙组实验结果分析,HA是________酸(选填“强”或“弱”)。该混合溶液中离子浓度由大到小的顺序是________________________________。
(4)丁组实验所得混合溶液中由水电离出的c(OH-)=________mol·L-1。
写出该混合溶液中下列算式的精确结果(不能做近似计算)。
c(Na+)-c(A-)=________mol·L-1 c(OH-)-c(HA)=________mol·L-1
22.(4分)在纯碱溶液中滴加酚酞,溶液变红。若在该溶液中滴入过量的氯化钡溶液,所观察到的现象是____________ ,
其原因是_________ 。(以离子方程式和简要文字说明)。
21.(8分)有下列物质:(1)金属钠 (2)石墨 (3)食盐晶体 (4)蔗糖 (5)氯化氢
(6)二氧化碳 (7)稀硫酸 (8)盐酸 (9)硫酸钡 (10)乙酸 (11)熔融氯化钠
(1)能导电的有(填序号,下同)__________________________________;
(2)属于非电解质的是_________________________________________;
(3)属于强电解质的是_________________________________________;
(4)属于弱电解质的是_________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com