
题目列表(包括答案和解析)
14. 在下列给定条件的溶液中,一定能大量共存的离子组是
 A.无色溶液:Ca2+、HCO3-、NH4+、AlO2-
A.无色溶液:Ca2+、HCO3-、NH4+、AlO2-
B.能使pH试纸呈红色的溶液:Na+、Fe2+、NO3-、SO42-
C.FeCl2溶液:Fe3+、Na+、SO42-、NO3-
D.加入Mg生成H2的溶液:K+,Na+、H+,NO3-
13. 某离子晶体的晶胞结构如下图所示:则该离子晶体的化学式为
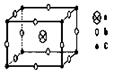 A.abc B.abc3 C.ab2c3 D.ab3c
A.abc B.abc3 C.ab2c3 D.ab3c
12. 在浓盐酸中H3AsO3与SnCl2反应的离子方程式为:3SnCl2+12Cl-+2H3AsO3+
6H+=2As+3SnCl62-+6M 关于该反应的说法中正确的组合是
① 氧化剂是H3AsO3 ; ② 还原性:Cl->As;③ 每生成1molAs,反应中转移电子的物质的量为3mol;④ M为OH-;⑤ SnCl62-是氧化产物。
A.①③⑤ B.①②④⑤ C.①②③④ D.只有①③
11. 已知充分燃烧ag乙炔气体时生成1mol二氧化碳气体和液态水,并放出热量bkJ,则乙炔燃烧的热化学方程式正确的是
A.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(g);ΔH=-4bkJ/mol
B.C2H2(g)+5/2O2(g)=2CO2(g)+H2O(l);ΔH=-2bkJ/mol
C.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l);ΔH=4bkJ/mol
D.2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l);ΔH=2bkJ/mol
10. 根据图示判断下列叙述符合事实的是
|
|
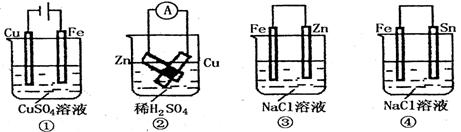
A.按图①连接并放置一段时间后,Fe片表面会“镀”上一层铜
B.按图②连接好导线后(Zn片与Cu片相接触),灵敏电流表会发生非常明显的偏转
C.按图③连接并放置片刻,在Fe片附近加一滴KSCN溶液,溶液变为深红色
D.按图④连接并放置一段时间后,在Sn片上有无色气泡聚集
9. 5.12克铜和一定质量的硝酸反应,当铜消耗完时,共收集到标准状况下的气体3.36升,若把装有这些气体的集气瓶倒立在盛水的水槽中,需通入多少升标准状况下的氧气才能使集气瓶充满溶液。
A. 0.336升 B. 0.224升 C .0.896升 D. 1.12升
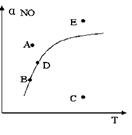
8. 在其它条件一定时,图中曲线表示反应:
2NO(g)
+ O2(g)  2NO2(g)(△H>0)达平衡时NO的转化率与温度的关系,图上标有A、B、C、D、E点,其中表示未达平衡状态且V(正)>V(逆)的点是
2NO2(g)(△H>0)达平衡时NO的转化率与温度的关系,图上标有A、B、C、D、E点,其中表示未达平衡状态且V(正)>V(逆)的点是
A.C点 B.B点 C.A或E D.D点
7. 下列排列顺序正确的是① 热稳定性:H2O>HF>H2S ② 沸点:H2O>HF>HI>HBr>HCl ③ 酸性:H3PO4>H2SO4>HClO4④
结合质子能力:OH->CH3COO->Cl-
下列排列顺序正确的是① 热稳定性:H2O>HF>H2S ② 沸点:H2O>HF>HI>HBr>HCl ③ 酸性:H3PO4>H2SO4>HClO4④
结合质子能力:OH->CH3COO->Cl-
A.①③ B.①④ C.②④ D.②③
5.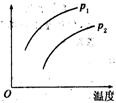 在容积一定的密闭容器中发生可逆反应:A(g)+2B(g)
在容积一定的密闭容器中发生可逆反应:A(g)+2B(g) 2C(g);DH>0.平衡移动关系如右图所示.下列说法正确的是
2C(g);DH>0.平衡移动关系如右图所示.下列说法正确的是
A.P1<P2,纵坐标指A的质量分数
B.P1>P2,纵坐标指C的质量分数
C.P1<P2.纵坐标指A的转化率
D.P1<P2,纵坐标指混合气体的平均摩尔质量
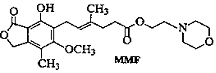 6.霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物。下列关于说法正确的是 A.MMF能溶于水
6.霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物。下列关于说法正确的是 A.MMF能溶于水
B.MMF能发生取代反应和消去反应
C.1molMMF能与6mol氢气发生加成反应
D.1molMMF
能与含3molNaOH的水溶液完全反应
4.实验室用铅蓄电池作电源电解饱和食盐水制取氯气,已知铅蓄电池放电时发生如下反应: 负极: Pb+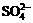 = PbSO4+2e- 正极:PbO2+4H++
= PbSO4+2e- 正极:PbO2+4H++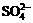 +2e- = PbSO4+2H2O今若制得Cl2 0.050 mol,这时电池内消耗的H2SO4的物质的量至少是
+2e- = PbSO4+2H2O今若制得Cl2 0.050 mol,这时电池内消耗的H2SO4的物质的量至少是
A. 0.025 mol B. 0.050 mol C. 0.10 mol D. 0.20 mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com