
题目列表(包括答案和解析)
2.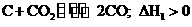 ,,反应速率v1,
,,反应速率v1,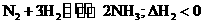 ,反应速率v2。如升温,v1和v2的变化是
,反应速率v2。如升温,v1和v2的变化是
A.同时增大 B.同时减少 C.v1增大,v2减少 D.v1减少,也增大
1.下列对化学反应的认识错误的是
A.会引起化学键的变化 B.会产生新的物质
C.必然引起物质状态的变化 D.必然伴随着能量的变化
23.(6分) 某温度下,在装有催化剂的容积为2 L的密闭容器中,充入SO2和O2各4 mol ,发生反应:2SO2(g) +O2(g)
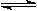 2SO3(g)。充分反应5 min后达到平衡,测得反应容器内混合气体的压强为原来的80 %。求:(本题要求写出计算过程)K^S*5U.C#O%
2SO3(g)。充分反应5 min后达到平衡,测得反应容器内混合气体的压强为原来的80 %。求:(本题要求写出计算过程)K^S*5U.C#O%
(1)SO2的转化率
(2)该反应的平衡常数
 华安、连城、永安、漳平一中,龙海二中,泉港一中”六校联考
华安、连城、永安、漳平一中,龙海二中,泉港一中”六校联考
2010-2011学年上学期第二次月考
22.(8分)工业上由FeS2制H2SO4的转化关系如下:

填写下列空白:
(1)吸收塔中发生反应的化学方程式为 。
(2)接触室内发生的反应为:
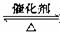 SO2(g)+
SO2(g)+ 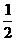 O2(g) SO3(g) △H=
a kJ•mol-1
O2(g) SO3(g) △H=
a kJ•mol-1
下表为不同温度(T)下该反应的化学平衡常数(K):
|
T/K |
673 |
723 |
823 |
923 |
|
K |
423 |
37.4 |
20.5 |
4.68 |
① 根据上表数据及化学平衡理论,上述反应中a 0(填“>”或“<”)。
② K值越大,表明反应达到平衡时 (填标号)。
A.SO2的转化率一定越高 B.SO3的产量一定越大
C.正反应进行得越完全 D.化学反应速率越大
(3)考虑综合经济效益,当炉渣含铁量大于45%时,可用于制硫酸亚铁等。下列利用炉渣里的Fe2O3制FeSO4的方案中,最能体现绿色化学理念的方案是 (填标号)。
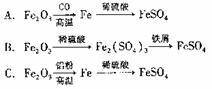
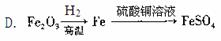
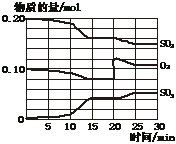
21、 (10分)一定条件下,将SO2和O2充入一密闭容器中,发生如下反应:2SO2(g)+O2(g) 2SO3(g)(正反应放热)反应过程中SO2、O2、SO3物质的量变化如下图所示,回答下列问题:
2SO3(g)(正反应放热)反应过程中SO2、O2、SO3物质的量变化如下图所示,回答下列问题:
(1)降低温度,SO2的转化率_________,化学反应速度_________。
(填“增大”“减小”或“不变”)
(2)反应处于平衡状态的时间是_________。
(3)反应进行至20 min时,曲线发生变化的原因是______________________(用文字表达)。10 min到15 min的曲线变化的原因可能是_________(填写编号)。
a. 加了催化剂 b. 缩小容器体积 c. 降低温度 d. 增加SO3的物质的量
高考 资¥源@网
20.(8分) 已知反应:aA(g)+bB(g) 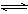 cC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
cC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应为 (填“吸热反应”或“放热反应”),且a+b c(填“>”、“=”或“<”)。
(2)若降低温度,则平衡时B、C的浓度之比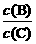 将
(填“增大”、“减小”或“不变”) 。
将
(填“增大”、“减小”或“不变”) 。
(3)若B是有色物质,A、C均无色,维持容器体积不变,加入C至平衡,混合物颜色 ;维持容器内压强不变,充入氖气时,混合物颜色 (填“变深”、“变浅”或“不变”)
18.(4分)某同学为了验证镀锌铁板(俗称白铁)和一块镀锡铁板(俗称马口铁)在不同条件下的腐蚀情况,设计了以下实验:
(1)如果将剪碎的白铁和纯锌,放入稀盐酸中,我们可以看到的现象是:白铁在开始的阶段产生气体的速率要比纯锌的快,一段时间后白铁的速率减小,锌的反应速率增加;这是因为 。
(2)在日常生活中马口铁常被涂以金色故马口铁皮俗称黄金板,用来做罐头的包装;而白铁常用来做水桶、陈放垃圾的簸箕等日常用具,试从金属腐蚀的原理加以解释
。高考 资¥源@网
19,(6分)恒温下,将a mol N2与b mol H2的混合气体通入一个固体容积的密闭容器中,发生如下反应:N2(g)+3H2(g)
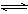 2NH3(g)
2NH3(g)
(1)若反应进行到某时刻t时,nt(N2)=13 mol,nt(NH3)=6 mol, a = 。
(2)反应达到平衡时,混合气体的体积为716.8L(标况下),其中NH3的含量(体积分数)为25%。平衡时NH3的物质的量为 。
(3)原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同),n(始):n(平)= 。
(4)原混合气体中,a:b= 。
(5)达到平衡时,N2和H2的转化率之比,a(N2):a(H2)= 。
(6)平衡混合气体中,n(N2):n(H2):n(NH3)=
17.(10分)在密闭容器中通入a mol H2和b mol I2(g),改变下列条件,反应速率将如何改变?(填写 “加快” ,“减慢 ”或“不变”)
(1)升高温度 ______ ;(2)加入正催化剂 _______ ;(3)体积不变充入更多的H2 ________;
(4)扩大容器的体积 _______; (5)容器体积不变,通入氖气 ________;
16.在一定温度条件下,对于以达到平衡的反应:FeCl3
+3KSCN  3KCl+Fe(SCN)3 ,在此溶液中作如下处理,平衡左移的是:( )
3KCl+Fe(SCN)3 ,在此溶液中作如下处理,平衡左移的是:( )
A.加入少量氯化钾固体 B.加入少量氯化铁固体C.减少Fe(SCN)3的浓度 D.加水稀释
15.在一个密闭、恒容的容器中进行下列反应: 4NH3(g)+5O2(g)
 4NO(g)+6H2O(g)在一定的条件下达到平衡,现向反应容器中通入少量的氯化氢气体,产生的结果是( )
4NO(g)+6H2O(g)在一定的条件下达到平衡,现向反应容器中通入少量的氯化氢气体,产生的结果是( )
A.容器内压强增大 B.原平衡不受影响
C.正反应速率增大 D.NO浓度降低高考 资¥源@网
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com