
题目列表(包括答案和解析)
20. 等体积、等物质的量浓度的硫酸、氢氧化钠溶液分别放在甲、乙两烧杯中,各加等质量的铝,生成氢气的体积比为5:6,则甲、乙两烧杯中的反应情况可能分别是
A.甲、乙中都是铝过量 B.甲中铝过量、乙中碱过量
C.甲中酸过量、乙中铝过量 D.甲中酸过量、乙中碱过量
19. 下列离子方程式书写正确的是
A.铝粉投入到NaOH溶液中:2Al+2OH- = 2AlO2-+H2↑
B.AlCl3溶液中加入足量的氨水:Al3++ 3OH- = Al(OH)3↓
C.三氯化铁溶液中加入铁粉: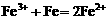
D.FeCl2溶液跟Cl2反应:2Fe2++Cl2=2Fe3++2Cl-
18. 将Fe、Cu、Fe2+、Fe3+和Cu2+盛于同一容器中充分反应,如Fe有剩余,则容器中只能有
A.Cu、Fe3+ B.Fe2+、Fe3+ C.Cu、Cu2+、Fe D.Cu、Fe2+、Fe
17. 将物质的量浓度相同的明矾溶液与Ba(OH)2溶液按体积比为1︰2充分混合,此时铝元素的主要存在形式是
A.Al(OH)3 B.AlO2 - C.Al(OH)3和AlO2- D.Al3+和Al(OH)3
16. 将Na、Mg、Al各0.3mol分别放入100mL 1mol·L-1的盐酸中,同温同压下产生气体的体积比为
A.1︰2︰3 B.6︰3︰2 C.3︰1︰1 D.1︰1︰1
15. 现有下列4种物质:①NaHCO3 ②Al(OH)3 ③(NH4)2CO3 ④Al,其中既能与NaOH溶液反应,又能与盐酸反应,且都有气体生成的一组是
A.①③ B.③④ C.①④  D.②④
D.②④
14. 取两份等量的铝粉,分别与足量的盐酸、浓氢氧化钠溶液反应,在相同状态下产生的气体体积之比是

A.1:1 B.1:2 C. 1:3 D. 3:2
13. 证明溶液中是否有Fe2+,其操作正确的顺序是
①加少许酸化的KMnO4溶液 ②加少许氯水 ③滴加少许KSCN溶液
A.①② B.②③ C.①②③ D.③②
12. 某溶液中含有Na+、Al3+、Cl-、SO42-四种离子,若Na+、Al3+、Cl-的个数之比为3︰2︰1,则溶液中Al3+与SO42-的个数比为
A.3︰4 B.3︰2 C.1︰2 D.1︰4
11.若pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈酸性,其原因可能是
A.生成了一种强酸弱碱盐 B.弱酸溶液和强碱溶液反应
C.一元强酸溶液和强碱溶液反应 D.二元强酸溶液和强碱溶液反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com