
题目列表(包括答案和解析)
4、下列关于能量变化的说法正确的是 ( )
A、“冰,水为之,而寒于水”。说明水和冰相比较,水的能量高
B、化学反应遵循质量守恒的同时,也遵循能量守恒
C、化学反应在物质变化的同时,伴随着能量变化,其表现形式只有吸热和放热两种
D、已知C(石墨,s) === C(金刚石,s ); ΔH>0,则金刚石比石墨稳定
3、下列关于蛋白质的叙述中不正确的是( )
A、蛋白质溶液中加入饱和硫酸铵溶液,蛋白质析出,如再加水也不溶解
B、蛋白质溶液中的蛋白质分子能透过滤纸,但不能透过半透膜
C、重金属盐能使蛋白质变性,可以喝大量的牛奶解毒
D、浓硝酸溅在皮肤上,能使皮肤呈黄色是由于蛋白质和浓HNO3发生颜色反应
2、下列各对物质中,互为同系物的是( )
A、CH3-CH=CH2与 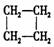 B、
B、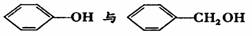
C、HCOOC2H5与CH3COOCH3 D、 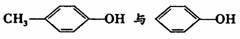
1、下列物质肯定为纯净物的是( )
A、汽油 B、C2H6O C、聚乙烯 D、葡萄糖
27. (12分)下图是元素周期表中的一部分。
(12分)下图是元素周期表中的一部分。
|
|
IA |
|
0 |
|||||
|
1 |
1 H 氢 1.008 |
|
2 He 氦 4.003 |
|||||
|
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|||
|
2 |
3 Li 锂 6.941 |
4 Be 铍 9.012 |
5 B 硼 10.81 |
6 C 碳 12.01 |
7 N 氮 14.01 |
8 O 氧 16.00 |
9 F 氟 19.00 |
10 Ne 氖 20.18 |
|
3 |
11 Na 钠 22.99 |
12 Mg 镁 24.31 |
13 Al 铝 26.98 |
14 Si 硅 28.09 |
15 P 磷 30.97 |
16 S 硫 32.06 |
17 Cl 氯 35.45 |
18 Ar 氩 39.95 |
在元素周期表中,同一周期(横行)中的元素,除0族(最右纵行)元素外,从左到右原子序数依次增多,原子半径逐渐减小,在化学反应中,原子失电子能力逐渐减弱,得电子能力逐渐增强。
请回答:
(1)硅的相对原子质量为 ;原子序数为8的元素位于元素周期表的第 周期,元素符号为 ,它属于 (填“金属”或“非金属”)元素。
(2)原子半径:钠 镁(填“>”或“=”或“<”,下同),原子得电子能力:硫 氯。
淮安五校2010-2011学年度第一学期高二期末
|
|
26.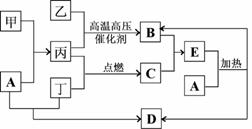 (8分)下列框图所示的物质转化关系中,甲是日常生活中常见的金属,乙、丙、丁是常见的气体单质,且丁为黄绿色气体。气体B与气体C相遇产生大量的白烟,D是海水中浓度最高的盐(部分反应物和生成物及溶剂水已略去)。
(8分)下列框图所示的物质转化关系中,甲是日常生活中常见的金属,乙、丙、丁是常见的气体单质,且丁为黄绿色气体。气体B与气体C相遇产生大量的白烟,D是海水中浓度最高的盐(部分反应物和生成物及溶剂水已略去)。
⑴甲的化学式是 ,
C的化学式 。
⑵写出A溶液和丁反应生成的离子方程式: 。
⑶写出A和E反应的化学方程式: 。
25. (7分)洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
(1)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为: 。
(2)漂白粉的有效成分是(填化学式) 。
(3)漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为 。
(4)反应(1)和反应(3)中,属于氧化还原反应的是(填编号) 。
24. (4分) 用Na2CO3固体配制1mol/L的Na2CO3溶液100mL。
(1)供选用的仪器有:①玻璃棒;②胶头滴管;③100mL量筒;④100mL容量瓶;⑤250mL量筒;⑥天平;⑦50mL烧杯;应选用的仪器有(填编号) 。
(2)应称取Na2CO3的质量为 。
23.从节约原料和防止环境污染因素考虑,用铜制取硝酸铜,方法最佳的是
A.Cu 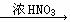 Cu(NO3)2
B.Cu
Cu(NO3)2
B.Cu 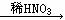 Cu(NO3)2
Cu(NO3)2
C.Cu 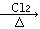 CuCl2
CuCl2 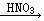 Cu(NO3)2 D.Cu
Cu(NO3)2 D.Cu 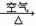 CuO
CuO 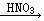 Cu(NO3)2
Cu(NO3)2
22.下列反应中原子利用率达100%的是
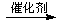

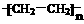 A.制聚乙烯: nCH2=CH2
A.制聚乙烯: nCH2=CH2
B.制CuSO4: Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
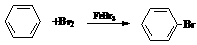
C.制溴苯: +HBr
 D.制乙烯: C4H10
C2H4+C2H6
D.制乙烯: C4H10
C2H4+C2H6
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com