
4.欲将蛋白质溶液和食盐溶液进行分离,并从水中析出蛋白质而又不改变它的性质,
应采用的方法是 ( )
A.先进行渗析,然后加入饱和Na2SO4溶液
B.先进行过滤,然后加入甲醛溶液
C.先进行盐析,然后加入甲醛溶液
D.先进行分液,然后加入饱和Na2SO4溶液
3.CCTV《科技博览》报道:中科院首创用CO2合成可降解塑料聚二氧化碳。下列相
关说法合理的是 ( )
A.聚二氧化碳塑料是通过加聚反应制得的
B.聚二氧化碳塑料与干冰互为同素异形体
C.聚二氧化碳塑料与干冰都是纯净物
D.聚二氧化碳塑料的使用会产生白色污染
2.从某微粒的原子结构示意图可以反映出 ( )
A.质子数和中子数 B.中子数和电子数
C.核电荷数和核外电子层排布的电子数 D.质量数和核外电子层排布的电子数
1.化学与科技、社会、生产密切结合,下列有关说法不正确的是 ( )
A.“乙醇汽油”的广泛使用能有效减少有害气体的排放
B.“无磷洗涤剂”的推广使用,能有效减少水体富营养化的发生
C.“无氟冰箱”取代“含氟冰箱”,对人类的保护伞--臭氧层起到保护作用
D.“绿色化学”可以解决“白色污染”,指用自然界中的天然材料取代所有人工合成材料
24.(9分)(7、9、10班做)有机物A和B的相对分子质量都小于200,完全燃烧时只生成CO2和H2O。B燃烧时消耗的氧气与生成的二氧化碳的物质的量相等。B中碳、氢元素总的质量分数为46.67%。B不发生银镜反应,但跟NaHCO3溶液反应放出CO2。1mol A水解生成1mol苯甲酸和1mol B。A溶液具有酸性,但遇FeCl3溶液不显色。
(1)A与B相对分子质量之差为______________;B分子中应有___________个氧原子。
(2)A的结构简式为_________________________
(3)B与NaHCO3溶液反应的化学方程式:_____________________________________
(4)写出B属于酯的同分异构体的结构简式:_________________________________。
24.(9分)(普通班做)某烃的含氧衍生物A的相对分子质量为240,碳的质量分数为80.0%,氧的质量分数是氢的质量分数的2倍,且分子结构中含有2个苯环,每个苯环上都只有一个取代基,该取代基无支链。A在稀酸中加热可得到B和C,C的相对分子质量为108。
请填空:
(1)A的分子式______________________;
(2)B的结构简式为__________________;C的结构简式为__________________;
(3)A在稀酸溶液中反应的化学方程式为___________________________。
(4)写出B属于酯的同分异构体的结构简式:______________________________。
23.(10分)有机物A在一定条件下有如下图的转换关系:
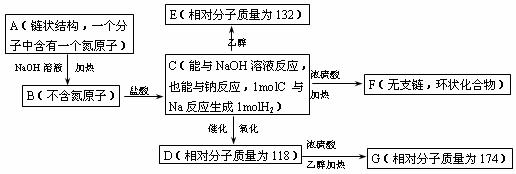
试回答下列问题:
(1)在A~G中属于酯类化合物的是__________________。
(2)写出A、D、F的结构简式:A:_____________D:____________ F:____________。
(3)写出下列反应的化学方程式:
A→B:_______________________________________________________________
C→D:____________________________________________________________
22.(11分)已知:
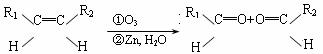
(1)该反应的生成物中含有的官能团的名称是__________,该物质在一定条件下能发生_______(填序号)。
①银镜反应 ②酯化反应 ③还原反应
(2)已知HCHO分子中所有原子都在同一平面内,若要使R1CHO分子中所有原子可能都在同一平面内,R1可以是________(填序号)。
①-CH3 ②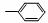 ③-CH═CH2
③-CH═CH2
(3)某氯代烃A的分子式为C6H11Cl,它可以发生如下转化:
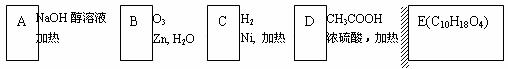
结构分析表明E分子中含有两个甲基且没有支链。
①A、E的结构简式分别为__________________、_______________________。
②写出下列转化的反应方程式及反应类型:
A→B__________________________________________________;___________
D→E__________________________________________________;____________
21.(6分)化学式C7H7NO2的有机物A、B、C、D分子中均含有一个苯环、两个相邻的侧链,其中A只显酸性,B只显碱性,C显中性,D既能与酸反应又能与碱反应。
写出符合下列条件的各物质的结构简式
A__________________________ B__________________________
C__________________________ D__________________________
20.(10分)氢氧化铜是一种常用试剂。例如,利用新制氢氧化铜验证醛类物质的还原性。
(1)新制氢氧化铜悬浊液的配制,实验室配制新制的氢氧化铜悬浊液的操作方法:在试管里加入10%的氢氧化钠溶液2mL,滴入2%的硫酸铜溶液4~6滴,振荡即成。这样操作的目的是______________________________。
下面是三个研究性学习小组分别从不同层面开展的研究性学习活动。
(2)研究性学习小组甲:对教材实验结论“乙醛与新制氢氧化铜反应生成的红色沉淀是Cu2O”提出质疑,他们认为红色沉淀不一定是氧化亚铜。为了确定红色沉淀的成分,开展了如下研究:提出猜想:_____________________________________。
查阅资料:①氧化亚铜属于碱性氧化物;②+1价的铜离子在酸性条件下易发生自身氧化还原反应;③在空气中灼烧氧化亚铜生成氧化铜。
设计方案:方案1:取该红色沉淀溶于足量的稀硝酸中,观察溶液颜色变化
方案2:取该红色沉淀溶于足量的稀硫酸中,观察是否有残渣
方案3:称取红色沉淀a g,在空气中充分灼烧至完全变黑,并在干燥器里冷却,再称重,反复多次至到固体恒重,称得质量为b g,比较a、b关系。
方案4:取红色固体沉淀装入试管里,加入酸化的硝酸银溶液,观察是否有银白色银析出。
你认为合理的方案是________________。
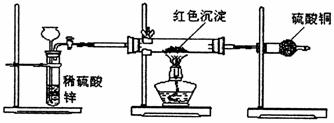
(3)研究性学习小组乙针对小组甲的质疑,设计新的探究方案,装置如下图所示。你认为要测定上述红色沉淀成分必须测定下列哪些物理量(只填序号):_________。
①通入氢气体积;②反应前,红色沉淀+硬质玻璃管的总质量;③完全反应后红色固体+硬质玻璃管的总质量;④实验前,干燥管质量;⑤硬质玻璃管质量;⑥锌粒质量;⑦稀硫酸中含溶质的量;⑧实验后,干燥管质量
(4)研究性学习小组丙上网查阅新闻得知,“2005年诺贝尔化学奖授予了三位研究绿色化学的科学家”。绿色化学强调对环境友好,实现零排放。“变废为宝”符合绿色化学要求。他们收集上述红色沉淀制备化学试剂--蓝矾。请你帮助他们设计一个简单且符合绿色化学要求的实验方案:_________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com