
9.下列反应的离子方程式书写正确的是 ( )
A.铁屑溶于足量稀硝酸:Fe+4H++NO3-=Fe3++NO↑+2H2O
B.碳酸氢钙溶液中加入足量烧碱溶液:HCO3-+OH-=CO32-+H2O
C.过氧化钠固体与水反应: 2O22-+2H2O → 4OH-+O2↑
D.向KI与稀硫酸的混合溶液中通入氧气:4H++O2+4I-===2I2+2H2O
8.最近,美国普度大学的研究人员开发出一种利用铝镓合金加水制造氢气的新工艺。这项技术具有广泛的能源潜在用途,包括为汽车提供原料、潜水艇提供燃料等。该技术通过向铝镓合金注水,铝生成氧化铝,同时生成氢气。合金中镓(Ga,ⅢA)是关键成分,可阻止铝形成致密的氧化膜。下列关于铝、镓的说法正确的是 ( )
A.铝的金属性比镓强
B.铝的熔点比镓低
C.Ga(OH)3与Al(OH)3性质相似,一定能与NaOH溶液反应
D.铝、镓合金与水反应后的物质可以回收利用冶炼铝
7.某强酸性溶液中可能存在NO3-、I-、Cl-、Fe3+中的一种或几种。向该溶液中加入溴水后,Br2被还原,由此推断该溶液中 ( )
A.不含NO3-,含Fe3+ B.含有NO3-、I-、Cl-
C.含I-,但不能确定是否含Cl- D.含有Fe3+
6.下列反应中,调节反应条件以后,反应产物不会改变的是 ( )
A.钠与氧气 B.硫酸与铝片
C.盐酸与铁粉 D.二氧化硫与氨水
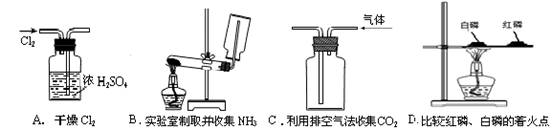
5.下列装置或操作能达到实验目的的 ( )
4.下列有关物质用途的说法中,正确的是 ( )
A.二氧化硅可用来制造半导体材料 B.硝酸常用作金属铜加工前的酸洗
C.氢氧化钠可用于治疗胃酸过多 D.三氧化二铁常用作红色油漆和涂料
3.符合实际并用于工业生产的是 ( )
A.CO2通入氢氧化钠溶液中制Na2CO3 B.H2和Cl2光照制HCl
C.Cl2通入澄清石灰水中制漂粉精 D.用硫磺制硫酸
2.海水是一个巨大的化学资源库,下列有关海水综合利用的说法正确的是.... ( )
A.从海水中可得到NaCl,电解熔融NaCl或其水溶液都可制得Cl2
B.因海水中含有镁元素,故不需经过化学变化就可以得到镁单质
C.利用蒸馏原理从海水中提取淡水是海水淡化技术发展的新方向
D.无论是海水波浪发电还是潮汐发电,都是将化学能转化为电能
1.下列选项体现了物质物理性质的是 ( )
A.纯碱除去油污 B.食醋清洗水垢
C.木炭吸附色素 D.臭氧消毒餐具
19.欲测定烟雾中的SO2含量,可做下列实验:取100L该空气(标准状况),通过盛放100mL过氧化氢(H2O2)水溶液的吸收瓶,使它们充分反应,生成硫酸。在吸收后的水溶液中加入BaCl2溶液,生成白色沉淀,经测定其质量为11.65g。
(1)试写出SO2和H2O2反应的离子方程式。
(2)写出H2SO4与BaCl2反应的离子方程式。
(3)求100L空气中SO2的体积分数。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com