
21.重水D2O的离子积为1.6×10-15,可以用PH一样的定义来规定pD=-lgc(D+),以下关于pD的叙述正确的是 ( )
A.中性溶液中PD=7
B.在1LD2O的溶液中溶解0.01mol NaOD(设溶液的体积为1L),其中pD=12
C.在1L D2O中溶解 0.01mol DCl(设溶液的体积为1L),其中pD=2
D.在100mL 0.25mol·L-1的NaOD重水溶液中加入50mL 0.2mol·L-1DCl的的重水溶液,其pD=1
20.恒温下,容积均为2L的密闭容器M、N中,分别有以下列两种起始投料建立的可逆反应3A(g)+2B(g)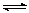 2C(g)+xD(s)的化学平衡状态,相关数据如下:M:3 mol A,2
mol B;2 min达平衡,生成D 1.2 mol,测得从反应开始到平衡C的速率为0.3 mol·(L·min)-1。N:2molC、ymolD;达平衡时c(A)=0.6 mol·L-1。下列推断的结论中不正确的是 ( )
2C(g)+xD(s)的化学平衡状态,相关数据如下:M:3 mol A,2
mol B;2 min达平衡,生成D 1.2 mol,测得从反应开始到平衡C的速率为0.3 mol·(L·min)-1。N:2molC、ymolD;达平衡时c(A)=0.6 mol·L-1。下列推断的结论中不正确的是 ( )
A.x=2 B.平衡时M中c(A)<0.6mol/L
C.y>0.8 D.y<0.8
19.500 mL KNO3和Cu(NO3)2的混合溶液中c(NO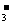 )=6mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4 L气体(标准状况),假定电解后溶液体积仍为500 mL,下列说法正确的是 (
)
)=6mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4 L气体(标准状况),假定电解后溶液体积仍为500 mL,下列说法正确的是 (
)
A.原混合溶液中 c (K+)为2 mol·L-1
B.上述电解过程中共转移4 mol电子
C.电解得到的Cu的物质的量为0.5mol
D.电解后溶液中c(H+)为2 mol·L-1
18.体积相同的甲、乙两容器中分别充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2 +
O2 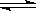 2SO3并达到平衡,在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器内SO2的转化率为P%,则乙容器中SO2的转化率 ( )
2SO3并达到平衡,在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器内SO2的转化率为P%,则乙容器中SO2的转化率 ( )
A.等于P% B.大于P% C.小于P% D.无法判断
17.可逆反应aA(g) + bB(g) cC(g) + dD(g)符合下图。则下列叙述正确的是 (
)
cC(g) + dD(g)符合下图。则下列叙述正确的是 (
)
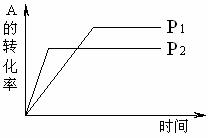
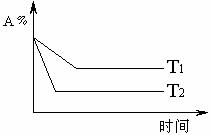
A.a+b < c+d;正反应吸热 B.a+b > c+d;正反应放热
C.a+b < c+d;正反应放热 D.a+b > c+d;正反应吸热
16.某密闭容器中发生如下反应:X(g)+3Y(g) 2Z(g);ΔH<0。下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是 ( )
2Z(g);ΔH<0。下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是 ( )
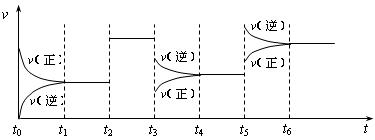
A.t2时加入了催化剂 B.t3时降低了温度
C.t5时增大了压强 D.t4-t5时间内转化率一定最低
15.已知NaHSO4在水中的电离方程式为:NaHSO4==Na++H++SO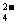 。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,不正确的是 ( )
。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,不正确的是 ( )
A.该温度高于25℃
B.由水电离出来的H+的浓度是1.0×10-12mol·L-1
C.加入NaHSO4晶体抑制了水的电离
D.该温度下加入等体积pH为12的NaOH溶液可使该溶液恰好呈中性
14.燃烧a g乙醇(液态),生成二氧化碳气体和液态水,放出的热量为Q,经测定,a g乙醇与足量钠反应,能生成标准状况下的氢气5.6L,则乙醇燃烧的热化学方程式书写正确的是( )
A.C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(1); △H = -Q
B.C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(1); △H = -Q/2
C.1/2 C2H5OH(1)+3/2O2(g)=CO2(g)+3/2H2O(1); △H = -Q
D.C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(1); △H = -2Q
13.阿波罗宇宙飞船上使用的是氢氧燃料电池,其电池反应为:2H2+O2=2H2O,电解液为KOH,反应保持在较高温度,使H2O蒸发,下列叙述正确的是 ( )
A.电池能发出蓝色火焰 B.H2为正极,O2为负极
C.正极反应为: O2+2H2O+4e -=4OH- D.正极反应为: 2H2+4OH--4e-=4H2O;
12.可以将反应Zn+Br2 = ZnBr2设计成蓄电池,下列4个电极反应
①Br2 + 2e- = 2Br- ②2Br- - 2e- = Br2 ③Zn – 2e- = Zn2+ ④Zn2+ + 2e- = Zn
其中表示充电时的阳极反应和放电时的负极反应的分别是 ( )
A.②和③ B.②和① C.③和① D.④和①
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com