
3.在烧杯中加入水和苯(密度:0.88 g/cm3)各50 mL。将一小粒金属钠(密度:0.97 g/cm3)投入烧杯中。观察到的现象可能是 ( )
A.钠在水层中反应并四处游动
B.钠停留在苯层中不发生反应
C.钠在苯的液面上反应并四处游动
D.钠在苯与水的界面处反应并可能作上、下跳动
2.在氯化铁、氯化铜和盐酸混合溶液中加入铁粉,待反应结束,所剩余的固体滤出后能被磁铁吸引,则反应后溶液中存在较多的阳离子是 ( )
A.Cu2+ B.Fe3+ C.Fe2+ D.H+
1.下列块状金属在常温时能全部溶于足量浓HNO3的是 ( )
A.Ag B. Au C.Al D.Fe
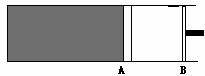
28.(11分)一定量的碳和1克水加热到1000℃发生C(s)+H2O(g)  CO(g)+H2(g)在一钢筒中达到平衡时活塞处于A处:
CO(g)+H2(g)在一钢筒中达到平衡时活塞处于A处:
(1)当温度不变时将活塞推到B处时混合气体的平均分子量将如何变化?(要求写出分析过程,仅写结果不给分)
(2)如果开始在一钢筒中加xmol的H2O,ymol CO,zmol的H2和一定量的碳,在上述条件下使混合气体的平均分子量的变化与上述变化相反,则x,y,z的关系如何?原混合气体的平均分子量应该满足什么条件?
27.(10分)有甲、乙两个容积相等的恒容密闭容器,向甲中通入6mol A和2mol B,向乙中通入1.5mol A、0.5mol B和3mol C,将两容器的温度恒定在770K,使反应3A(g)+B(g) xC(g)达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2,试回答下列有关问题:
xC(g)达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2,试回答下列有关问题:
(1)若平衡时,甲、乙两容器中A的物质的量相等,则x=_________;若平衡时,甲、乙两容器中A的物质的量不相等,则x=_________。
(2)若平衡时两容器中的压强不相等,则两容器中压强之比为 。
(3)平衡时甲、乙两容器中A、B的物质的量之比是否相等____________(填“相等”或“不相等”),平衡时甲中A的体积分数为____________。
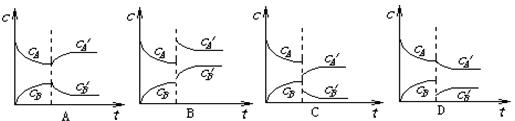
26.(16分)可逆反应2A(g)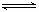 B(g)(放热反应)从反应开始至建立平衡后改变某一外界条件(外界条件指的是温度、压强、浓度和催化剂)使平衡发生了移动至新的平衡,该过程中各物质的浓度(用c表示)随时间变化情况如下图所示,试分析各图,指出导致平衡移动的因素和平衡移动的方向:
B(g)(放热反应)从反应开始至建立平衡后改变某一外界条件(外界条件指的是温度、压强、浓度和催化剂)使平衡发生了移动至新的平衡,该过程中各物质的浓度(用c表示)随时间变化情况如下图所示,试分析各图,指出导致平衡移动的因素和平衡移动的方向:
|
序号 |
平衡移动的因素 |
平衡移动的方向 |
|
A |
|
|
|
B |
|
|
|
C |
|
|
|
D |
|
|
25.在密闭容器中进行下列反应:M (g)+N (g)  R
(g)+2
L此反应符合下边图像。下列叙述正确的是
( )
R
(g)+2
L此反应符合下边图像。下列叙述正确的是
( )
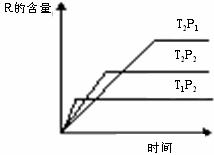
A.正反应吸热,L是气体 B.正反应吸热,L是固体
C.正反应放热,L是液体 D.正反应放热,L是气体
第Ⅱ卷(非选择题,共50分)
24.常温下,某溶液中由水电离的c(H+) = 1×10-13mol·L-1,该溶液可能是 ( )
①二氧化硫水溶液 ②氯化铵水溶液
③硝酸钠水溶液 ④氢氧化钠水溶液
A.①④ B.①② C.②③ D.③④
23.可以证明可逆反应N2 + 3H2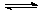 2NH3已达到平衡状态的是 ( )
2NH3已达到平衡状态的是 ( )
①一个N≡N断裂的同时,有3个H-H键断裂
②一个N≡N键断裂的同时,有6个N-H键断裂
③其它条件不变时,混合气体平均式量不再改变
④保持其它条件不变时,体系压强不再改变
⑤NH3%、N2%、H2%都不再改变
⑥恒温恒容时,密度保持不变
⑦正反应速率v(H2) = 0.6mol/(L·min),逆反应速率v(NH3) = 0.4mol/(L·min)
A.全部、 B.只有①③④⑤ C.②③④⑤⑦ D.只有③⑤⑥⑦
22.pH=11的x、y两种碱溶液各5mL,分别稀释至500mL,其pH与溶液体积(V)的关系如图所示,下列说法正确的是 ( )
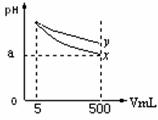
A.稀释后x溶液中水的电离程度比y溶液中水电离程度小
B.若x、y是一元碱,等物质的量浓度的盐酸盐溶液y的pH大
C.若x、y都是弱碱,则a的值一定大于9
D.完全中和x,y两溶液时,消耗同浓度稀硫酸的体积V(x)>V(y)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com