
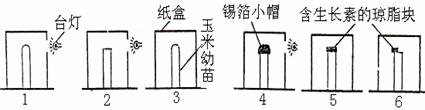
(一)方法步骤:取6个小花盆,各栽入一株品种、粗细和大小都相同的玉米幼苗(要求幼苗的真叶未突破胚芽鞘)。按下图所示方法进行实验处理。接通台灯电源24h后,打开纸盒,观察并记录6株玉米幼苗的生长情况。
14.当两分子间的距离为r0时,分子间的作用力为零,如果距离变为r,则:
A、当r>r0时分子间的作用力为斥力,当r<r0时分子间的作用力为引力
B、当r>r0时分子间的作用力为斥力,当r<r0时分子间的作用力也为斥力
C、当r>r0时分子间的作用力为引力,当r<r0时分子间的作用力为斥力
D、当r>r0时分子间的作用力为引力,当r<r0时分子间的作用力也为引力
15.关于电场强度的关系式E=F/q,下列的说法中正确的是:
A、电场强度的大小E跟电场力F的大小成正比
B、电场强度的大小E跟电量q的大小成反比
C、电场强度的大小E可以用电场力F跟电量q的比值来计算
D、不放入点电荷,就没有电场力,电场强度也就为零
16.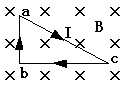 如图所示,直角三角形形状的闭合导线框abc通以顺时针方向的电流I,放在匀强磁场中,线框平面与磁场方向垂直,ab∶bc∶ca=3∶4∶5,则线框受到的安培力的合力为:
如图所示,直角三角形形状的闭合导线框abc通以顺时针方向的电流I,放在匀强磁场中,线框平面与磁场方向垂直,ab∶bc∶ca=3∶4∶5,则线框受到的安培力的合力为:
A、垂直于ab向左 B、垂直于bc向下
C、垂直于ca斜向上 D、为零
17.下列关于电势高低的判断,正确的是:
A、正电荷从A点移到B点时,其电势能增加,A点电势一定较低。
B、正电荷只在电场力作用下,从A点移动到B点,A点的电势一定较高。
C、负电荷从A点移到B点,负电荷克服电场力做功,A点的电势一定较高。
D、负电荷从A点移到B点,电势能增加,A点的电势一定较低。
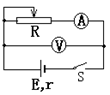
18.如图所示的电路,当电键S闭合后,电流表和电压表的示数分别为I1和U1,可变电阻R的滑动触头向右移动后,电流表和电压表的示数分别变成为I2和U2,则有:
 A、I1<I2,U1<U2 B、I1<I2,U1>U2
A、I1<I2,U1<U2 B、I1<I2,U1>U2
C、I1>I2,U1>U2 D、I1>I2,U1<U2
19.如图所示,A、B为带等量异号点电荷,A带正电,B带负电.在A、B的连线上取a、b、c三点,其中b为连线的中点,a、c两点与b点等距,则:
A、a点的电场强度与c点的电场强度相同
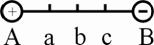 B、a点电势与c点电势相同
B、a点电势与c点电势相同
C、a、b间的电势差与b、c间的电势差相同
D、将另一点电荷q由b点沿垂直A、B的连线方向移动,电场力做功为零
20.下列说法中正确的是:
A、做功和热传递在改变内能的效果上是等效的,因此做功与热传递是没有区别的
B、虽然做功和热传递在改变内能的效果上是等效的,但我们还是可以通过分析改变前后的物体的内能,来区别是做功还是热传递改变内能的
C、做功和热传递在改变内能的效果上是等效的,表明要使物体的内能发生变化,既可以通过做功来实现,也可以通过热传递来实现
D、做功和热传递在改变内能的效果上是等效的,说明人在出汗散热时,还可以通过对外做功来代替出汗改变内能
21.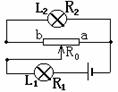 如图所示,灯L1、L2的电阻分别为R1、R2,变阻器最大的电阻为R0,若有电流通过,灯就发光,而且灯的电阻不变。当变阻器的触头P由a端向b端移动时,L1、L2的亮度变化情况是:
如图所示,灯L1、L2的电阻分别为R1、R2,变阻器最大的电阻为R0,若有电流通过,灯就发光,而且灯的电阻不变。当变阻器的触头P由a端向b端移动时,L1、L2的亮度变化情况是:
A、当R2>R0时,L1变暗,L2变亮;
B、当R2>R0时,L1先变暗后变亮,L2先变亮后变暗;
C、当R2<R0时,L1先变暗后变亮,L2先变亮后变暗;
D、当R2<R0时,L1先变暗后变亮,L2不断变亮。
第Ⅱ卷(非选择题)
22.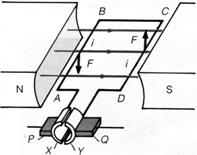 右图是直流电动机的原理图,其中P、Q和X、Y是电动机中的两个部件,电动机中的转子能够不停地绕同一方向转动,是利用上述部件中________部件实现的,我们把这一部件叫做________。
右图是直流电动机的原理图,其中P、Q和X、Y是电动机中的两个部件,电动机中的转子能够不停地绕同一方向转动,是利用上述部件中________部件实现的,我们把这一部件叫做________。
23.表格中所列数据是测量小灯泡U-I关系的实验数据:
|
U(V) |
0.0 |
0.2 |
0.5 |
1.O |
1.5 |
2.0 |
2.5 |
3.0 |
|
I(A) |
0.000 |
0.050 |
0.100 |
0.150 |
0.180 |
0.195 |
0.205 |
0.215 |
(1)根据表格中的数值,在右方的方格纸内画出小灯泡的U-I图线,并给此曲线标上字母M。
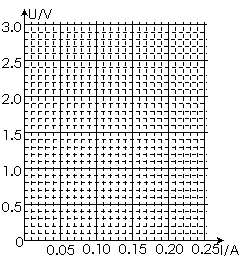
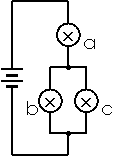
(2)如下图所示,用三个上述小灯泡组成一个串并联组合电路,连接到内阻不计、电动势为3V的电源上。
(a)说明怎样利用图像求解流过灯泡b的电流。
1.____________________________
2.____________________________
3.____________________________
(b)流过小灯泡b中的电流约为______A。
24.(12分)带电量分别为+1.0×10-6C和-9.0×10-6C的两个点电荷,测得它们之间的相互作用力的大小为0.1N,则两点电荷之间的距离为多少m?
(静电力常量k=9.0×109N·m2/C2)
25.(18分)如图所示,在与水平方向成60°角的光滑金属导轨间连一电源,在相距1m的平行导轨上放一重力为3N的金属棒ab,棒上通过3A的电流,磁场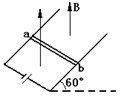 方向竖直向上,这时金属棒恰好静止,求:
方向竖直向上,这时金属棒恰好静止,求:
(1)匀强磁场的磁感强度为多大?
(2)ab棒对导轨的压力为多大?
26.(21分)长江三峡工程位于长江西陵峡中段,坝址在湖北省宜昌市三斗坪。三峡工程是一座具有防洪、发电、航运及养殖和供水等巨大综合利用效益的特大型水利水电工程。主要数据如下表。试根据表中数据,计算:
(1)三峡每年可利用的最大水力能为多少?
(2)有百分之几转化为了电能?
(3)26台发电机组全部建成发电后,按设计要求年发电时间为多少天?
(重力加速度g=9.8m/s2)
|
大坝 |
坝高 l85m |
蓄水位 175m |
坝长 2335m |
|
水库 |
总库容量 3.93×1010m3 |
防洪库容量 2.215×1.010m3 |
平均年流量 4.51×1011m3 |
|
电站 |
总装机数 26台 |
总装容量 1.82×107kW |
年平均发电量 8.468×1010kW·h |
|
通航 |
船闸 万吨级双线5级船闸一座 |
垂直升船机 3000t级单线垂直升船机1座 |
年单向通船能力 5×107t |
27.(7分)与淀粉相关的物质间转化关系如下图所示。其中B的分子中含有一个甲基,B与羧酸和醇均能发生酯化反应;C的催化氧化产物既是合成酚醛树脂的原料之一,又是常见的居室污染物;E能使Br2的CCl4溶液褪色。


(1)B的结构简式是 。
(2)E→F的化学方程式是 。
(3)某同学欲验证淀粉完全水解的产物A,进行如下实验操作:①在试管中加入少量淀粉 ②加热3-4 min ③加入少量新制的Cu(OH)2悬浊液 ④加入少量稀硫酸 ⑤加热 ⑥待冷却后,滴加NaOH溶液至溶液呈碱性。
则以上操作步骤正确的顺序是(填选项序号) 。
a.①②④⑤③⑥ b.①④②③⑤⑥ c.①④②⑥③⑤ d.①⑤③④⑥②
28.(14分)A、B、C、D、E是中学常见的5种化合物,A、B是氧化物,元素X、Y的单质是生活中常见的金属,相关物质间的关系如下图所示。
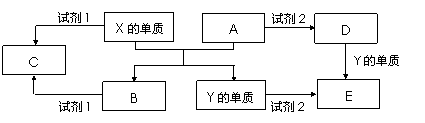
(1)X的单质与A反应的化学方程式是 。
(2)若试剂1是NaOH溶液,X的单质与试剂1反应的离子方程式是 。
(3)若试剂1和试剂2均是稀硫酸。
①检验物质D的溶液中金属离子的方法是 。
②将物质C溶于水,其溶液呈酸性,原因是(用离子方程式表示) 。
③某高效净水剂是由Y(OH)SO4聚合得到的。工业上以E、稀硫酸和亚硝酸钠为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是 。
29.(12分)有机物A可作为合成降血脂药物安妥明和某聚碳酸酯工程塑料
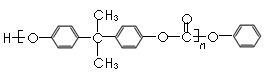
( )的原料之一。
已知: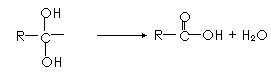 ①如下有机物分子结构不稳定,会发生变化:
①如下有机物分子结构不稳定,会发生变化:
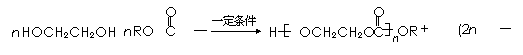 ②某些醇或酚可以与碳酸酯反应生成聚碳酸酯,如:
②某些醇或酚可以与碳酸酯反应生成聚碳酸酯,如:
相关的合成路线如下图所示。
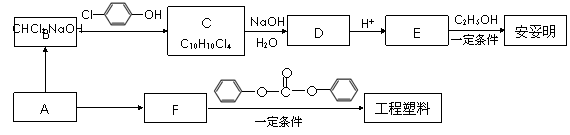
(1)经质谱测定,有机物A的相对分子质量为58,燃烧2.9 g有机物A,生成标准状况下3.36 L CO2和2.7 g H2O,A的核磁共振氢谱只出现一个吸收峰。则A的分子式是 。
(2)E→安妥明反应的化学方程式是 。
(3)C可能发生的反应类型(填选项序号) 。
a.取代反应 b.加成反应 c.消去反应 d.还原反应
(4)F的结构简式是 。
(5)写出同时符合下列条件的,E的同分异构体X的结构简式(只写1种即可) 。
①X能与饱和溴水发生取代反应
②X的苯环上有2个取代基,且苯环上的一溴取代物只有2种
③1 mol X与足量NaHCO3溶液反应生成1 mol CO2,与足量Na反应生成1 mol H2
④X与NaOH水溶液发生取代反应所生成的官能团能被连续氧化为羧基
30.(15分)某校化学小组学生利用下图所列装置进行“铁与水反应”的实验,并利用产物进一步制取FeCl3·6H2O晶体。(图中夹持及尾气处理装置均已略去)
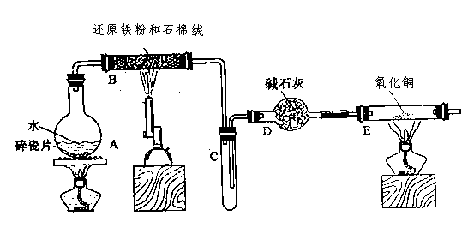
⑴ 装置B中发生反应的化学方程式是___________________________________。
⑵ 装置E中的现象是_______________________________________。
⑶ 停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤。
简述检验滤液中Fe3+的操作方法______________________________________ _____________________________________________________________________。
⑷ 该小组学生利用上述滤液制取FeCl3·6H2O晶体,设计流程如下:
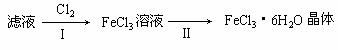
① 步骤I中通入Cl2的作用是___________________________________________。
② 步骤II从FeCl3稀溶液中得到FeCl3·6H2O晶体的主要操作包括:_____________________________________________________________________。
③ 该流程中需保持盐酸过量,主要原因是(结合离子方程式简要说明) ____________________________________________________________________。
31.(12分)小苏打、胃苏平、达喜都是常见的中和胃酸的药物。
(1)小苏打每片含0.5gNaHCO3,2片小苏打和胃酸完全中和,被中和的H+是
mol。
(2)胃苏平每片含0.245gAl(OH)3,中和胃酸时,6片小苏打片相当于胃苏平 片。
(3)达喜的化学成分是铝和镁的碱式盐。
①取该碱式盐3.01g加入2.0molL-1盐酸使其溶解,当加入盐酸42.5mL时,开始产生CO2,加入盐酸45mL时正好反应完全,该碱式盐样品中氢氧根离子与碳酸跟离子的物质的量之比为 。
②在上述碱式盐溶于盐酸后的溶液中加入过量的氢氧化钠,过滤,沉淀物进行干燥后重1.734g,若该碱式盐中氢元素的质量分数为0.040,则该碱式盐的化学式是 。
32、为了验证植物向光性与植物生长素的关系,有人设计了如下实验方案。
13.多硫化钠Na2Sx(x≥2)在结构上与Na2O2、FeS2、CaC2等有相似之处。Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,而NaClO被还原为NaCl,反应中Na2Sx与NaClO的物质的量之比为1∶16,则x值是
A.5 B.4 C.3 D.2
12.印刷铜制电路板的“腐蚀液”为FeCl3溶液。已知铜、铁均能与FeCl3溶液反应,反应方程式分别为:Cu+2FeCl3=2FeCl2+CuCl2,Fe+2FeCl3=3FeCl2。现将一包铜、铁的混合粉末加入到盛有FeCl3溶液的烧杯中,充分反应后烧杯中仍有少量固体,关于烧杯中物质组成的说法正确的是
A.溶液中一定含FeCl3,固体一定是铁和铜
B.溶液中一定含FeCl2,固体一定含铜
C.溶液中一定含FeCl2、CuCl2,固体一定含铜
D.溶液中一定含FeCl2,固体一定是铁和铜
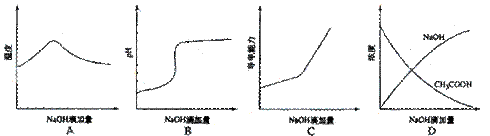
11.将氢氧化钠稀溶液滴加到醋酸稀溶液中,下列各图示意混合溶液有关量或性质的变化趋势,其中错误的是
10.关于浓度均为0.1 mol/L的三种溶液:①氨水、②盐酸、③氯化铵溶液,下列说法不正确的是
A. c(NH+4):③>①
B. 水电离出的c(H+):②>①
C.
①和②等体积混合后的溶液:c(H+)=c(OH )+c(NH3·H2O)
)+c(NH3·H2O)
D.
①和③等体积混合后的溶液:c(NH+4)>c(Cl )>c(OH
)>c(OH )>c(H+)
)>c(H+)
9.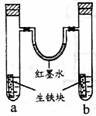 右图装置中,U型管内为红墨水,a、b试管内分别盛有食盐水和氯化铵溶液,各加入生铁块,放置一段时间。下列有关描述错误的是
右图装置中,U型管内为红墨水,a、b试管内分别盛有食盐水和氯化铵溶液,各加入生铁块,放置一段时间。下列有关描述错误的是
A.生铁块中的碳是原电池的正极
B.红墨水柱两边的液面变为左低右高
C.两试管中相同的电极反应式是:Fe-2e-﹦Fe2+
D.a试管中发生了吸氧腐蚀,b试管中发生了析氢腐蚀
8.在体积可变的密闭容器中,反应mA(g)+nB(s) pC(g)达到平衡后,压缩容的体积,发现A的转化率随之降低。下列说法中,正确的是
A.(m+n)必定小于p B.(m+n)必定大于p
C.m必定小于p D.n必定小于p
7.人类生活质量与环境因素密切相关,下列关于环境的说法正确的时
A.二氧化碳与二氧化硫一样回导致形成酸雨
B.人类应当将大气中的二氧化碳全部除去,以防止温室效应
C.不使用含碳能源是当前我国减少二氧化碳排放最为有效的措施
D.用“CCS”技术捕获的二氧化碳来制造纯碱,1000kg二氧化碳最多可制得纯碱2409kg
6. O3和H2O2都是常见的氧化剂,下列有关说法错误的是
A.O3和O2互为同位素
B.O3和H2O2的分子内都含有共价键
C.H2O2具有氧化性,可用于消毒杀菌
D.高空中的O3层保护保护人类免受紫外线的伤害
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com