
4.永动机不可能制成
第一类永动机:不消耗任何能量,却可以源源不断地对外做功.这种永动机违背能量守恒定律,是不可能制造成的.
第二类永动机:只从单一热源吸收热量,全部用来做功,而没有冷凝.这类永动机虽然不违反能量守恒定律,但与热力学第二定律却是矛盾的,这类永动机也是不可能制造成的.
●典例剖析
[例1]图8-1-2中关于布朗运动的实验,下列说法正确的是
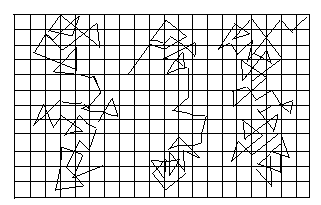
图8-1-2
A.图中记录的是分子无规则运动的情况
B.图中记录的是微粒做布朗运动的轨迹
C.实验中可以看到,微粒越大,布朗运动越明显
D.实验中可以看到,温度越高,布朗运动越剧烈
[解析]图中记录的是每隔若干时间(如30 s)微粒位置的连线,而这段时间内微粒的运动情况却不得而知.虽然图示所反映的不是微粒的轨迹,但却可看出其运动的无规则性.
做布朗运动的微粒都很小,一般为10-6 m左右.微粒做布朗运动的根本原因是:各个方向的液体分子对它的碰撞不平衡.因此,只有微粒越小、温度越高时布朗运动才越剧烈.故选D.
[说明] 针对课本中演示实验的考查在往年的高考中经常出现,做好这类题目的关键是:搞清原理、认真观察,在可能的情况下亲自动手做一做.
[设计意图] 布朗运动是说明分子运动规律的重要宏观现象,通过本例加深学生对布朗运动的认识.
[例2]已知水的密度ρ=1.0×103 kg/m3,水的摩尔质量Mmol=1.8×10-2 kg/mol,求:
(1)1 cm3的水中有多少个水分子.
(2)估算一个水分子的线度多大.
[解析] 水的摩尔体积
Vmol=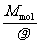 =
=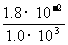 m3/mol
m3/mol
=1.8×10-5 m3/mol
(1)1 cm3水中的水分子数
n=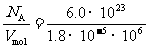 /cm3=3.3×1022/cm3
/cm3=3.3×1022/cm3
(2)建立水分子的球模型,有
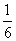 πd3=
πd3=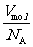
水分子直径
d=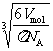 =
= m=3.9×10-10
m
m=3.9×10-10
m
建立水分子的立方体模型,有
d3=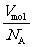
水分子直径
d=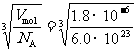 m=3.1×10-10
m.
m=3.1×10-10
m.
[说明] 不论把分子看做球体,还是看做立方体,都只是一种简化的模型,是一种近似处理的方法.由于建立的模型不同,得出的结果稍有不同,但数量级都是10-10 m .一般在估算固体或液体分子线度或分子间距离时采用球模型,在估算气体分子间的距离时采用立方体模型.
[设计意图] 阿伏加德罗常数是联系宏观量和微观量的重要常数,涉及阿伏加德罗常数的计算也是高考常考的内容.通过本例说明以阿伏加德罗常数为桥梁,由宏观量求微观量或由微观量求宏观量的方法.
※[例3]如图8-1-3所示,在质量为M的细玻璃管中盛有少量乙醚液体,用质量为m的软木塞将管口封闭.加热玻璃管使软木塞在乙醚蒸气的压力下水平飞出,玻璃管悬于长为l的轻杆上,细杆可绕上端O轴无摩擦转动.欲使玻璃管在竖直平面内做圆周运动,在忽略热量损失的条件下,乙醚最少要消耗多少内能?
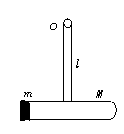
图8-1-3
[解析] 加热玻璃管的过程中乙醚内能增大,由液态变成气态.管内压强增大将软木塞顶开,乙醚内能减少,玻璃管和软木塞机械能增大.根据动量守恒定律和能量守恒定律即可求出乙醚内能的改变量.
设软木塞水平飞出时M和m的速率分别为v1和v2,由动量守恒定律得:
mv2=Mv1=0 ①
细玻璃管恰能越过最高点的条件是速度为零,由机械能守恒定律得:
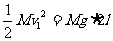 ②
②
由能量守恒定律知,管塞分离时二者动能之和等于乙醚消耗的内能E内,即:
E内=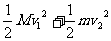 ③
③
联立①②③式可得E内=2Mgl(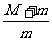 ).
).
[说明] 能量守恒定律贯穿于整个物理学的始终,从能量的角度分析和求解问题是一条重要的途径.在利用能量守恒定律列方程时,一定要分析清有几种形式的能量,它们是如何实现转化和转移的,哪种形式的能量增加,哪种形式的能量减少.这些都清楚了,然后列式运算才会少出错误.
[设计意图] 通过本例说明综合利用有关规律分析解决力、热综合问题的思路方法.
●反馈练习
★夯实基础
3.物体的内能与温度和体积的关系
温度变时分子动能变,体积变时分子势能变,因此物体的内能决定于它的温度和体积.但这句话却不能作为判断两物体内能大小的依据.如两物体温度和体积均相同,而内能却没有确定的关系.再如,0℃的冰融化成0℃的水,体积减少,不能就此认为其势能也减少.而应从改变内能的两种方式上去分析.冰融化过程吸收热量,内能增加,而温度不变,所增加的只是分子的势能.
2.分子间的相互作用力
分子力是邻近的分子间原子核的正电荷和核外电子之间的相互作用引起的有复杂规律的力.分子力的变化可由图8-1-1所示.分子距离r在0-r0间合力F表现为斥力;在r>r0后合力表现为引力,且引力先增大后减小;当r达到十几个埃时,分子力减为零.
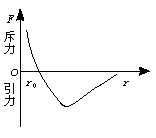
图8-1-1
由分子间的相对位置和相互作用而决定的能叫分子势能.当物体被拉伸时,r>r0,外力克服分子引力做功,分子势能增加;当物体被压缩时,r<r0,外力克服分子斥力做功,分子势能增加,通常状态下,分子距离r=r0,分子力为零,分子势能最小.
总之,分子的热运动让分子分散开,分子间的相互作用力让分子聚集在一起,二者相互制约,构成了固、液、气三态,决定了物体的内能.
能量既不能凭空产生,也不能凭空消失,它只能从一种形式转化为别的形式,或从一个物体转移到别的物体,在转化和转移的过程中其总量不变.
●疑难解析
1.阿伏加德罗常数是联系微观物理量和宏观物理量的桥梁.在此所指微观物理量为:分子的体积v、分子的直径d、分子的质量m.宏观物理量为:物质的体积V、摩尔体积Vmol、物质的质量M、摩尔质量Mmol、物质的密度ρ.
(1)计算分子质量:m=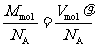
(2)计算分子的体积:v=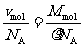
分子直径:d=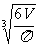 (球体模型),d=
(球体模型),d=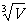 (立方体模型)
(立方体模型)
(3)计算物质所含的分子数:
n=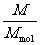 ·NA=
·NA=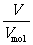 ·NA=
·NA=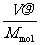 ·NA=
·NA=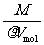 ·NA
·NA
例如,估算标准状况下气体分子间的距离时,由于气体分子间距离较大,各分子虽然做热运动,但仍可看做是均匀分布的.1 mol任何气体在标准状况下的体积均为22.4 L,将其分成若干个小立方体,每个小立方体内装一个分子,立方体的边长即分子间的距离.
d=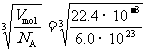 m≈3×10-9 m
m≈3×10-9 m
3.热力学第三定律
不可能用有限的手续使一物体冷却到绝对温度的零度(绝对零度不可能达到).
2. 热力学第二定律
表述一:不可能使热量由低温物体传递到高温物体,而不引起其他变化.
表述二:不可能以单一热源吸收热量并把它全部用来做功,而不引起其他变化.
热力学第二定律使人们认识到:自然界中进行的涉及热现象的宏观过程都具有方向性.
1.热力学第一定律
在一般情况下,如果物体跟外界同时发生做功和热传递的过程,外界对物体所做的功W加上物体从外界吸收的热量Q等于物体内能的增加ΔU.即:
ΔU=Q+W
利用ΔU=Q+W讨论问题时,必须弄清其中三个量的符号法则.外界对物体做功,W取正值,反之取负值;物体从外界吸收热量,Q取正值,反之取负值;物体内能增加,ΔU取正值,反之取负值.
2.热传递:吸收热量,物体内能增加;放出热量,物体内能减少.
做功和热传递在改变物体的内能上是等效的,但本质有区别.通过做功改变物体的内能,是使物体的内能和其他形式的能量发生转化.通过热传递改变物体内能,是使内能从一个物体转移到另一个物体.
改变物体的内能有两种方式:
1.做功:外力做功,物体内能增加;克服外力做功,物体内能减少.
3.物体的内能:物体内所有分子的动能和势能的总和叫物体的内能.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com