
2.物质熔沸点的比较
⑴不同类晶体:一般情况下,原子晶体>离子晶体>分子晶体
⑵同种类型晶体:构成晶体质点间的作用大,则熔沸点高,反之则小。
四种晶体熔、沸点对比规律
①离子晶体:结构相似且化学式中各离子个数比相同的离子晶体中,离子半径小(或阴、阳离子半径之和越小的),键能越强的熔、沸点就越高。如NaCl、 NaBr、Nal;NaCl、KCl、RbCl等的熔、沸点依次降低。 离子所带电荷大的熔点较高。如:MgO熔点高于 NaCl
②分子晶体:在组成结构均相似的分子晶体中,式量大的分子间作用力就大熔点也高。如:F2、Cl2、 Br2、I2和HCl、HBr、HI等均随式量增大。熔、沸点升高。但结构相似的分子晶体,有氢键存在熔、沸点较高。
③原子晶体:在原子晶体中,只要成键原子半径小,键能大的,熔点就高。如金刚石、金刚砂(碳化硅)、晶体硅的熔、沸点逐渐降低。
④金属晶体:在元素周期表中,主族数越大,金属原子半径越小,其熔、沸点也就越高。如ⅢA的Al, ⅡA的Mg,IA的Na,熔、沸点就依次降低。而在同一主族中,金属原子半径越小的,其熔沸点越高。
⑶常温常压下状态
①熔点:固态物质>液态物质
②沸点:液态物质>气态物质
1.离子晶体、原子晶体、分子晶体和金属晶体的比较
|
晶体类型 |
原子晶体 |
分子晶体 |
金属晶体 |
离子晶体 |
|
晶体质点 (粒子) |
原子 |
分子 |
金属阳离子、自由电子 |
阴、阳离子 |
|
粒子间作用(力) |
共价键 |
分子间作用力 |
复杂的静电作用 |
离子键 |
|
熔沸点 |
很高 |
很低 |
一般较高,少部分低 |
较高 |
|
硬度 |
很硬 |
一般较软 |
一般较硬,少部分软 |
较硬 |
|
溶解性 |
难溶解 |
相似相溶 |
难溶(Na等与水反应) |
易溶于极性溶剂 |
|
导电情况 |
不导电 (除硅) |
一般不导电 |
良导体 |
固体不导电,熔化或溶于水后导电 |
|
实例 |
金刚石、水晶、碳化硅等 |
干冰、冰、纯硫酸、H2(S) |
Na、Mg、Al等 |
NaCl、CaCO3 NaOH等 |
5. 晶格能越大,形成的离子晶体_________________________,而且熔点_______________,硬度______________.典型的离子晶体,晶格能的大小与离子所带的电荷和离子半径的关系一般是:离子电荷高,晶格能 ,离子半径大,晶格能 。
[方法导引]
4. 离子晶体的晶格能的定义是________________________________________________.离子晶体的晶格能是最能反映_____________________的数据.
3.___________________________________是决定离子晶体结构的重要因素.此外, 离子晶体的结构还取决于____________________________.
2. 离子晶体中的配位数是指___________________________________________________.
1.构成离子晶体的粒子是 ,粒子之间的相互作用是 ,这些粒子在晶体中 (能或不能)自由移动,所以离子晶体 (能或不能)导电.
14.函数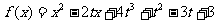 , 其中
, 其中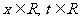 , 将
, 将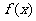 的最小值记为
的最小值记为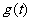 .
.
(1)求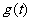 的表达式;
的表达式;
(2)讨论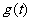 在区间[-1,1]内的单调性;
在区间[-1,1]内的单调性;
(3) 若当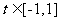 时,
时,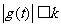 恒成立,其中
恒成立,其中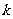 为正数,求
为正数,求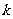 的取值范围.
的取值范围.
解: (1) 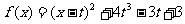 ,
,
当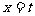 时,
时, 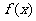 达到其最小值
达到其最小值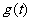 ,即
,即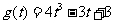 ;
;
(2)因为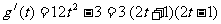 ,
,
列表如下:
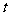
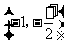
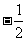
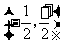
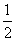
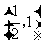

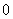
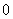

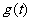 |
增 |
极大值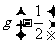 |
减 |
极小值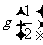 |
增 |
由此可见,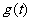 在区间
在区间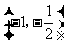 和
和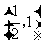 单调递增,在区间
单调递增,在区间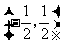 单调递减;
单调递减;
(3) 
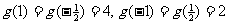 ,所以
,所以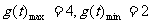 ;
;

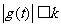 既
既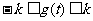 恒成立,所以
恒成立,所以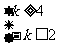 ,综合可得k的范围为
,综合可得k的范围为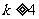 。
。
13.已知函数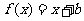 的图像与函数
的图像与函数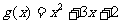 的图象相切,记
的图象相切,记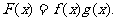
(1)求实数b的值及函数F(x)的极值;
(2)若关于x的方程F(x)= k恰有三个不等的实数根,求实数k的取值范围.
解:(1)依题意,令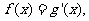 ,得
,得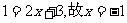

列表如下:
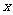 |
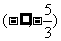 |
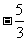 |
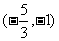 |
-1 |
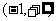 |
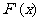 |
+ |
0 |
- |
0 |
+ |
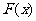 |
增 |
极大值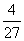 |
减 |
极小值0 |
增 |
从上表可知 处取得极小值
处取得极小值
(2)由(1)可知函数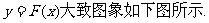 作函数
作函数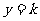 的图象,当
的图象,当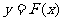 的图象与函数
的图象与函数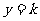 的图象有三个交点时,关于x的方程
的图象有三个交点时,关于x的方程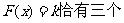

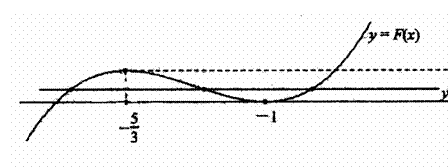
12.已知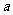 为实数,函数
为实数,函数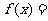
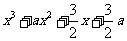 .
.
(1)若函数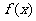 的图象上有与
的图象上有与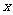 轴平行的切线,求
轴平行的切线,求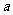 的取值范围;
的取值范围;
(2)若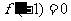 ,对任意
,对任意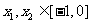 ,不等式
,不等式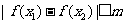 恒成立,求
恒成立,求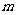 的最小值.
的最小值.
解:(1)∵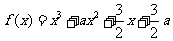 ∴
∴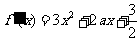 .
.
由题意知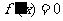 有实数解. ∴△
有实数解. ∴△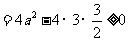
∴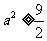 ,即
,即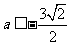 或
或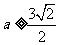 . 故
. 故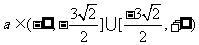 .
.
(2)∵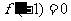 ∴
∴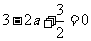 即
即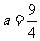 .
.
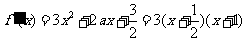 ,令
,令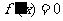 得
得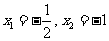 .
.
当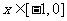 时,
时,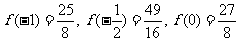
∴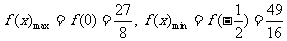 .
.
故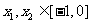 时,
时,  所以
所以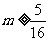 ,即
,即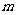 的最小值为
的最小值为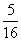 .
.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com