
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
1°¢‘⁄“ª∂®Œ¬∂»œ¬±£≥÷—π«øœ‡µ»µƒ√‹±’»›∆˜÷–£¨≥‰»Î1molA°¢2molB∑¢…˙A(g)+B(g)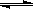 2C(g)+D(g)£¨¥ÔµΩ∆Ω∫‚ ±Aµƒ∫¨¡øŒ™w£¨œ¬¡–ŒÔ÷ ◊È∫œ≥‰»Î∏√»›∆˜÷–£¨Aµƒ∫¨¡ø»‘Œ™wµƒ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
°°°°
2C(g)+D(g)£¨¥ÔµΩ∆Ω∫‚ ±Aµƒ∫¨¡øŒ™w£¨œ¬¡–ŒÔ÷ ◊È∫œ≥‰»Î∏√»›∆˜÷–£¨Aµƒ∫¨¡ø»‘Œ™wµƒ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
°°°°
A°¢2molC+1molD°°°°°°°°°°°°°°°° B°¢1molB+2molC+1molD
C°¢1molA+1molB°°°°°°°°°°°°°°°° D°¢1molA+4molB+4molC+2molD
9°¢∑¥”¶A(g)+B(g)£ΩC(g) °˜H>0“—¥Ô∆Ω∫‚£¨…˝∏flŒ¬∂»£¨∆Ω∫‚ƒÊ“∆£¨µ±∑¥”¶“ª∂Œ ±º‰∫Û∑¥”¶”÷¥Ô∆Ω∫‚£¨‘ÚÀŸ¬ ∂‘ ±º‰µƒ«˙œflŒ™(°°)


8°¢‘⁄“ª∂®Ãıº˛œ¬£¨∂˛—ıªØ¡Ú∫Õ—ı∆¯∑¢…˙»Áœ¬∑¥”¶£∫2SO2(g)+O2(g) 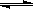 2SO3(g)°˜H£º0°°
2SO3(g)°˜H£º0°°
 (1)–¥≥ˆ∏√∑¥”¶µƒªØ—ß∆Ω∫‚≥£ ˝±Ì¥Ô ΩK£Ω_____________________
(2)ΩµµÕŒ¬∂»£¨∏√∑¥”¶K÷µ________£¨∂˛—ıªØú◊™ªØ¬ ___________£¨ªØ—ß∑¥”¶ÀŸ∂»___________(“‘…œæ˘ÃÓ‘ˆ¥Û°¢ºı–°ªÚ≤ª±‰)
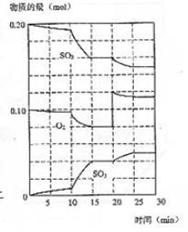
(3)600°Ê ±£¨‘⁄“ª√‹±’»›∆˜÷–£¨Ω´∂˛—ıªØú∫Õ—ı∆¯ªÏ∫œ£¨∑¥”¶π˝≥Ã÷–SO2°¢O2°¢SO3ŒÔ÷ µƒ¡ø±‰ªØ»ÁÕº£¨∑¥”¶¥¶”⁄∆Ω∫‚◊¥Ã¨µƒ ±º‰ «_________________°£
°°(4)æ›Õº≈–∂œ£¨∑¥”¶Ω¯––÷¡20min ±£¨«˙œfl∑¢…˙±‰ªØµƒ‘≠“Ú «___________________________________________(”√Œƒ◊÷±Ì¥Ô)£ª10minµΩ15minµƒ«˙œfl±‰ªØµƒ‘≠“Úø…ƒ‹ «_____________(ÃÓ–¥±‡∫≈)°£
°°A°¢º”¡À¥flªØº¡°° B°¢Àı–°»›∆˜Ãª˝
°°C°¢ΩµµÕŒ¬∂»°°°° D°¢‘ˆº”SO3µƒŒÔ÷ µƒ¡ø
(1)–¥≥ˆ∏√∑¥”¶µƒªØ—ß∆Ω∫‚≥£ ˝±Ì¥Ô ΩK£Ω_____________________
(2)ΩµµÕŒ¬∂»£¨∏√∑¥”¶K÷µ________£¨∂˛—ıªØú◊™ªØ¬ ___________£¨ªØ—ß∑¥”¶ÀŸ∂»___________(“‘…œæ˘ÃÓ‘ˆ¥Û°¢ºı–°ªÚ≤ª±‰)
(3)600°Ê ±£¨‘⁄“ª√‹±’»›∆˜÷–£¨Ω´∂˛—ıªØú∫Õ—ı∆¯ªÏ∫œ£¨∑¥”¶π˝≥Ã÷–SO2°¢O2°¢SO3ŒÔ÷ µƒ¡ø±‰ªØ»ÁÕº£¨∑¥”¶¥¶”⁄∆Ω∫‚◊¥Ã¨µƒ ±º‰ «_________________°£
°°(4)æ›Õº≈–∂œ£¨∑¥”¶Ω¯––÷¡20min ±£¨«˙œfl∑¢…˙±‰ªØµƒ‘≠“Ú «___________________________________________(”√Œƒ◊÷±Ì¥Ô)£ª10minµΩ15minµƒ«˙œfl±‰ªØµƒ‘≠“Úø…ƒ‹ «_____________(ÃÓ–¥±‡∫≈)°£
°°A°¢º”¡À¥flªØº¡°° B°¢Àı–°»›∆˜Ãª˝
°°C°¢ΩµµÕŒ¬∂»°°°° D°¢‘ˆº”SO3µƒŒÔ÷ µƒ¡ø
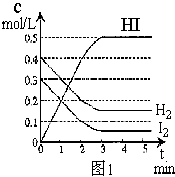
7°¢‘⁄ƒ≥“ª»›ª˝Œ™2Lµƒ√‹±’»›∆˜ƒ⁄£¨º”»Î0.8molµƒH2∫Õ0.6molµƒI2£¨‘⁄“ª∂®µƒÃıº˛œ¬∑¢…˙»Áœ¬∑¥”¶£∫
H2(g)+I2(g) 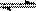 2HI(g)°° °°°˜H£º0
∑¥”¶÷–∏˜ŒÔ÷ µƒ≈®∂»ÀÊ ±º‰±‰ªØ«Èøˆ»ÁÕº1£∫
(1)∏√∑¥”¶µƒªØ—ß∆Ω∫‚≥£ ˝±Ì¥Ô ΩŒ™____________£ª
(2)∏˘æ›Õº1 ˝æ›£¨∑¥”¶ø™ º÷¡¥ÔµΩ∆Ω∫‚ ±£¨∆Ωæ˘ÀŸ¬ v(HI)Œ™______________________£ª
(3)∑¥”¶¥ÔµΩ∆Ω∫‚∫Û£¨µ⁄8∑÷÷” ±£∫
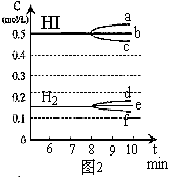
¢Ÿ»Ù…˝∏flŒ¬∂»£¨ªØ—ß∆Ω∫‚≥£ ˝K(ÃÓ–¥‘ˆ¥Û°¢ºı–°ªÚ≤ª±‰)HI≈®∂»µƒ±‰ªØ’˝»∑_________________£ª
(”√Õº2÷–a-cµƒ±‡∫≈ªÿ¥)
¢⁄»Ùº”»ÎI2£¨H2≈®∂»µƒ±‰ªØ’˝»∑µƒ «____________________°£(”√Õº2÷–d-fµƒ±‡∫≈ªÿ¥)
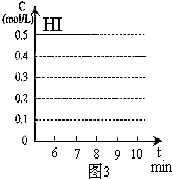
(4)∑¥”¶¥ÔµΩ∆Ω∫‚∫Û£¨µ⁄8∑÷÷” ±£¨»Ù∑¥»›∆˜µƒ»›ª˝¿©¥Û“ª±∂£¨«Î‘⁄Õº3÷–ª≠≥ˆ8∑÷÷”∫ÛHI≈®∂»µƒ±‰ªØ«Èøˆ°£
2HI(g)°° °°°˜H£º0
∑¥”¶÷–∏˜ŒÔ÷ µƒ≈®∂»ÀÊ ±º‰±‰ªØ«Èøˆ»ÁÕº1£∫
(1)∏√∑¥”¶µƒªØ—ß∆Ω∫‚≥£ ˝±Ì¥Ô ΩŒ™____________£ª
(2)∏˘æ›Õº1 ˝æ›£¨∑¥”¶ø™ º÷¡¥ÔµΩ∆Ω∫‚ ±£¨∆Ωæ˘ÀŸ¬ v(HI)Œ™______________________£ª
(3)∑¥”¶¥ÔµΩ∆Ω∫‚∫Û£¨µ⁄8∑÷÷” ±£∫
¢Ÿ»Ù…˝∏flŒ¬∂»£¨ªØ—ß∆Ω∫‚≥£ ˝K(ÃÓ–¥‘ˆ¥Û°¢ºı–°ªÚ≤ª±‰)HI≈®∂»µƒ±‰ªØ’˝»∑_________________£ª
(”√Õº2÷–a-cµƒ±‡∫≈ªÿ¥)
¢⁄»Ùº”»ÎI2£¨H2≈®∂»µƒ±‰ªØ’˝»∑µƒ «____________________°£(”√Õº2÷–d-fµƒ±‡∫≈ªÿ¥)
(4)∑¥”¶¥ÔµΩ∆Ω∫‚∫Û£¨µ⁄8∑÷÷” ±£¨»Ù∑¥»›∆˜µƒ»›ª˝¿©¥Û“ª±∂£¨«Î‘⁄Õº3÷–ª≠≥ˆ8∑÷÷”∫ÛHI≈®∂»µƒ±‰ªØ«Èøˆ°£
 °°°°
°°°°
 °°°°
°°°°
6°¢ ”“Õº «Œ¬∂»∫Õ—π«ø∂‘X+Y
”“Õº «Œ¬∂»∫Õ—π«ø∂‘X+Y 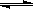 2Z∑¥”¶”∞œÏµƒ æ“‚Õº°£Õº÷–∫·◊¯±Í±Ì æ∆Ω∫‚ªÏ∫œ∆¯ÃÂ÷–ZµƒÃª˝∑÷ ˝°£œ¬¡–– ˆ’˝»∑µƒ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
(°°°° )
°°A°° X∫ÕY÷–÷ª”–“ª÷÷Œ™∆¯Ã¨£¨ZŒ™∆¯Ã¨
°°B°° X°¢Y°¢Zæ˘Œ™∆¯Ã¨
°°C°°…œ ˆø…ƒÊ∑¥”¶µƒ’˝∑¥”¶Œ™∑≈»»∑¥”¶
°°D°°…œ ˆ∑¥”¶µƒƒÊ∑¥”¶µƒ¶§H>0
2Z∑¥”¶”∞œÏµƒ æ“‚Õº°£Õº÷–∫·◊¯±Í±Ì æ∆Ω∫‚ªÏ∫œ∆¯ÃÂ÷–ZµƒÃª˝∑÷ ˝°£œ¬¡–– ˆ’˝»∑µƒ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
(°°°° )
°°A°° X∫ÕY÷–÷ª”–“ª÷÷Œ™∆¯Ã¨£¨ZŒ™∆¯Ã¨
°°B°° X°¢Y°¢Zæ˘Œ™∆¯Ã¨
°°C°°…œ ˆø…ƒÊ∑¥”¶µƒ’˝∑¥”¶Œ™∑≈»»∑¥”¶
°°D°°…œ ˆ∑¥”¶µƒƒÊ∑¥”¶µƒ¶§H>0
5°¢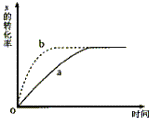 ”“Õº«˙œfla±Ì æ∑≈»»∑¥”¶X(g)+Y(g)
”“Õº«˙œfla±Ì æ∑≈»»∑¥”¶X(g)+Y(g) 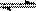 Z(g)+M(g)+N(s)Ω¯––π˝≥Ã÷–Xµƒ◊™ªØ¬ ÀÊ ±º‰±‰ªØµƒπÿœµ°£»Ù“™∏ƒ±‰∆ ºÃıº˛£¨ π∑¥”¶π˝≥Ã∞¥b«˙œflΩ¯––£¨ø…≤…»°µƒ¥Î © «°°°°°°°°°°°°°°°°°°°°°°°°
A°¢…˝∏flŒ¬∂» °°B°¢º”¥ÛXµƒÕ∂»Î¡ø°° C°¢º”¥flªØº¡°°
Z(g)+M(g)+N(s)Ω¯––π˝≥Ã÷–Xµƒ◊™ªØ¬ ÀÊ ±º‰±‰ªØµƒπÿœµ°£»Ù“™∏ƒ±‰∆ ºÃıº˛£¨ π∑¥”¶π˝≥Ã∞¥b«˙œflΩ¯––£¨ø…≤…»°µƒ¥Î © «°°°°°°°°°°°°°°°°°°°°°°°°
A°¢…˝∏flŒ¬∂» °°B°¢º”¥ÛXµƒÕ∂»Î¡ø°° C°¢º”¥flªØº¡°°
D°¢‘ˆ¥Ûê˝
4°¢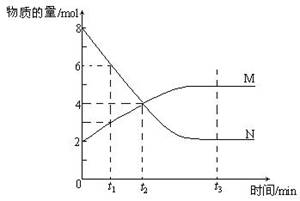 ‘⁄“ª∂®Œ¬∂»œ¬£¨»›∆˜ƒ⁄ƒ≥“ª∑¥”¶÷–M°¢NµƒŒÔ÷ µƒ¡øÀÊ∑¥”¶ ±º‰±‰ªØµƒ«˙œfl»Áœ¬Õº£¨œ¬¡–±Ì ˆ÷–’˝»∑µƒ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
°°A£Æ∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™£∫2 M
‘⁄“ª∂®Œ¬∂»œ¬£¨»›∆˜ƒ⁄ƒ≥“ª∑¥”¶÷–M°¢NµƒŒÔ÷ µƒ¡øÀÊ∑¥”¶ ±º‰±‰ªØµƒ«˙œfl»Áœ¬Õº£¨œ¬¡–±Ì ˆ÷–’˝»∑µƒ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
°°A£Æ∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™£∫2 M 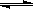 N
°°B£Æt2 ±£¨’˝ƒÊ∑¥”¶ÀŸ¬ œ‡µ»£¨¥ÔµΩ∆Ω∫‚°°
°°C£Æt3 ±£¨’˝∑¥”¶ÀŸ¬ ¥Û”⁄ƒÊ∑¥”¶ÀŸ¬ °°°°
°°D£Æt1 ±£¨Nµƒ≈®∂» «M≈®∂»µƒ2±∂
N
°°B£Æt2 ±£¨’˝ƒÊ∑¥”¶ÀŸ¬ œ‡µ»£¨¥ÔµΩ∆Ω∫‚°°
°°C£Æt3 ±£¨’˝∑¥”¶ÀŸ¬ ¥Û”⁄ƒÊ∑¥”¶ÀŸ¬ °°°°
°°D£Æt1 ±£¨Nµƒ≈®∂» «M≈®∂»µƒ2±∂
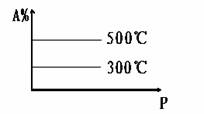
3°¢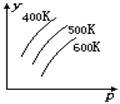 Õº÷–±Ì æÕ‚ΩÁÃıº˛(T°¢P)µƒ±‰ªØ∂‘œ¬¡–∑¥”¶µƒ”∞œÏ£∫°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
Õº÷–±Ì æÕ‚ΩÁÃıº˛(T°¢P)µƒ±‰ªØ∂‘œ¬¡–∑¥”¶µƒ”∞œÏ£∫°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°
L(s)+G(g) 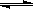 °°2R(g);°˜H>0 £¨y ÷·±Ì 浃 «
°°2R(g);°˜H>0 £¨y ÷·±Ì 浃 «
(A) ∆Ω∫‚ ±£¨ªÏ∫œ∆¯÷–Rµƒ∞Ÿ∑÷∫¨¡ø
(B) ∆Ω∫‚ ±£¨ªÏ∫œ∆¯÷–Gµƒ∞Ÿ∑÷∫¨¡ø
(C) Gµƒ◊™ªØ¬
(D) Lµƒ◊™ªØ¬
2°¢∂‘”⁄∑¥”¶mA(g)+nB(g) 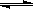 pC(g)+qD(g)°°°°°°°°
pC(g)+qD(g)°°°°°°°°
∏˘æ›œ¬ÕºÕ∆∂œ:’˝∑¥”¶Œ™°°°°°°°°°° ∑¥”¶£¨m+n°°°° p+q
1°¢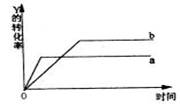 ∑¥”¶X(g)+Y(g)
∑¥”¶X(g)+Y(g)  °°2Z(g); °˜H<0,‘⁄“ª∂®Ãıº˛œ¬£¨
°°2Z(g); °˜H<0,‘⁄“ª∂®Ãıº˛œ¬£¨
∑¥”¶ŒÔYµƒ◊™ªØ¬ ”Î∑¥”¶ ±º‰(t)µƒπÿœµ»Á”“œ¬ÕºÀ˘ æ°£»Ù π«˙œfla±‰Œ™«˙œflbø…≤…»°µƒ¥Î © «°°°°°°°°°°°°°°°° (°°°° )
A º”¥flªØº¡°°
 B ΩµµÕŒ¬∂»°°
B ΩµµÕŒ¬∂»°°
C ‘ˆ¥Û—π«ø°°
D ‘ˆ¥ÛYµƒ≈®∂»
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒfi÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com