
题目列表(包括答案和解析)
24.已知:2H2(g)+ O2(g)=2H2O(l) ΔH=-571.6kJ· mol-1
CH4(g)+ 2O2(g)=CO2(g)+2H2O(l) ΔH=-890kJ· mol-1
现有H2与CH4的混合气体112L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695kJ,则原混合气体中H2与CH4的物质的量之比是( )
A.1∶1 B.1∶3 C.1∶4 D.2∶3
23.在密闭的容器中进行如下的反应:
 H2
(g)+I2(g)
H2
(g)+I2(g) 2HI(g),在温度T1和T2时,产物的量与时间的关系如右图所示,符合图象的正确的判断是( )
2HI(g),在温度T1和T2时,产物的量与时间的关系如右图所示,符合图象的正确的判断是( )
A.T1>T2,△H>0 B.T1>T2,△H<0
C.T1<T2,△H>0 D.T1<T2,△H<0
22.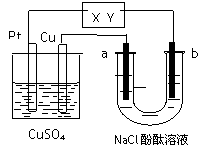 如图所示a、b都是惰性电极,通电一段时间后,a极
如图所示a、b都是惰性电极,通电一段时间后,a极
附近溶液显红色。下列说法中正确的是( )
A.X是正极,Y是负极 B.X是负极,Y是正极
C. CuSO4溶液的浓度逐渐减小 D.CuSO4溶液的pH减小
21. 阿波罗宇宙飞船上使用的是氢氧燃料电池,其电池反应为:2H2+O2=2H2O,电解液为KOH溶液,反应保持在较高温度,使生成的H2O蒸发。下列叙述正确( )
A.此电池能发出蓝色火焰
B.H2为正极,O2为负极
C.工作时,电能转化为化学能
D.电极反应为:负极2H2+4OH--4e-=4H2O;正极O2+2H2O+4e-=4OH-
20. 在密闭容器中,反应X2(g) +Y2(g) 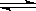 2XY(g);△H<0,达到平衡。在仅改变某一条件后,达到乙平衡,对此过程的分析正确的是.( )
2XY(g);△H<0,达到平衡。在仅改变某一条件后,达到乙平衡,对此过程的分析正确的是.( )
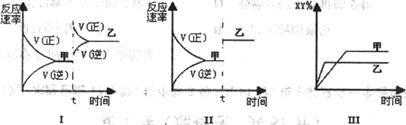
A.图I是加入适当催化剂的变化情况
B.图II是扩大容器体积的变化情况
C.图III是增大压强的变化情况
D.图III是升高温度的变化情况
19.右图所示为800 ℃ 时A、B、C三种气体在密闭容器中反应时浓度的变化,只从图上分析不能得出的结论是( )。
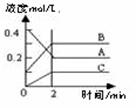 A.A是反应物
A.A是反应物
B.前2 min A的分解速率为0.1 mol·L-1·min-1
C. 达平衡后,若升高温度,平衡向正反应方向移动
D.反应的方程式为:2A (g) 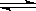 2 B(g) + C(g)
2 B(g) + C(g)
18. 下列各溶液中pH最大的是 ( )
A.pH=4的醋酸稀释100倍 B.pH=5的盐酸稀释100倍
C.pH=9的烧碱溶液稀释100倍 D.pH=9的氨水稀释100倍
17. 汽车尾气净化中的一个反应如下:
NO(g)+CO(g)⇌1/2N2(g)+CO2(g) ΔH=-373.4kJ·mol-1
在恒容的密闭容器中,反应达到平衡后,改变某一条件,下列示意图正确的是( )

16. 下列事实一定能说明HNO2是弱电解质的是( )
①用HNO2溶液做导电性实验灯泡很暗
②HNO2和NaCl 不能发生反应
③0.1mol·L-1HNO2溶液的pH=2.1
A. ①②③ B. ②③ C. ③ D. ①③
15.已知热化学反应方程式:
Zn(s)+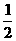 O2(g)
O2(g) ZnO(s);ΔH=-351.5 kJ·mol-1
ZnO(s);ΔH=-351.5 kJ·mol-1
Hg(l)+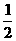 O2(g)
O2(g)
 HgO(s);ΔH=-90.8 kJ·mol-1
HgO(s);ΔH=-90.8 kJ·mol-1
则锌汞电池中热化学方程式:Zn(s)+HgO(s)  ZnO(s)+Hg(l)的ΔH为(
)
ZnO(s)+Hg(l)的ΔH为(
)
A. ΔH= +260.7 kJ·mol-1 B. ΔH= -260.7 kJ·mol-1
C. ΔH= -444.2 kJ·mol-1 D. ΔH= +444.2 kJ·mol-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com